
直到6个月前,帕克癌症免疫疗法研究所(Parker Institute for Cancer Immunotherapy)的副所长Fred Ramsdell还表示从未听说过Tessa Therapeutics这家公司。

美国时间6月18日,帕克研究所宣布将与新加坡的Tessa Therapeutics公司合作,准备跨越式进入癌症的下一代细胞疗法。这里值得提醒大家的是,帕克研究所的背后是曾任Facebook总裁,总资产逾10亿美元的传奇投资人Sean Parker先生。
而且在这项合作中,像Fred Hutch癌症中心的Phil Greenberg和斯坦福大学的Crystal Mackall等大咖级免疫治疗专家也参与到了Tessa的研究团队,由首席科学官John Connolly和首席营销官Han Chong Toh(新加坡国家癌症中心的副主任,也是该地区最顶尖的癌症研究人员之一)领导。
目前TessaTherapeutics公司正在进行的一项III期(NCT02578641)临床试验,希望能在该领域开辟新的篇章,以期与迄今主导免疫治疗领域的领导者们共享焦点。显然,免疫治疗领域的CAR-T细胞疗法一直占据着这个主导地位,新闻热度居高不下。Ramsdell对此表示:“那太棒了!Tessa正在做的研究是不同于CAR-T的。”
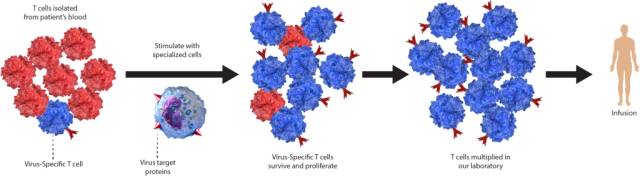
Virus-Specific T Cell (VST) Platform,来源于Tessa官网
Tessa公司所采取的技术并不是提取T细胞并对其重新设计以追捕和杀死癌细胞。而是通过扩增病毒特异性T细胞来靶向病毒相关的肿瘤,例如鼻咽癌、宫颈癌和头颈部癌等。
这些癌症共同的特征就是都与特定的病毒感染有关。病毒隐藏在宿主细胞内,引起改变最终导致肿瘤的形成。虽然免疫系统难以对其检测,但病毒会在肿瘤表面表达一些蛋白质。这些病毒抗原是VST(病毒特异性T细胞)平台治疗的主要目标。
与化疗或常规药物不同,VST治疗是一种基于每个患者个体和独特免疫系统的活体治疗。患者接受的是活细胞功能并能够对癌症作出反应的T细胞,而且这种治疗方式能够在患者体内产生持续的抗肿瘤作用。
在六月初刚刚闭幕的ASCO年会上,Tessa公布了其基于此项技术的候选产品TT10的一项II期临床试验结果,包括35例与Epstein-Barr病毒相关的4c级鼻咽癌或NPC的罕见病例。临床数据显示,2年和3年总体生存率分别为62.9%和37.1%,这与之前的临床试验相比,一线治疗晚期鼻咽癌(NPC)的生存结果是最好的。
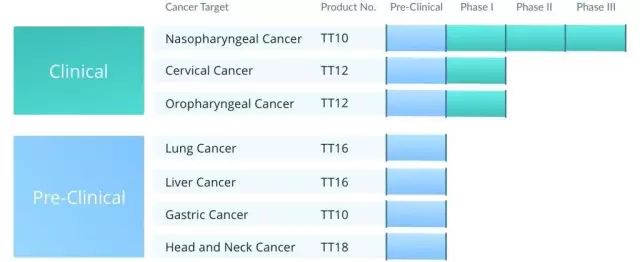
研发管线,来源于Tessa官网
III期临床结果预计将于2018年公布,到时候公司将有机会展示他们如何用Epstein-Barr病毒转染B细胞,其超越了嵌合抗原受体T细胞的随机激活,能够不断追捕和杀死特定的癌细胞,成为潜在的更有针对性的细胞治疗方式。HPV程序也可以对头部、颈部和其他癌症做同样的处理。当你开始将其与其他免疫疗法结合的时候,你就可以想象到Tessa的目标:消除实体肿瘤,夺得细胞疗法的圣杯(the Holy Grail)。
目前,Connolly和Han Chong Toh正在指导后期的项目进展,并且FDA已经授予了其快速评审通道以及孤儿药认定资格。Tessa预期这可能将是FDA批准的第一个实体瘤的细胞治疗方式。
那VST技术为何能显示出治疗实体瘤的临床安全性和疗效?这可归因于VST的以下特征:
1、毒性较小(Target Specificity-Limited Toxicity)
2、肿瘤浸润性较高(High Tumor Penetrance-Better Efficacy)
3、肿瘤逃逸可能性较低(Polyclonality-Lower Chance of Tumor Escape)
4、能够持续对抗肿瘤(Memory and Durability-Stronger Persistence)
病毒抗原作为癌症治疗的靶标,由于其特异性表达于病毒相关性癌症,而不在健康组织上表达。所以对健康细胞的附带损伤最小,毒性也最小。这从临床数据上可以反映出来,接受VST(病毒特异性T细胞)治疗的患者中副作用或并发症显著减少。
Ramsdell被这一种能够避免毒性的治疗方法所吸引。他还相信,在涉及到自然信号的情况下,更有可能创造出能够持续攻击的记忆细胞,从而引发持久的抗肿瘤反应。
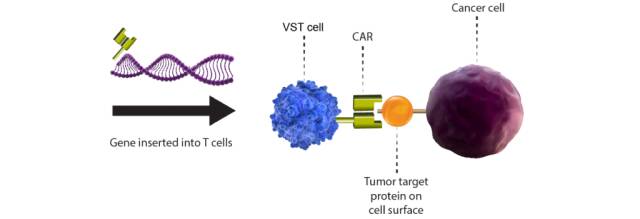
Virus-Specific T Cells &Chimeric Antigen Receptors,来源于Tessa官网
Tessa公司还开发了VST(病毒特异性T细胞)联合嵌合抗原受体技术,通过对病毒特异性T细胞(VST)进行嵌合抗原受体(CAR)修饰,从而使其能够针对多种实体瘤进行治疗。该组合平台即利用了VST的持久性和肿瘤穿透的强度,同时也保持CAR的抗原特异性和细胞毒性。
Ramsdell说:“我们非常希望将CAR-T技术推向下一代,并将有效载荷放入CAR-T等等。不得不说,针对实体瘤的免疫疗法,Tessa的技术、概念和自然科学上更加先进。”
就在几个月前,Tessa与位于美国明尼苏达州罗切斯特的Vyriad公司达成了一项合作,Vyriad公司临床阶段的产品是具有感染和破坏癌细胞的溶瘤病毒,而且还使用抗原来标记免疫系统,Tessa也将其视为抗癌的协同技术。溶瘤病毒与VST组合能够重定向针对肿瘤的有效的抗病毒和持续的免疫应答。此外,Tessa专有的溶瘤病毒已被遗传修饰以产生选择性抗体和免疫调节细胞因子,这进一步增强了T细胞的活化和肿瘤的杀伤作用。目前公司正在准备结合溶瘤病毒和VST来治疗鳞状细胞癌(头颈部癌)的一项I期临床试验。

Tessa的首席科学家John Connolly的研究团队,来源于santafenewmexican.com
另外,Tessa在3月份收购了另一家新加坡公司Euchloe,该公司一直致力于研究抗体,包括PD-1以及下一代CAR的嵌合抗原受体技术。目前Tessa正在开发的下一代VST策略,旨在克服实体瘤中存在的免疫抑制环境。这些策略之一就涉及到双特异性融合系统的开发。在CAR上通过单链可变片段(ScFV)识别肿瘤抗原时,释放出诱导分子,然后再募集额外的T细胞/ NK细胞以在次级免疫应答中攻击这些癌细胞。
Tessa公司旨在利用多管齐下的治疗方法来潜在地克服免疫抑制性实体瘤环境。这有助于为“难以治疗”的实体瘤患者提供有效的免疫治疗解决方案。虽然Tessa可能还处于全球生物技术现场首次亮相的早期阶段。但是,随着亚洲生物技术在药物开发中发挥更重要的作用,它可能已经准备要放大招了。
参考出处:
http://www.tessatherapeutics.com
https://endpts.com/billionaire-backed-parker-institute-tackles-the-holy-grail-of-cancer-rd-with-a-virtual-unknown/
http://www.parkerici.org
http://www.watertowndailytimes.com/national/coffee-meeting-in-singapore-inspires-new-way-to-kill-cancer-20170305
https://clinicaltrials.gov/ct2/show/NCT02578641
本文转载自医麦客
点击阅读原文,查看更多精彩资讯与行业报告















