▎药明
康德/
编译(来源:Immuno-Oncology Research Trends)
本文由药明康德团队整理,欢迎分享至朋友圈。转载请于文章开头注明“本文来源于药明康德微信公众号(ID:WuXiAppTecChina)”
近日,一篇讨论肿瘤免疫疗法的文章引起了许多行业人士的关注。这篇文章发表于“肿瘤免疫疗法研究趋势”网站,作者是杨森制药(Janssen Pharmaceutical Companies)的肿瘤免疫学家Nataša Obermajer博士。
在这篇文章里,作者深度讨论了两类使T细胞靶向肿瘤的方法——嵌合抗原受体(CAR)与双特异性抗体(BsAb)。
在今天的报道里,药明康德微信团队也将为各位读者整理这篇文章的核心内容。
在最新一代的肿瘤免疫疗法中,科学家们将目光投向了T细胞。利用这些细胞的肿瘤杀伤能力,我们有望设计出全新的抗癌疗法。
在过去的几年里,CAR-T细胞疗法与双特异性抗体疗法使T细胞能有效地靶向CD19等抗原,为罹患B细胞恶性癌症的患者带来了极好的缓解,也为肿瘤免疫疗法领域带来了革新。
尽管这些创新疗法带来了积极的临床效果,但它们面临着类似的问题:在血液癌症中,它们有潜在的毒性风险。而在实体瘤的治疗上,它们的疗效还尚未得到证实。为此,我们有必要了解这些疗法背后的机理与局限,以及它们在未来的应用潜力。
CAR是指一类人工合成的受体,它包括了细胞外的肿瘤抗原识别区域,以及一个用于细胞内信号通路的CD3ζ区域。
此外,CAR抗体还会包括1到2个共刺激域。当其单链可变片段(scFv)与肿瘤发生结合后,能激活T细胞受体,从而导致T细胞对表达抗原的细胞产生反应。
本文来源:药明康德
去年,美国FDA批准了两款CAR-T疗法上市,它们分别是诺华的
Kymriah
(tisagenlecleucel)与Kite Pharma(已被吉利德收购)的
Yescarta
(axicabtagene ciloleucel)。这两款CAR-T疗法都靶向致癌性B细胞表面的CD19抗原:前者治疗B细胞急性淋巴性白血病,能取得高达83%的缓解率;后者则在B细胞非霍奇金淋巴瘤的治疗中,取得了72%的缓解率。
在这两款疗法之外,还有不少CAR-T疗法正在开发之中,它们来自Juno Therapeutics,Celgene,bluebird bio,Mustang Bio,Servier,Pfizer,Cellectis,以及Celyad等生物医药公司。
不同研发人员开发的CAR-T疗法,其CAR结构可以很多样化,细胞外结构域,跨膜结构域,以及细胞质结构域都能有所区别。

▲CAR分子的一些设计
(图片来源:参考资料[2])
最近,一些新药研发人员也正在设计全新的CAR。
其中一些CAR-T细胞能特异性靶向肿瘤微环境,以克服肿瘤的免疫抑制效果。
举例来说,IL4R细胞外结构域与IL7R细胞内结构域的融合,可以靶向细胞因子,从而让T细胞在抑制性细胞因子IL4存在的情况下,依然可以得到激活和增殖;此外,表达趋化因子受体CCR2b的CAR-T细胞也能靶向肿瘤表面高度表达的CCL2;一些CAR能靶向肿瘤血管上过量表达的VEGFR2或αvβ3,增强CAR-T细胞对肿瘤的穿透能力;还有一些新颖的疗法可以将CAR-T细胞作为特定细胞因子或共刺激因子的递送者,增强内源效应T细胞的浸润。
在CAR之外,另一个使用单链可变片段(scFv)技术的新领域是双特异性抗体。
在上世纪80年代中期,人们造出了首个能将T细胞导向特定抗原的双特异性抗体。自那以后,双特异性抗体领域取得了快速的发展。
到2017年,这一领域的论文总数已经超过了2500篇。目前,绝大部分的双特异性抗体是通过DNA重组技术来生成的,而通过化学方法将两个单克隆抗体进行交联的技术也在一些研究中证明了其可行性。在这一领域的蓬勃发展下,大量双特异性抗体正在临床前和临床试验中验证它们的潜力。通过将T细胞直接引导至靶向细胞,这些T细胞的激活将不受MHC的限制,也不需要依赖于天然T细胞受体的特异性。
双特异性抗体的构型有许多种。一些研究表明,针对某些特定的抗原,某种构型可能表现更佳。
但通常意义上说,一种结构是不足以满足所有需求的。
这是因为单克隆抗体的互动、抗原上的表位位置、以及抗原在靶向细胞表面的密度与运动性,都会影响到T细胞的激活。
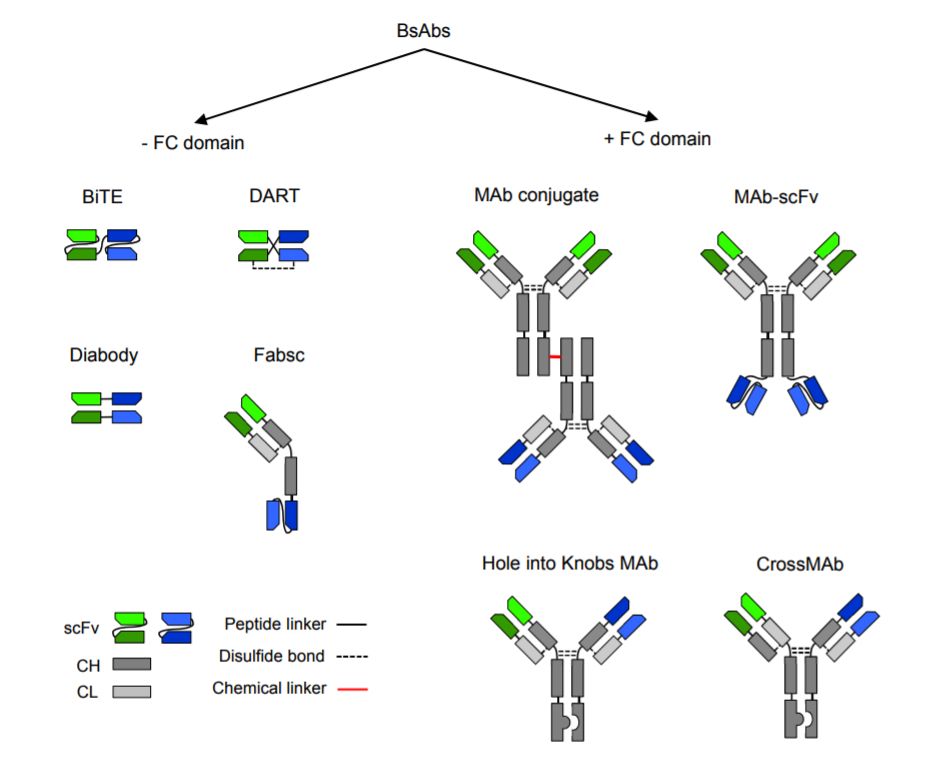
▲一些双特异性抗体的设计
(图片来源:参考资料[3])
在诸多双特异性抗体中,许多研究人员对双特异性T细胞接头(BiTEs)有独特的兴趣。
这是一类重组的双特异性蛋白,具有两个相连的单链可变片段,其中一个靶向T细胞表面的分子(如CD3ε),另一个靶向癌细胞表面的抗原。这两种单链可变片段被灵活地连接在一起。
2014年,美国FDA批准了能够针对CD19的BiTE分子Blincyto®(blinatumomab),用于费城染色体阴性的复发或难治性B细胞前体急性淋巴性白血病(ALL)的治疗。Blinatumomab由VL-VH向的抗CD19单链可变片段,与VH-VL向的抗CD3单链可变片段,通过G4S连接。
由于分子体积较小,这些BiTE的半衰期只有1.25小时。
为了克服这一限制,人们正在研究一些新的方法,譬如将BiTE连接到重链片段,或是做出其他新的设计,以提高它在血清里的半衰期。此外,它也能通过连续的输注治疗,确保体内的浓度。
本文来源:药明康德
最近,行业对BiTE的体内制造产生了兴趣。
其一大策略是通过基因改造的T细胞来产生BiTE,这能克服其半衰期较短的问题。另一种方法是使用溶瘤病毒来表达BiTE。
与此同时,研究人员们也指出了BiTE的一大挑战:它的活性取决于肿瘤部位的T细胞种类和密度。倘若这些T细胞都已经耗竭,或都是调节性T细胞,就会影响到BiTE的效果。
另一种双特异性抗体——
双链抗体(diabody)
是由两条链组成的双价分子,每一条链都具有VH和VL结构域。在双链抗体中,两个可变结构域通过较短的连接子(如G4S)相连。也正是由于这些连接序列较短,双链抗体无法通过链内重组形成抗原结合位点。相反,这两条链会以“头-尾”的方向形成双聚体,成为一个紧实的分子。如果在同一个细胞内同时表达这两条链,就有望产生双特异性的异体双聚体,带来相应的可变域(VHA-VLB / VHB-VLA,或VLA-VHB / VLB-VHA)。但此类双链抗体的一个潜在问题在于,如果形成同源双聚体,则无法带来正确的可变域(VHA / VLB或VHB / VLA)。一个替代做法是在这两条链的C端上,将半胱氨酸共价链接,
即
双亲性重靶向蛋白(dual-affinity retargeting proteins, DART)。
T细胞的亚群:
在CAR-T细胞疗法中,CD4阳性和CD8阳性的T细胞经常被混在一起进行基因编辑,插入CAR,再被输注回患者体内。
尽管CD8阳性的T细胞被认为是杀伤癌细胞的主力军,但CD4阳性的T细胞在装备了CAR之后,同样能被激活
,并显示出细胞裂解的活性。同样,在与BiTE分子共同培育时,CD8和CD4阳性的T细胞也都能被激活,诱导靶向肿瘤细胞的死亡。其中的区别在于CD8阳性的T细胞杀伤速度更快。
T细胞的表型:
现在我们知道,分化水平越低的CAR-T细胞,在体内的疗效越好。因此,研究人员们期望能尽量产生TSCM(stem memory T cell)与TCM(central memory T cell),并对其保持维持。但在BiTE领域,我们需要不同的T细胞类型。初始T细胞在BiTE的作用下,无法被激活。因此, BiTE介导的细胞毒性,需要和共刺激信号通路无关的T细胞群体参与。
本文来源:药明康德
连接的结构域:
由BiTE与CAR介导的T细胞-靶向细胞的结合在形式上有所不同。这可能是因为BiTE涉及到了天然的CD3复合体。对于BiTE来说,肿瘤相关抗原表位与靶向细胞膜之间的距离,决定了它的活性。这可能是不同双特异性抗体疗效产生差异的原因。

▲
相关阅读:
药明康德独家深度报告:免疫疗法能消灭癌症吗?
(图片来源:123RF)
T细胞的扩增:
CAR-T细胞在扩增后,可达到体内循环淋巴细胞的20%之多。而对于BiTE来说,大量曾接触过抗原的T细胞能直接加以利用,从而减少了对于细胞扩增的依赖。相比CAR-T细胞动辄扩增1000倍以上,在一些BiTE案例中,T细胞只需扩增2-4倍。这一特性有望让BiTE在实体肿瘤的治疗上更具优势。当然,这需要建立在对实体瘤进行良好穿透的前提下。
亲和性:
最初,人们认为较低的CD3亲和性(KD ~ 10 ^ -7M或以上)能避免非特异性的T细胞激活。这是因为高亲和性(KD ~ 10 ^ -9M - 10 ^ -8M或以下)的二价CD3结合可能会带来非靶向特异的T细胞激活。但后续的研究则表明这些非特异的激活可能与抗体的交联有关,而非二价结合的直接后果。
作者在文章中指出,
在T细胞疗法领域,未来主要的几大策略包括:












