正文

2017年共有237个药品被纳入药品优先审评名单,呈现出明显的地域聚集现象。
2015年8月,国务院出台《关于改革药品医疗器械审评审批制度的意见》,药品医疗器械审评审批改革大幕自此正式拉开,在近两年中取得了明显的进步。2017年10月,国务院办公厅印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,要求
加快临床急需药品和医疗器械的上市审评速度
,解决公众用药需求。
为了加强药品注册管理,
加快具有临床价值的新药和临床急需仿制药的研发上市
,解决药品注册申请积压的矛盾,CFDA在2016年2月发布了《总局关于解决药品注册申请积压实行优先审评审批的意见》,开始受理药品优先审评审批申请。2017年12月28日,CFDA发布《总局关于鼓励药品创新实行优先审评审批的意见》,同时废止原来的《总局关于解决药品注册申请积压实行优先审评审批的意见》。
截至目前,已有
436个药品
被纳入优先审评品种名单,其中2017年共有
237个药品
被纳入名单。
在2017年新纳入优先审评品种名单的药品中,
新药148个
,
仿制药89个
。
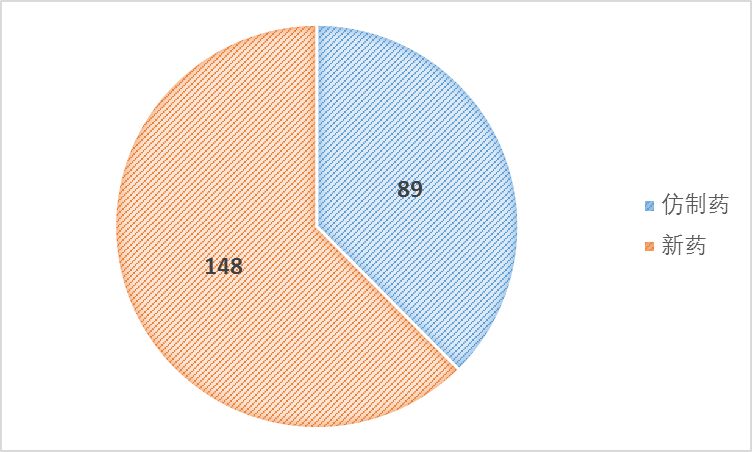
图1 2017年药品优先审评名单注册类型分布
此外,国产药品和进口药品的数量分别是130个和107个,生物制品中
进口药品占比较大
,达到60.5%,化药中国产药品占比57.4%。
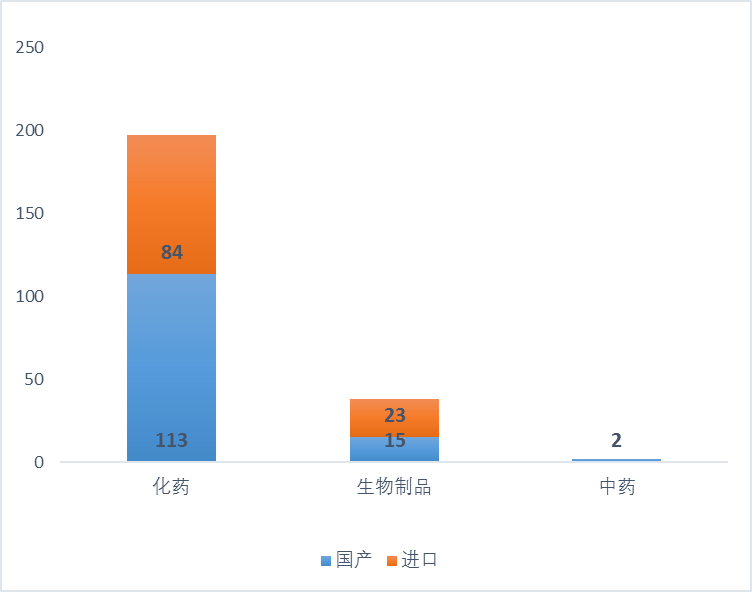
图2 2017年药品优先审评名单的药品类型分布
从地域分布来看,上海、北京、江苏、广东和浙江是数量最多的五个地区,分别是52、45、42、22和18个,占2017年总量的75.5%,从一个侧面也反映出
我国生物医药产业在环渤海地区、珠三角和长三角地区越发明显的产业集聚效应。
从企业方面来看,2017年新纳入药品优先审评名单数量最多的TOP10企业中,
本土企业和跨国药企各占一半
,其中广东东阳光药业有限公司、浙江华海药业股份有限公司和江苏恒瑞医药股份有限公司三家公司的数量最多。
表 1 2017年新纳入药品优先审评名单数量TOP10企业
|
公司名称
|
数量
|
|
广东东阳光药业有限公司
|
10
|
|
浙江华海药业股份有限公司
|
10
|
|
江苏恒瑞医药股份有限公司
|
9
|
|
拜耳医药保健有限公司
|
8
|
|
辉瑞制药有限公司
|
8
|
|
北京诺华制药有限公司
|
7
|
|
正大天晴药业集团股份有限公司
|
7
|
|
勃林格殷格翰(中国)投资有限公司
|
6
|
|
灵北(北京)医药信息咨询有限公司
|
6
|
|
石药集团欧意药业有限公司
|
6
|
东阳光药是一家专注于抗病毒、内分泌及代谢类疾病、心血管疾病等治疗领域产品开发、生产及销售的中国制药企业,2015年12月29日在
香港交易所
上市
。
目前,公司的三大主要治疗领域为抗病毒、内分泌及代谢类疾病以及心血管疾病,主要产品分别是可威(磷酸奥司他韦)胶囊剂及颗粒剂、尔同舒(苯溴马隆片)以及欧美宁(替米沙坦片)和欣海宁(苯磺酸氨氯地平片)。
在东阳光药的
10个
纳入名单的药品中,包含了克拉霉素缓释片、克拉霉素片、盐酸莫西沙星片、英莱布韦钠、英莱布韦钠片和左氧氟沙星片等几个品种。
作为中国医药国际化先导企业,华海药业是
中国首家通过美国FDA制剂质量认证并自主拥有ANDA文号的制药公司
,也是首家在美国实现规模化制剂销售的中国制药公司。2003年,华海药业在
上交所主板A股上市
。
华海药业业务覆盖化学药、生物药、医药包装、贸易流通等多个领域,产品涵盖心血管、精神类、抗病毒、抗组胺等领域,是
全球主要的心血管、精神类健康医疗产品制造商。
在华海药业的
10个
纳入名单的药品中,包含了伏立康唑片、缬沙坦氢氯噻嗪片、盐酸度洛西汀肠溶胶囊、盐酸多奈哌齐片、盐酸多奈哌齐一水合物和依非韦伦等品种。
江苏恒瑞医药股份有限公司是一家从事医药创新和高品质药品研发、生产及推广的医药健康企业,创建于1970年,2000年在
上海证券交易所上市
,是
国内知名的抗肿瘤药、手术用药和造影剂的供应商。
恒瑞医药
9个
纳入名单的药品包括了阿齐沙坦片、苯磺顺阿曲库铵注射液、地氟烷、马来酸吡咯替尼、注射用替莫唑胺和注射用紫杉醇(白蛋白结合型)等。
正大天晴药业集团是集科研、生产和销售为一体的创新型医药集团企业,是国内知名的
肝健康药物研发和生产基地
。正大天晴产品治疗领域涉及肝病、肿瘤、呼吸、感染、消化等多种疾病领域,
14个年销售过亿元的产品形成了“亿元产品群”
。其中年销售额过20亿元产品2个,分别为国家一类新药异甘草酸镁注射液(天晴甘美)和国内首家上市的恩替卡韦分散片(润众)。















