约有40%的EGFR突变阳性非小细胞肺癌(NSCLC)患者会在病程中发生中枢神经系统(CNS,脑或脑膜)转移(Rangachari et al.Lung Cancer 2015),这类患者预后不良。尽管一代和二代EGFR-TKIs对于突变患者显示出了较好的疗效,但中枢神经系统转移一直是临床治疗的难点。接受一代EGFR-TKI治疗的EGFR突变型NSCLC,约1/3的患者疾病进展是因为脑和/或脑膜转移。根据临床前研究数报道的数据,第三代EGFR-TKI奥希替尼能克服上述瓶颈。在鼠成瘤模型中,奥希替尼相比于吉非替尼,rociletinib和阿法替尼能更好穿透血脑屏障。此外,在PC9鼠脑转移成瘤模型中,奥希替尼可以诱导肿瘤持续缩小。目前,这些临床前研究数据在临床试验中得到验证。在今年的ASCO会议上,公布了奥希替尼有效控制脑转移和脑膜转移的两项研究进展。
表1. AZD9291,吉非替尼,CO-1686和阿法替尼口服剂量即血浆和脑内Cmax
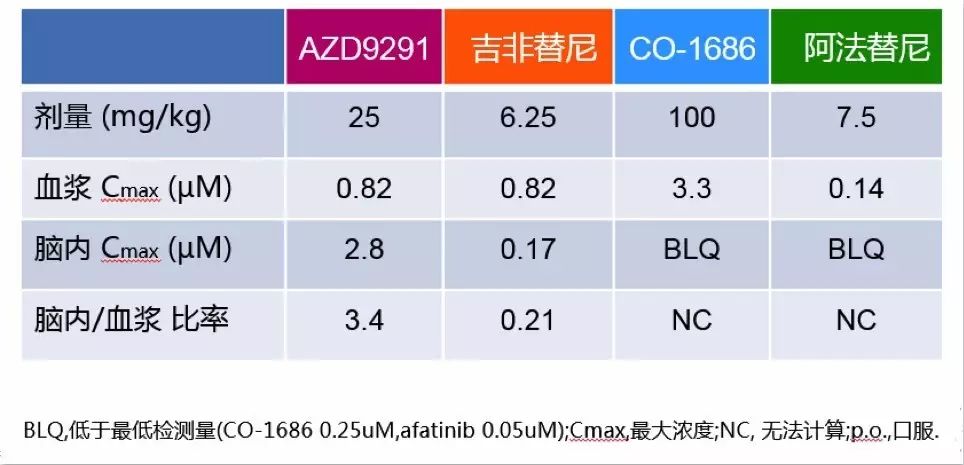
图1. AZD9291,CO-1686和对照组对小鼠PC9肿瘤生长抑制情况
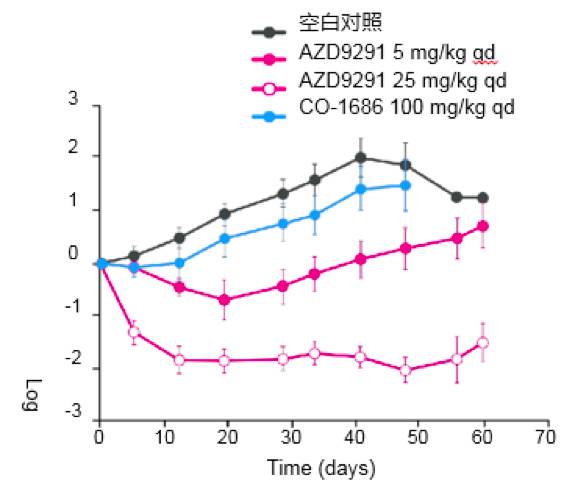
研究一:
AURA3
研究脑转移亚组分析
AURA3研究是第一个III期临床试验,证实在一线EGFR-TKI治疗进展后EGFR T790M阳性的NSCLC患者中,奥希替尼的疗效显著优于含铂双药化疗。该研究奠定了奥希替尼用于EGFR-TKI后进展,EGFR T790M突变的晚期NSCLC的标准治疗地位。既往的II期研究(AURAext及AURA2)的研究分析显示,在经一线EGFR-TKI治疗进展后EGFR T790M阳性且CNS转移的NSCLC患者中,奥希替尼治疗CNS的ORR为54%,DCR为92%。
本次ASCO大会上,Garassino教授公布了AURA3 研究中脑转移亚组的分析结果:T790M阳性的晚期NSCLC患者接受奥希替尼治疗的中枢神经系统反应。这是第一个头对头使用BICR(盲态中央评估)比较奥希替尼和化疗用于EGFR T790M突变的脑转移患者(前瞻性入组)中疗效的研究结果。
在AURA3的研究设计时即计划将对脑转移亚组进行分析,并由BICR的方法进行评估,采用RECIST v1.1标准,评价中枢神经系统的ORR, DoR和PFS。根据脑转移灶是否可测量将研究人群细分为:CNS全分析集(cFAS)--至少有≥1个可测量和/或不可测量的中枢神经系统转移灶的患者;CNS可评估疗效集(cEFR)--仅包括≥1个可测量中枢神经系统转移灶的患者。
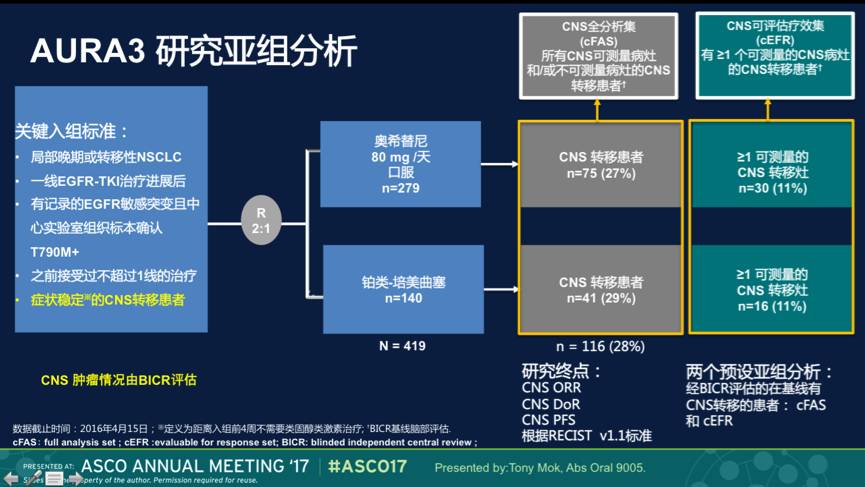
在AURA3入组的419例患者中,伴有CNS转移的患者116例(占28%,CNS全分析集),其中可评估疗效集患者46例(占11%)。在可评估疗效集中,奥希替尼组CNS 的ORR为70%(21/30; 95%CI:51-85),化疗组为31%(5/16; 95%CI:11-59),比值比(OR)为5.13; 95%CI:1.44-20.64; P= 0.015。奥希替尼组CNS的中位DoR为8.9个月 (95% CI :4.3-NC) ,化疗组为5.7个月(95%CI :NC-NC)。
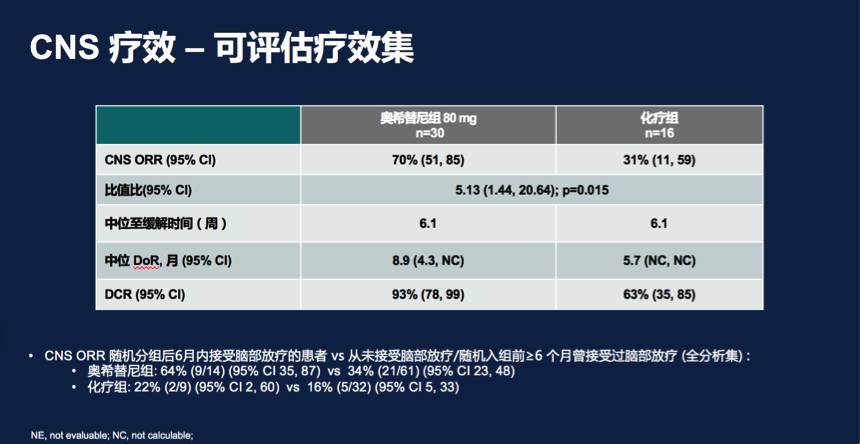
在CNS全分析集中,奥希替尼组和化疗组CNS的ORR分别为40%(30/75)和17%(7/41),OR为3.24(P= 0.014)。奥希替尼组CNS的中位PFS显著优于化疗组,分别为11.7m vs. 5.6 m,HR= 0.32; 95%CI:0.15-0.69,P= 0.004。和既往脑转移病人数据不同的是,本次公布的数据是试验预设的分组分析(而不是回顾性的分析脑转移病人数据),而且采用BICR (独立盲态中心审核)来评估进展情况。脑转移数据分成cFAS组(n=116,基线有>=1个可衡量病灶和\或有不可衡量的病灶)和cEFR组(n=46,基线有>=1个可衡量病灶)。cEFR组和cFAS组数据是不同的,值得注意。
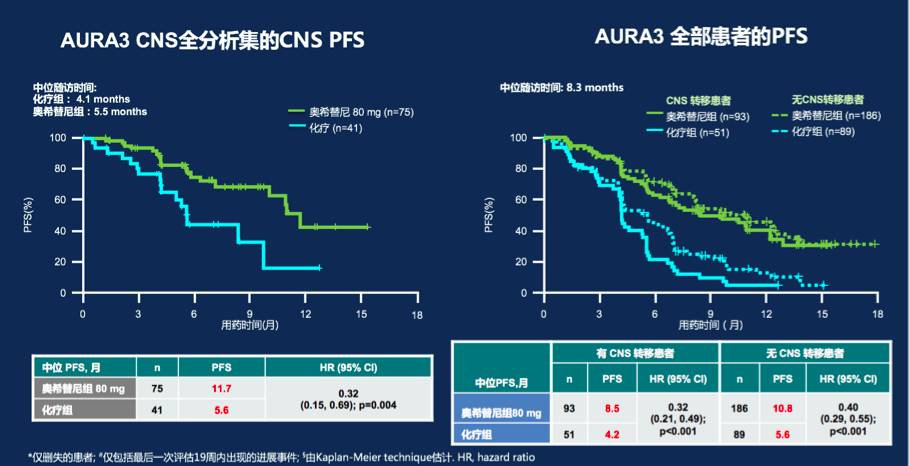
研究还同时分析了CNS全分析集中,患者在3各约及6各月时CNS进展可能性(在此时间内,患者未发生竞争风险的条件下),奥希替尼组低于化疗组。此外,奥希替尼组与化疗组的累积发病率曲线明显分开,在随访时间内,无论是CNS进展还是非CNS进展,均是奥希替尼组获益更大。
基于RANO-LM评分的独立的影像学检查回顾性分析表明:基线时,奥希替尼组中,软脑膜转移患者占CNS转移患者的7/116。7例软脑膜转移患者中的4例软脑膜病灶得到缓解,其中2 例CR,2 例PR。此外,软脑膜病灶得到缓解的患者中,同样观察到CNS及系统性病灶有获益。

研究总结:在基线伴有CNS转移的患者中,相对比于化疗,奥希替尼显著延长CNS转移患者的PFS,具有更高的 CNS ORR 。伴有CNS转移的患者,口服奥希替尼后,在6.1周时观察到CNS缓解 (可评估疗效集)。无论患者之前是否接受过脑部放疗,均可观察到CNS疗效。此外,奥希替尼组的CNS进展累积发病率更低。值得一提的是,奥希替尼在伴有软脑膜转移的患者中观察到令人鼓舞的疗效。
来自英国马斯登皇家医院的Sanjay Popat教授在现场点评道:“奥希替尼治疗CNS转移疗效显著,脑转移患者同样获得了较长的PFS。对于一代EGFR TKI耐药的患者,若EGFR T790M阳性,应该尽早接受奥希替尼治疗。”
会上,肿瘤资讯同时采访了AURA3的主要研究者之一,来自意大利的Marina Garassino教授:“在本研究中,由专门的神经科医生对脑转移患者进行评估,因此缓解率结果可能较其他研究的可信度更高。这项研究的结果与其他相关的研究结果是一致的,我们知道在前续报道的来自两项II期合并数据分析里(AURA ext和AURA2),奥希替尼的CNS缓解率为54%,而在本研究中奥希替尼的缓解率为70%。由于奥希替尼在中枢神经系统中的有效率非常高,所以在病情稳定的脑转移患者中可以首先使用奥希替尼,如果奥希替尼还不能控制脑转移灶再选择放疗。”
研究二:奥希替尼用于
EGFR
敏感突变伴软脑膜转移的
NSCLC
I期临床试验BLOOM研究旨在探索奥希替尼用于EGFR敏感突变的晚期NSCLC的安全性,可耐受性,药代动力学和初步抗肿瘤疗效。BLOOM研究剂量拓展阶段,患者接受奥希替尼160mg,qd治疗,分为两个队列:队列1入组EGFR突变型NSCLC伴软脑膜转移(LM)的患者,要求颅外病灶稳定,N=21,本次会议上报道了这一队列的更新数据。队列2入组了EGFR T790M突变型NSCLC伴软脑膜转移的患者,无论患者是否有颅外稳定病灶,N=20,目前这一队列仍在入组。

研究方法:LM活性评估基于:CSF细胞学检查(每6周一次,直至疾病进展)、中枢神经系统检查、MRI扫描(脑、脊柱)、CNS症状改善评估。 LM缓解定义为:患者至少一处可以被MRI评估且适合重复评估的CNS LM病灶,不要求有CNS可测量病灶或可测量的颅外病灶,需要4周后复查确认疗效。CSF缓解定义为:无任何进展证据,CSF中100%肿瘤细胞清除,且需要下一次CSF细胞学检查确认疗效。要求第2次CSF标本采集距离第1次CSF清除不少4周;CSF缓解率定义为:至少有1次CSF缓解的LM患者的比例。不良事件(AE)根据CTCAE分级(V4.0)评估。研究同时还采用ddPCR进行了CSF中EGFR突变DNA的定量检测。并于药物稳定状态时采集血浆及CSF标本用于药代动力学分析。
截至2017年2月3日,共有41例患者接受治疗。其中EGFR T790M状态未选择组21例(队列1);所有患者均为亚裔、转移性腺癌。入组患者的中位年龄位59岁(范围:44-75),其中男性6例,女性15例。基线神经功能状态分析,正常患者11例(52%),异常患者10例(48%)。ECOG PS评分:0/1/2/3的患者人数和比例分别为1(5)/11(52)/9(43)/0。既往接受过全脑放疗的患者12例(57%)。中位治疗线数为2线(范围1-6)。EGFR突变类型如下(患者可能同时具有多种突变):L858R/19Del/T790M的患者人数和比例分别为13(62)/9(43)/2(10)。
药物的中位持续暴露时间为12.4月(0-22月)。5例(24%)患者减量,其中4例(19%)患者是AE导致的减量。
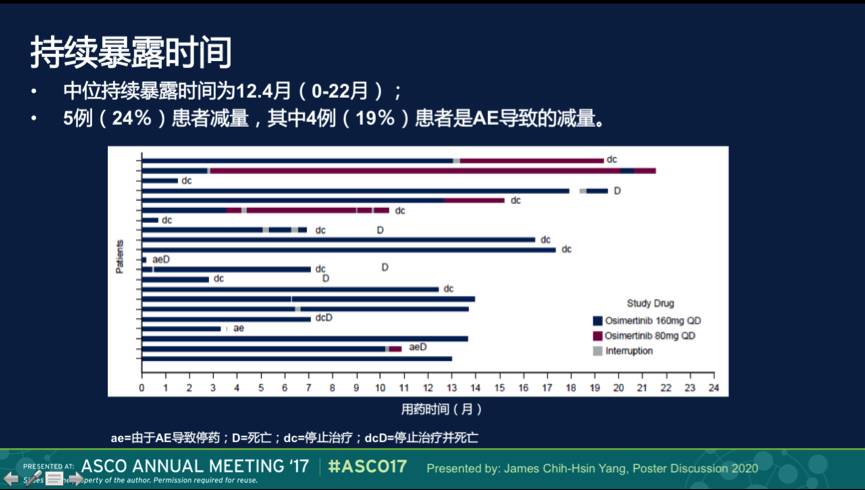
安全性分析:所有患者均出现不同程度的AE,其中13例患者(62%)≥3级;19例患者(90%)的AE研究者认为奥希替尼有关,其中5 例(24%)≥3级;6例患者(29%)出现剂量中断, 4 例患者 (19%)因AE减量, 4例患者 (19%)因AE导致剂量中止;9例患者(43%)出现SAE;3例患者 (14%) 因AE导致死亡;研究者认为无因奥希替尼药物导致死亡的患者。
影像学评估LM疗效,中位缓解持续时间:18.9月(5.6-19.3月,95% CI 11.1, NC)。
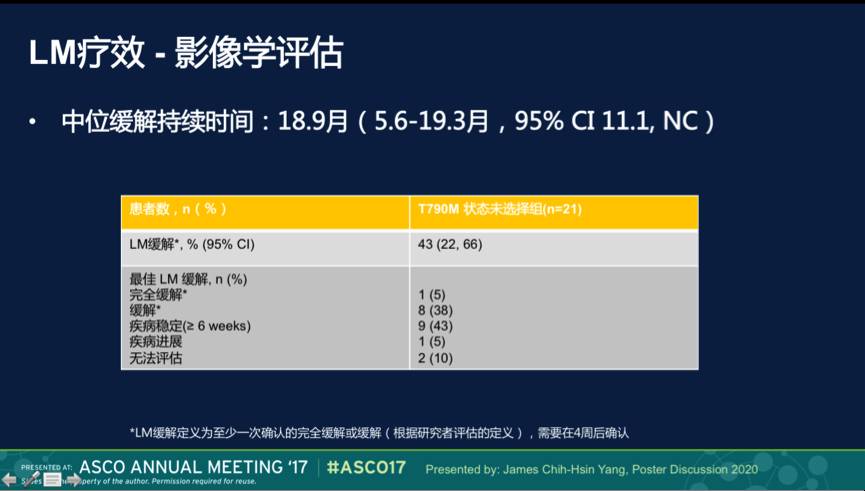
神经系统功能评估:11 例患者基线时神经系统检查正常, 其中10 例患者治疗前后神经系统检查评估无改变,1例患者由正常变为轻度异常;10例患者基线时神经系统检查异常,其中7例患者治疗后评估改善,3例患者数据缺失。
21例患者中的20例进行了CSF评估,其中6/20 (30%; 95% CI12, 54) 是经确认的CSF缓解;1例患者未进行CSF评估,是因为不符合CSF评估分析的标准,故排除在外。
探索性的药代动力学分析:稳定状态下,奥希替尼平均CSF浓度为7.5 nM (2.2–26.4 nM) (N=21);CSF中药物浓度为游离血药浓度 16.4%;平均全血中的药物浓度为884 nM,游离血药浓度为46.8 nM。奥希替尼的代谢产物 AZ5104、AZ7550 在CSF中约占奥希替尼原型的10%左右。
探索性分析CSF中EGFR突变DNA拷贝数的动态变化。15/21例患者中,从筛选期到第二周期第一天,CSF样本中EGFR突变DNA拷贝数平均减少39%;每一例患者的EGFR突变 DNA 拷贝数变化情况如下图。
图:EGFR突变DNA拷贝数 / mL (N=15)
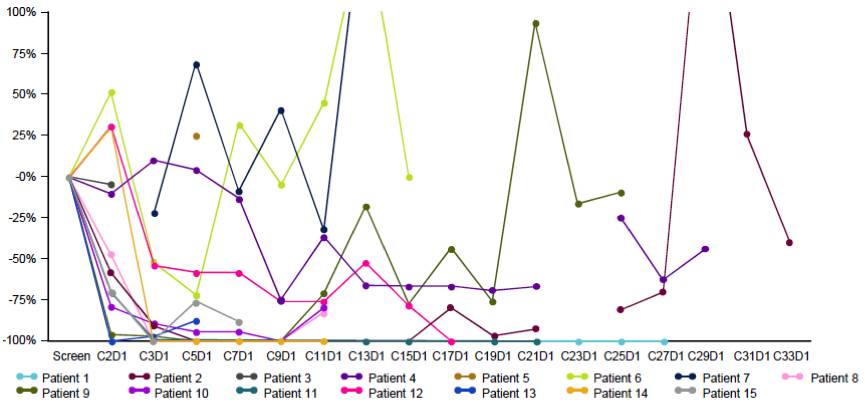
结论:在T790M状态未选择组中,奥希替尼160 mg/日可以穿透血脑屏障,平均CSF浓度为 7.5 nM 。奥希替尼160mg/日在 EGFR突变型NSCLC 伴有软脑膜转移的患者中表现出令人鼓舞的活性及良好的耐受性,LM ORR达到 43%;奥希替尼在软脑膜转移患者中的疗效尚需要大规模临床研究的验证,一经验证,奥希替尼将在软脑膜转移患者中具有巨大应用潜力;本研究仍在继续进行。
总结
脑转移在晚期NSCLC中较常见,患者的预后较差。NCCN指南推荐的治疗方案中,全脑放疗(WBRT)是脑转移治疗的重要手段,PFS约4-6月,DCR约52%。BRAIN研究挑战了脑转移传统治疗模式,首次提出对于EGFR突变伴多发脑转移的NSCLC患者,一线应用一代EGFR-TKI是推荐的首选治疗方案。第三代的EGFR-TKI 奥希替尼,相比一代和二代TKI,能更好的穿透血脑屏障,有效缓解颅内病灶。上述两项研究,分别显示了奥希替尼用于EGFR T790M阳性伴脑转移患者和EGFR突变型脑膜转移患者的显著疗效。期待BLOOM研究进一步的研究数据,真正开启肺癌脑转移治疗的新篇章。
















