5月18日,华海药业美国子公司PRINSTON的盐酸度洛西汀肠溶胶囊(20mg、30mg、60mg)获FDA批准。根据华海药业年报,2016年华海药业累计投入研发费用3.6亿人民币,同比增长33.49%,占营业收入8.89%。按照研发占比计算,华海已经跻身中我国药物研发投入前二十强。
1999年前,华海还是一个主营医药中间体制造与出口的化工企业。1999年,经当时的国家药品监督管理局批准,公司更名为浙江华海药业有限公司,营业范围扩大到药品、制剂和原料药,从此成为一家医药企业。
2003年,华海药业登陆A股,原料药和中间体为其贡献了绝大多数利润,主要产品为卡托普利、依那普利、赖诺普利、富马酸酮替芬等。那时,华海的发展战略还是紧密围绕心血管药物、抗抑郁药物、糖尿病药物、抗艾滋病药物,以医药制剂为先导,以原料药为支柱。制剂为先导彼时还是一句口号,华海药业96%的收入都来自于原料药和中间体。
中国医药工业信息中心的中国新药研发监测数据库CPM显示,华海第一个获批的原料药产品是厄贝沙坦(国药准字H20000505)。
关于批准文号:字母“H”代表 化学药品,数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,3、4位为原批准文号年份的后两位数字,后4位顺序号重新编排;例如:“19”、“20”代表2002年1月1日以前国家药品监督管理局批准的药品,原年份为“1998”、“1999”的,换发后第1、2位为“19”;原年份为“2000”、“2001”的,换发后第1、2位为“20”,第3、4位仍为原批准文号年份后两位。其它使用各省行政区划代码前两位的,为原各省级卫生行政部门批准的药品。
华海上市前的主要原料药产品有六个,凭借在生产成本以及工艺开发方面的较强优势,华海的普利类产品在国际市场上也占据了较大市场份额。

数据来源:中国医药工业信息中心 中国新药研发监测数据库CPM
2008年金融危机重创了世界经济,原料药和中间体的价格陷入低迷,以原料出口为主的华海遭遇了前所未有的危机。与此同时,以国内市场为主的企业仍保持了较大幅度的增长。2009年以来,医疗体制改革不断推进,医药行业整合和集中趋势日益明显,受国家投入增大和居民支付水平推动,国内医药行业收入和利润不断提高。华海加速了他回归国内和制剂转型的步伐。
2003年至2016年,华海有27个原料药、17个制剂品种获的批准文号。
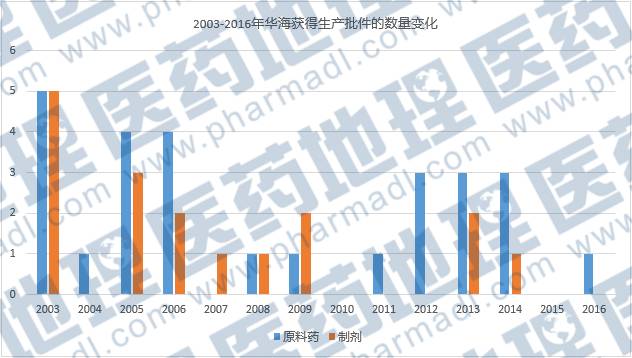
数据来源:中国医药工业信息中心 中国新药研发监测数据库CPM
受严重的仿制药审评积压影响,2010年后,华海药业有大量品种获得临床批件的时间在3年以上,2011年这种情况最为严重。2014年情况发生明显好转,但其中很重要的原因是遭遇“7·22”临床自查风暴撤回。其中也不乏一些已经在美国上市的仿制药产品,比如替米沙坦片、艾司西酞普兰、拉莫三嗪等。
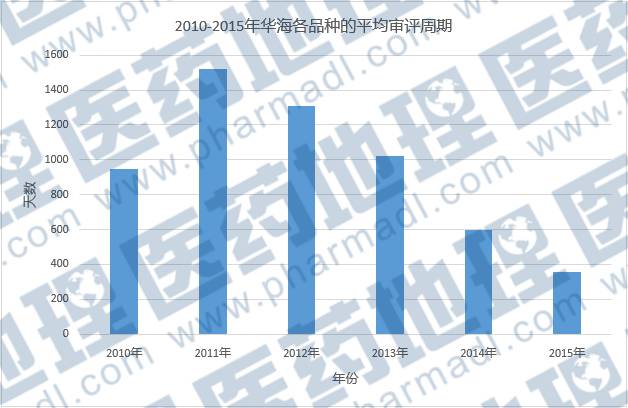
数据来源:中国医药工业信息中心 中国新药研发监测数据库CPM
目前华海处在审评流程中的品种中有18个,2个进入优先审评审批,分别是美国上市的缬沙坦片和治疗艾滋病的依非韦伦原料药。根据《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》,华海缬沙坦片上市后,如果能通过接下来的资料审核和现场核查,将视为通过仿制药一致性评价。
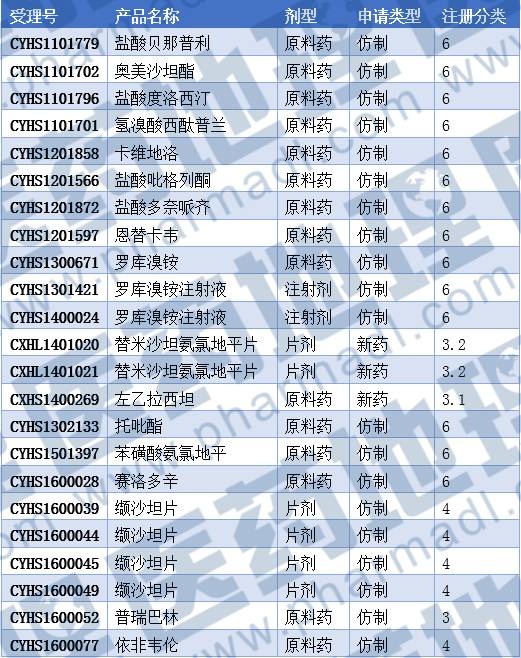
数据来源:中国医药工业信息中心 中国新药研发监测数据库CPM
除了继续加强在化学仿制药方面的优势外,华海药业也在积极布局生物药。近年来,随着生物技术的革命,各类生物大分子药物特别是抗体类药物的研发已经成为全球新药研发的热点,而新型抗体药物如抗体偶联物、双特异性抗体、纳米抗体、肿瘤免疫疗法等已经成为抗体药物研发的新趋势。2010 年-2015 年我国单抗产业 GAGR 近 50%,发展迅猛,其中单抗自身的技术优势、肿瘤治疗的巨大市场、政策利好及国外重磅单抗药物专利到期等因素是我国单抗产业高速发展的主要原因。

数据来源:中国医药工业信息中心 中国新药研发监测数据库CPM
如今,仿制药一致性评价、有限审评审批、临床试验机构备案制、允许社会资本建立临床试验机构等政策的出台和酝酿,使国内优秀的企业面临更加良性的发展环境,像华海这样已经受到欧美市场认可的仿制药企业迎来历史性的发展机遇。
















