▎药明
康德/报道
近日,
再生元(Regeneron)与赛诺菲(Sanofi )宣布,
由这两家公司合作研发的风湿性关节炎新药sarilumab(商品名Kevzara)已经获得了美国FDA的批准上市
,治疗罹患中度至重度风湿性关节炎,且先前接受过疾病缓解性抗风湿药物治疗,但缓解程度不足,或对药物出现耐受的成人患者。
值得一提的是,这是由再生元与赛诺菲这对组合带来的第三款抗体新药。在业内诸多分析师眼里,它也有望成为一款重磅药物。
▲
风湿性关节炎是一款影响广泛的疾病(图片来源:Rheumatoidarthritis.net)
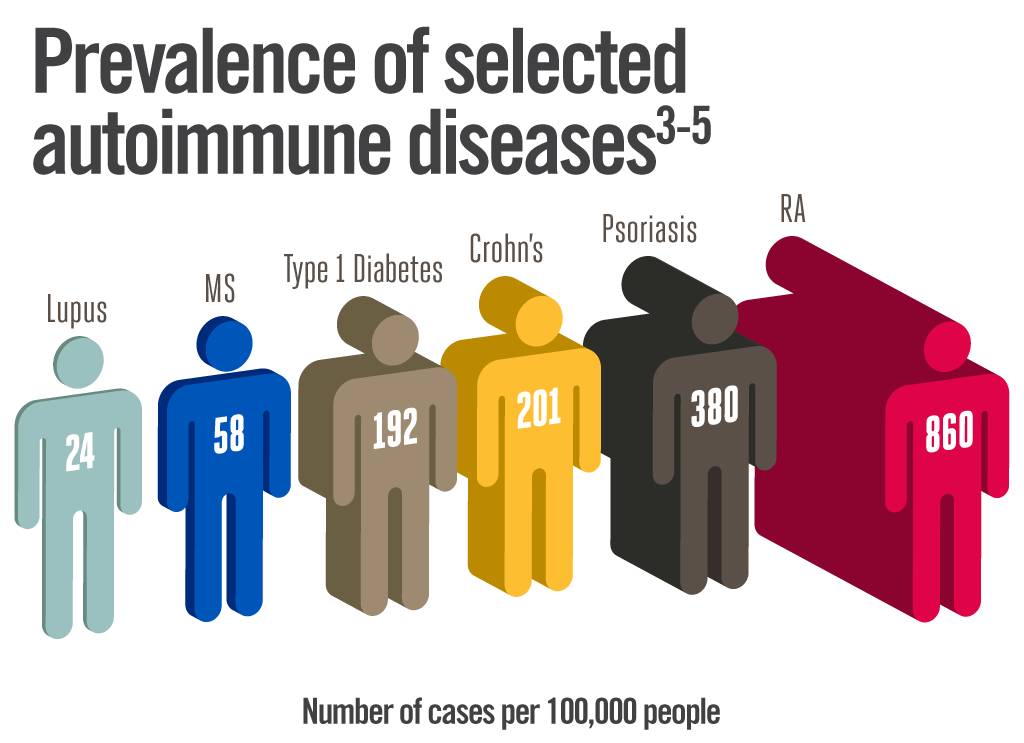
风湿性关节炎是一款慢性的自身免疫系统疾病,患者的免疫系统会攻击关节处的组织,造成炎症与疼痛,并最终导致关节受损,乃至残疾。这种疾病在任何年龄的成年人中均可出现,而尤其常见于30岁-60岁的人群。
据估计,风湿性关节炎在全球大约影响了8600万人,超过全球人口的1%。
在巨大的疾病负担面前,诸多患者们热切期盼能用上更多更好的新药。
Sarilumab是再生元与赛诺菲共同带来的人源化单抗新药
,它能结合白细胞介素-6受体,从而抑制由它介导的信号通路。
在人体中,白细胞介素-6是一种在炎症反应中扮演了重要作用了细胞因子。
当它的表达量长期高于正常水平时,就会造成一系列炎症反应,其中就包括了与风湿性关节炎有关的炎症。新药研发人员相信,倘若能抑制白细胞介素-6与受体的结合,就有望能缓解风湿性关节炎的症状。
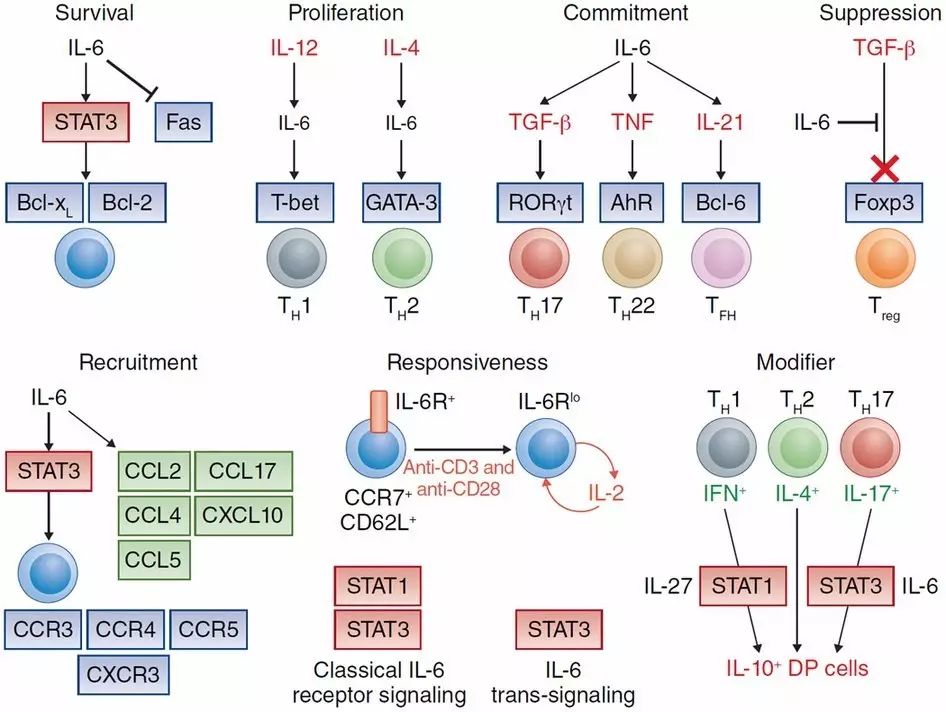
▲
IL-6在炎症反应中起到了重要作用(图片来源:《自然》)
Sarilumab的疗效与安全性在两项关键的3期临床试验中得到了验证。
在第一项名为MOBILITY的试验中,与只使用安慰剂与甲氨蝶呤的对照组相比,接受sarilumab与甲氨蝶呤联合治疗的患者症状在24周后有显著改善(
ACR20评分,200毫克组数据为66%,150毫克组数据为58%,对照组数据为33%
),抵达了主要临床终点。此外,在经治的的52周后,放射学研究发现,接受联合治疗的患者其关节损伤进展出现了显著的减少(
SHS评分,200毫克组数据为0.25,150毫克组数据为0.90,对照组数据为2.78
),这也抵达了另一项关键的临床终点。此外,接受sarilumab与甲氨蝶呤联合治疗的患者其运动能力也有更佳的改善。
在第二项名为TARGET的临床试验中,研究人员分析了sarilumab与疾病缓解性抗风湿药物联合治疗的效果。经治的24周后,与对照组相比,治疗组的患者同样出现了症状的显著改善(ACR20评分,200毫克组数据为61%,150毫克组数据为56%,对照组数据为34%),这抵达了主要临床终点。此外,他们的运动能力也有改善。

▲S
arilumab能靶向IL-6受体(图片来源:《Nature Reviews Rheumatology》)
尽管这两项有2900名成人患者参与的研究数据相当优异,sarilumab的获批上市之路却有一些小插曲。去年10月,美国FDA向再生元与赛诺菲送去了一封完全回应函,认为sarilumab的生产存在一定欠缺。在经过半年多的努力,这一欠缺终于得到了弥补, sarilumab也于昨日获批上市,
终成正果。
“在
临床试验中,sarilumab展现出了统计显著,临床有意义的改善,并能缓解症状,减少风湿性关节炎带来的结构损伤进展,并改善运动能力
,”参与sarilumab全球临床项目的负责人之一Alan Kivitz博士说:“这是非常重要的结果,因为并非所有的疗法都能对所有的患者起效。一些患者甚至花上了几年,在多种不同的疗法中来回转换,但都没有达到治疗的效果。Sarilumab和常用的生物制剂有着原理上的不同,对患者来说会是一个新选择。”

▲

















