
全麻药物作用机制的神经环路理论研究进展
杨谦梓,董海龙*
(第四军医大学西京医院麻醉科,陕西 西安 710032)
[ 摘要] 全麻药物应用于临床已近170 年,但其作用机制目前尚未完全阐明。近年来,随着神经科学的飞速发展,神经环路理论用于全麻机制的研究成为该领域的一个研究热点。研究证实,丘脑-皮质环路功能动态变化、睡眠-觉醒环路的网络调控、皮层碎片化均是麻醉导致意识消失的神经环路机制。综述全麻药物作用机制的神经环路理论研究进展,以期为全麻药物在脑内作用途径的研究提供新的理论基础。
[ 关键词] 全麻药物;意识消失;神经环路;皮层碎片化
尽管临床上麻醉医生能够熟练应用各类麻醉药品,为手术提供保障,但全麻药物如何发挥麻醉效应的具体作用机制目前尚未完全阐明。而理解全麻药物作用机制的关键在于,探究药物如何导致可逆性的意识消失(lossof consciousness,LOC)。近年来,随着各国“脑计划”的开展,神经环路理论逐渐受到重视,其在意识、认知、情绪等大脑功能及疾病等相关研究领域获得不断完善,麻醉机制与神经环路研究也取得了突破性进展。本文对全麻药物作用机制的神经环路理论研究进展作一综述,以期为全麻药物在脑内作用途径的研究提供参考。
1 神经环路用于麻醉机制研究历程
全麻药物应用于临床已有近170 年的历史,这期间有关全麻机制的研究先后经历了脂质学说(非特异性学说)、蛋白学说(特异性学说)2 个阶段,这2 个学说均曾为麻醉机制研究提供了突破性的理论贡献。然而至今,诸如全麻药物如何导致LOC 等作用机制尚未完全阐明。在分子生物学层面,已证明全麻药物作用于多个重要的蛋白离子通道,如γ-氨基丁酸(GABA)受体、N-甲基-D-天冬氨酸(NMDA)受体、乙酰胆碱(Ach)受体和双孔钾离子通道等。但从宏观角度看,全麻药物作用于这些离子通道如何产生全身麻醉效应并导致LOC 仍有待进一步研究。
近年来,神经环路理论逐渐被神经科学界所熟识,其在意识、睡眠、情感、认知等方面的研究过程中不断完善,目前认为是神经功能活动最为重要的物质基础与平台。2013 年4 月美国政府正式启动“脑计划”,该计划有一个宏伟的蓝图,即绘制人脑活动图谱、了解人脑运行机制,进而读出人们的思维活动,并推动脑部疾病检测;2014 年6 月美国国立卫生研究院(NIH)发布的脑研究计划实施路线(BRAIN 2025: AScientificVision)白皮书中,指出应该建立从突触联系到全脑的多维度神经环路图,并通过利用精确干预工具改变神经环路活动、明确大脑活动与行为之间的因果联系,从而实现对认知、情感、感知和神经疾病的深入理解。对于麻醉机制研究而言,药物如何作用于特定神经环路,从而引起LOC 这一过程则最为复杂。
实际上,神经环路理论用于全麻机制研究并不陌生,早在20 世纪40 年代就有研究报道了神经环路在麻醉和意识中的作用。Moruzzi 等发现,上行激活系统控制着动物的觉醒或清醒水平。其后大量研究显示,这个包含脑干、中脑、皮层等多种核团的神经网络体系在意识的形成中发挥重要作用,这就是神经环路理论的雏形。
2 麻醉对意识消失的影响
神经环路研究初期,研究者更多地关注与意识产生密切相关的脑区在麻醉过程中的变化。通过正电子发射体层显像(positron-emission tomography,PET)发现,LOC 过程中,除氯胺酮外,大部分麻醉剂可导致大脑的血流量显著降低,但存在脑区差异。丙泊酚、七氟烷、氙气可导致丘脑及中脑的上行激活系统的失活,从而分别使皮质的楔前叶、后扣带回、楔叶及额叶的某些区域不同程度失活。Bonhomme 等还发现,丙泊酚诱导麻醉后的脑血流变化虽然首先出现在躯体感觉皮质, 但只有当丘脑的血流发生改变后才会导致LOC。
此后更多研究发现,麻醉时大脑部分区域神经元放电活动增加,而且核团活性在不同麻醉状态下呈现时空差异。此类核团分布在脑干、下丘脑、丘脑等部位,通过不同的神经递质相互调控,形成复杂的网络,共同控制皮层的信息传入与交流。目前认为与麻醉和意识密切相关的神经环路主要有3 类:丘脑-皮质环路、下丘脑睡眠-觉醒环路、皮层碎片化。
3 神经环路理论用于全麻药物作用机制研究
3.1 丘脑- 皮质环路
丘脑是上行激活系统和下行易化通路的共同通道,也是皮层-皮层神经通路的中继站,同时与下丘脑核团也有广泛联系,因此丘脑是多个神经网络的交汇口。麻醉状态下丘脑功能受到抑制,丘脑-皮质环路信息处理受限,外周信息传递至皮质的通道受阻,这有可能是麻醉导致LOC 的共同本质。
丘脑-皮质环路由丘脑中的丘脑皮质神经元(thalamocortical neuron,TC)与网状神经元(reticularneuron,RT)以及由皮层发射的皮层-丘脑神经元共同形成。目前已证实,丘脑-皮质环路是睡眠特征性脑电波—— 梭形波的物质基础,也是丙泊酚麻醉维持期特征性脑电波形——α 波的物质基础。体内电生理研究表明,动物麻醉时由于双孔钾离子通道激活或GABA 能中间神经元功能增强,可导致丘脑TC 细胞显著超极化,而丘脑与皮质之间反复相互作用导致α波强度逐渐增加,丘脑与前额叶皮质神经元放电呈现高度一致,从而影响丘脑- 皮质环路处理信息的能力。通过数学建模证实,随着丙泊酚浓度增加,清醒时的特征性脑电波γ 波和β 波可通过丘脑-皮层环路同步化逐渐融合为α 震荡,随着麻醉深度增加,α 震荡由枕叶皮质向前额叶过渡,这也是由丘脑-皮质环路同步化放电逐渐增强所导致的。
在丘脑-皮质环路中研究最多的是丘脑非特异性核团与皮质之间的关系,其中丘脑中央正中核(centralmedial thalamus,CMT)是研究最多的核团。CMT 微注射Ach 受体激动剂尼古丁,能够促使被七氟烷麻醉的大鼠恢复翻正反射,并保持觉醒状态;而清醒状态下向CMT 区域注射GABA 受体激动剂,则能使大鼠翻正反射丧失,进入类似麻醉状态。在CMT 阻断电压依赖性Kv1.2 离子通道,能够使地氟醚麻醉下的大鼠恢复意识和动作,但此现象仅在1/3 大鼠中出现,另有1/3 大鼠无觉醒反应,还有1/3 出现抽搐。关于CMT核团的TC 神经元类型目前尚未阐明,其如何影响皮质活动仍需进一步探索。目前仅有Baker 等利用局部场电位(local field potential,LFP)技术证实,丙泊酚和右美托咪定麻醉时CMT 的LFP 频率与强度变化明显早于所投射皮质,也早于丘脑特异性核团腹侧基底核,提示在丘脑-皮质环路中,丘脑可能是介导麻醉效应的调控点。
3.2 经典睡眠- 觉醒环路
随着对网状激活系统的深入研究发现,围绕下丘脑等区域存在一些特定类型的神经元,参与睡眠和觉醒调控,从而构成睡眠中枢。此类核团分泌释放觉醒相关递质,如Ach、去甲肾上腺素(NE)、5-羟色胺(5-HT)、多巴胺(DA)、组胺(His)、食欲肽(Orx)以及睡眠相关递质GABA 等。核团包括基底前脑、蓝斑核(locus coeruleus,LC)、中缝核(raphe)、结节乳头核(tuberomammillary nucleus,TMN)、下丘脑腹外侧视前核(ventrolateral preoptic area,VLPO) 等。一个核团并非只释放一种递质,同一递质系统中相互关联的核团通过投射联系构成神经通路;不同递质系统间的神经通路通过核团交汇构成调控网络。多个核团之间构成复杂的投射和调控关系,共同控制睡眠-觉醒平衡。
由于麻醉与睡眠导致LOC 的效果相似,研究者也逐渐发现麻醉与睡眠存在部分共享机制,即表现在下丘脑睡眠-觉醒网络参与麻醉效应,但又不完全相同。总体而言,GABA 系统在麻醉和睡眠诱导阶段起直接作用,其余递质或参与诱导,或影响觉醒。目前对于下丘脑神经递质环路的调控关系仍未完全阐明。
新近研究发现,TMN 核团的组胺能神经元存在GABA 受体,并受到VLPO 核团GABA 能神经元支配,但特异性敲除 TMN 组胺神经元的 GABAA 或GABAB受体,虽然 TMN 细胞在体外对丙泊酚的抑制不敏感,但体内实验并不能改变丙泊酚诱导的LOC 效应,提示TMN 组胺神经元在体内可能存在其他支配方式。另外,目前广泛认为,右美托咪定作用于LC 的NE 能神经元细胞膜肾上腺素α2 受体,减弱LC 向VLPO 的支配强度,增加GABA 释放,使TMN 释放的组胺减少,导致镇静催眠作用;然而最新研究发现,敲除LC 肾上腺素α2A 受体,仅能消除右美托咪定诱导的翻正反射消失, 但不能影响其镇静作用, 真正介导其镇静作用的是包括VLPO 在内的下丘脑视前区。笔者关注到穹隆周区(Pef)orexin 能神经系统参与觉醒,但其作用途径非常广泛,包括激活基底前脑(BF)区胆碱能神经元,从而影响麻醉后意识恢复。然而以上研究只是神经递质系统间网络调控机制的冰山一角,更复杂的相互作用途径还需要进一步探索。此外,下丘脑神经递质系统如何产生最终效应,进一步影响丘脑向皮质投射还是直接影响皮层状态,也是神经环路理论需要解决的问题之一。
3.3 皮层碎片化的神经环路
皮层一直被认为是意识产生的来源。在全麻机制研究中也发现,一些诸如氯胺酮、N2O 等药物,并不作用于GABA 递质,觉醒维持递质如Ach 的释放也不受抑制,但皮质间有效连接及功能状态受到影响。进一步研究发现,氯胺酮、N2O 可直接作用于皮质锥体神经元NMDA 受体。而Li 等研究发现,皮质单个神经元的高频簇发放电(burst spiking)可引起全脑状态改变,表现在远隔部位局部场电位(LFP)发生类似于慢波睡眠向快动眼睡眠(REM sleep)转换的改变。
此外,Lewis 等发现,丙泊酚麻醉导致人LOC时脑电图中有明显的慢波(<1Hz)出现,并认为慢波与皮层功能活性有关。进一步研究发现,慢波与α 波的相位存在密切相关性,两者相位相反时(trough-max),皮层兴奋性增加,且trough-max 更局限地分布于前扣带回及周围前脑皮质,与网状上行激活系统中的兴奋性神经投射区域一致。由此推测,慢波机制可能与α 波同源,均由于丘脑GABA 能神经元活性增强所致。
慢波出现的同时,大脑皮层的电活动在时空上呈现出“碎片化”。总体上,远距离(2 cm)皮层间的信息传送中断,而短距离(< 4 mm)皮层电活动仍保持同步。具体表现为,慢波震荡的相位在远隔皮层差异较大,局部神经元放电活动与慢波同相发生,但这种同步在远隔皮层被打破。这意味着在麻醉时,皮层被分隔成若干孤立的小岛,当某一部位皮质兴奋时,远隔部位正处于抑制状态,从而失去了皮质之间的信息交流和处理能力。
4 结语与展望
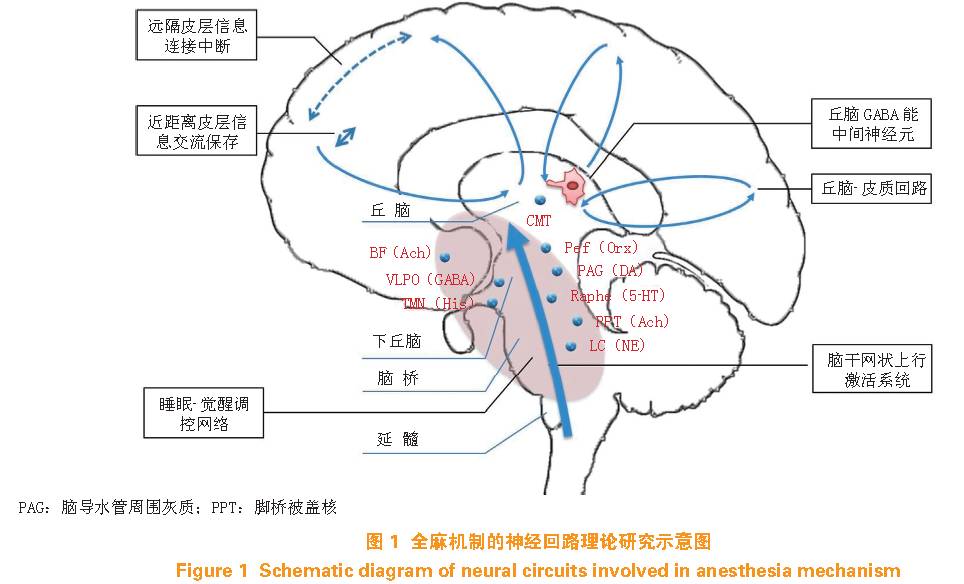
现代麻醉药物问世后,长期以来都被认为可以安全应用到临床。然而,近年来术后认知功能障碍、谵妄、麻醉神经毒性等麻醉相关并发症越来越引起医学界和社会的广泛关注,归根结底,麻醉作用机制不明是麻醉相关风险得不到解决的关键所在。目前,有关全麻机制的神经回路理论研究有:1)脑干和中脑网状结构收集来自躯体非特异性感受信息,向上传递至丘脑非特异性核团,其间受到皮质下众多核团投射,在丘脑整合后由此继续向上广泛投射至大脑皮层各个区域,形成上行激活系统,维持觉醒;2)皮质将收到的信息回馈至丘脑非特异性核团,并与上行的丘脑-皮质神经通路共同形成丘脑-皮质回路;3)在丘脑-皮质回路中,GABA 能中间神经元受麻醉药物影响,功能增强,导致丘脑TC 细胞显著超极化,并导致α 波强度逐渐增加;4)麻醉时远距离皮质间的信息交流和处理中断,而近距离皮质间联系仍保留;5)下丘脑和脑干中存在一群特殊核团,通过释放不同神经递质,调控睡眠,也参与麻醉效应(见图1)。回顾近年来有关麻醉机制的研究进展可见,神经环路理论更立体地将分子靶点、神经递质、核团联系和脑功能融为一体,为阐释麻醉药物在脑内的作用途径提供了一个更丰富的理论体系。然而深入研究发现,所有神经回路都并非独立存在,复杂的神经通路间如何合作或制约将是未来该领域研究的重点。
近几年全麻机制研究在国际上取得了突飞猛进的成果,首先得益于神经科学在技术上的突破,即功能影像、脑电记录、体外电生理等麻醉机制传统研究技术和软件得到大幅改进;同时在神经科学领域涌现诸如光遗传学、化学遗传学、钙成像等新兴生物科技,为全麻机制的研究提供了先进的技术支持,也为我们认识大脑功能、研究意识形成等科学问题提供了有力工具。其次,全麻机制引起广泛关注还有赖于学科交叉和融合带来的思想创新,神经生物学、模式动物学、分子影像学等学科相继加盟,使得多学科合作为全麻机制的研究带来创新源泉,预计这也将是全麻机制研究在未来的主要发展方向。
[ 专家介绍] 董海龙:第四军医大学西京医院麻醉科主任,教授,博士生导师,英国帝国理工大学客座教授,科技部中青年科技创新领军人才。兼任国际麻醉药理学会委员,中国麻醉药理学会副主任委员,中国心胸血管麻醉学会常务理事,中国麻醉医师协会常委,全军麻醉与手术设备质控委员会副主任委员,中华医学会麻醉学分会委员兼副秘书长等。担任Mol Neurobiol,Anesth Analg 等7 种SCI 杂志的特邀审稿人,《中华麻醉学杂志》等4 种国内核心期刊的编委。曾赴美国、英国及日本从事研究工作,被日本学术振兴会(JSPS)聘任为外国人特别研究者。近年来先后在J Clin Invest,Cereb Cortex,Anesthesiology 等国际权威杂志上发表SCI 论文77 篇。作为负责人主持国家自然科学基金(6项)、国家科技重大专项新药创制项目(2 项)等国家级及国际课题共12 项。研究成果获2005 年美国麻醉学年会青年学者旅行奖及2009 年亚太麻醉创新大奖。研究发现多次被写入麻醉学权威教科书《Miller’s Anesthesia》,《Anesthetic Pharmacology》等35 部国外英文专著。2011 年获国家自然科技进步一等奖1 项。

●感谢您阅读《药学进展》微信平台原创好文,也欢迎各位读者转载、引用。本文选自《药学进展》2017年第5期。
●《药学进展》是一本专注于医药领域前沿动态的专业媒体,月刊,铜版纸全彩印刷,全年360元,欢迎订阅!编辑部官网:www.cpupps.cn;电话:025-83271227。















