BioArt按:目前临床常用的阿司匹林、氯吡格雷等抗血小板药物对于部分糖尿病患者心脑血管并发症的治疗效果并不理想,存在阿司匹林抵抗、氯吡格雷抵抗现象,无法有效的减少心脑血管并发症的发生率。因此,明确糖尿病患者血小板异常激活和抗血小板药物抵抗背后的分子机制将有助于推动新型抗血小板药物的研发,为氯吡格雷抵抗的患者的个体化药物治疗提供重要的科学依据。近日,来自复旦大学基础医学院生物化学系丁忠仁课题组在Circulation杂志发表了题为“Platelets express activated P2Y12 receptor in patients with diabetes”的研究论文,该研究揭示了血小板上G蛋白偶联受体P2Y12受体高表达、信号通路的自发激活是糖尿病患者血小板异常激活、心脑血管疾病高发的新机制;其次,该研究还发现,与现有的抗血小板药cangrelor(坎格雷洛)相比,反向激动剂AR-C78511具有更好的抗血小板、抗血栓作用。该研究为新型抗血小板药物的研发、糖尿病患者的个体化药物治疗提供重要的科学依据。文章的第一作者为今年刚毕业的胡亮博士,通讯作者为丁忠仁教授。

论文解读:
随着我国居民生活水平的不断提高以及人口老龄化程度的不断加深,目前我国11.6%的成年人为糖尿病患者,占全球总糖尿病人数的1/4左右。有50%以上的糖尿病患者死于心脑血管并发症。血小板异常激活作为中风、冠心病等动脉血栓性疾病的重要病理基础,也是糖尿病人常规服用抗血小板药物预防心脑血管并发症的重要原因。
目前临床常用的阿司匹林、氯吡格雷等抗血小板药物对于部分糖尿病患者心脑血管并发症的治疗效果并不理想,存在阿司匹林抵抗、氯吡格雷抵抗现象,无法有效的减少心脑血管并发症的发生率。因此,明确糖尿病患者血小板异常激活和抗血小板药物抵抗背后的分子机制将有助于推动新型抗血小板药物的研发,为氯吡格雷抵抗的患者的个体化药物治疗提供重要的科学依据。
复旦大学基础医学院丁忠仁课题组与华山医院内分泌科叶红英课题组合作研究发现,糖尿病患者和糖尿病大鼠血小板上P2Y12受体表达显著增加、发生受体自发激活,在无激动剂结合的情况下向胞内传递受体激活信号,导致血小板异常激活、体内血栓形成增加。同时本研究发现,与2015年FDA新近审批上市的抗血小板新药cangrelor(坎格雷洛)相比,反向激动剂ARC-78511对于P2Y12受体高表达且自发激活的糖尿病人血小板有更好的抗血小板作用,对糖尿病大鼠具有更显著的抗血小板、抗血栓作用。利用糖尿病大鼠的巨核细胞(血小板前体)和体外高糖环境下培养的巨核细胞,本研究进一步发现ROS - NFκB信号通路激活是血小板P2Y12受体和多种炎症因子表达异常增加的幕后分子机制(下图)。
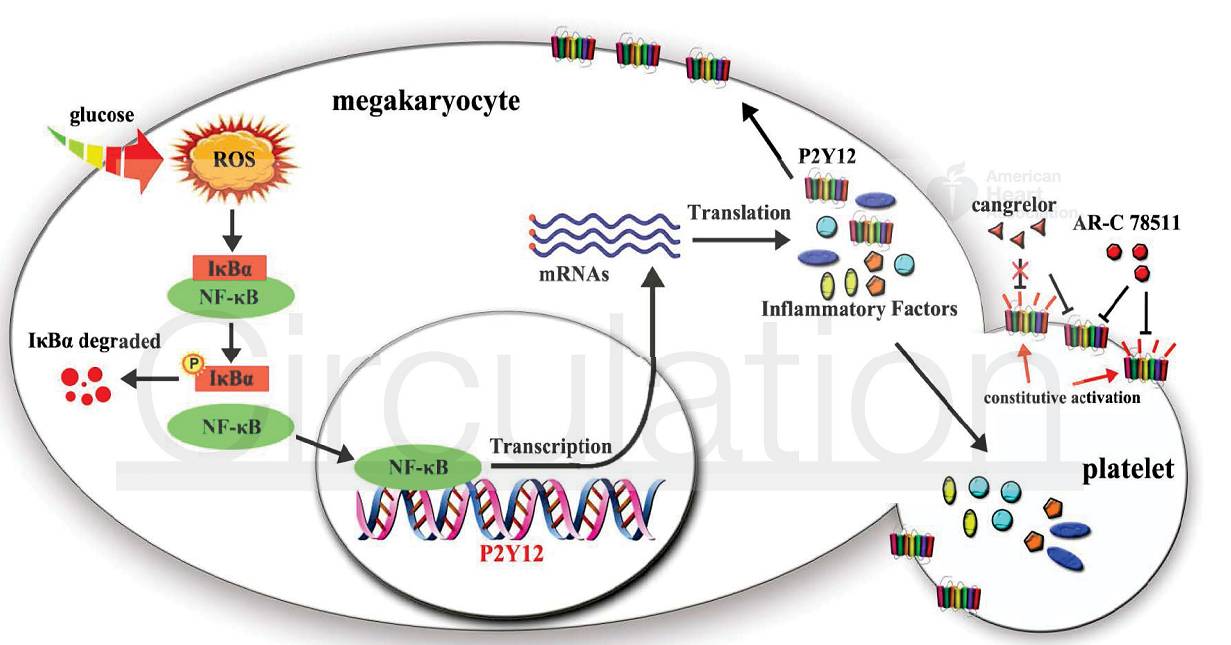
P2Y12受体作为血小板表面一种G蛋白偶联受体,在血小板激活、血栓形成中发挥重要的级联放大作用,也是抗血小板新药研发的最成功靶点。本研究首次揭示了糖尿病人血小板P2Y12受体高表达、异常激活的现象、机制、反向激动剂的治疗学优势,不但为糖尿病高发心脑血管并发症的原因找到了一条重要线索,也为抗血小板药物的研发、糖尿病患者心脑血管并发症的个体化药物治疗提供了新思路和新方向。
据悉,丁忠仁课题组长期从事血小板激活机制、抗血小板药作用机理和以P2Y12受体为靶点的抗血小板药的研发。自2008年5月份课题组成立以来,指导的研究生有多人次获得“国际血栓与止血学会(ISTH)”“Young Investigator Award”和国家奖学金,有多篇文章在Circulation 、J Thromb Haemost、Thromb Haemost上。

丁忠仁,博士,现任复旦大学基础医学院教授。1998年获中山医科大学医学博士学位,2000年8月起在在美国天普大学医学院Sol Sherry血栓研究中心从事血小板ADP受体的激活机制和以P2Y12受体为靶点的抗血小板药研究,2007年作为引进人才回复旦大学基础医学院从事教学、血小板激活机制和抗血小板药的研究工作,2008年入选首批“上海高校特聘教授(东方学者)”。先后负责国家自然科学基金面上项目4项、科技部和上海市科委新药创新基金(子课题)各1项、上海市教委人才基金2项, 指导的研究生曾在2011年的“第23届国际血栓与止血学会大会” (International Society on Thrombosis and HaemostasisⅩⅩⅢCongress, ISTH 2011)同时获得两项“青年研究学者奖”(Young Investigator Awards)。


BioArt,一心关注生命科学,只为分享更多有种、有趣、有料的信息。关注请长按上方二维码。投稿、合作、转载授权事宜请联系微信ID:fullbellies或邮箱:[email protected]。