操纵基因和细胞状态的新方法可以用于设计细胞功能,简化质量评估,提高生产工艺。这些策略有助于克服尚未解决的细胞治疗生产的挑战及将质量设计到这些复杂的细胞系统中的补充框架,最终增加患者获得存活的疗法。
细胞疗法,即用活细胞治疗患者,正被开发用于治疗各种各样毁灭性的疾病。用活细胞治疗患者,其功能取决于细胞对小环境变化的敏感特性,生产这些复杂的细胞治疗产品(CTPS)具有重大的挑战。我们最近讨论了如何运用质量源于设计(
QbD
)的框架来减少开发CTPS生产解决方案的风险(Lipsitzet al,2016)。该框架通过增加对确保产品质量和安全关键属性的了解,以及通过识别和控制这些属性可变性的来源来指导CTP生产过程的开发。然而,即使面对严格的实施框架,CTPS产品和过程开发的障碍仍然具有挑战性。这些包括确保坚实的产品功能,定量和快速的细胞鉴定以及生产工艺的成本效益。
通常,鉴定与开发前瞻性细胞治疗产品(CTPs)的主要标准总是对准临床相关的体内相应的表型,结合简单可靠的路径获得所需的细胞,或在体外生长或处理细胞的能力。
这种自底向上的方法通常不能有目的地针对特定的未满足的临床需求,而是鼓励在各种潜在的临床应用中测试现成的细胞。我们的领域花费了太多的时间和精力寻找所能培养细胞的临床应用。一种自上而下的方法确定了所需的产品概况(功能、特性和纯度,和生产工艺)所需治疗的特定指征,并进行技术实施形成这些先验设计的CTPs,应加快CTP的影响和效果(图1)。目标产物分析是制药行业和美国
FDA 10年来认可的工具(见网站资源),它仍然是构建过程开发的战略开发工具。虽然该工具最初用于药物开发,但该工具也作为优质的,生产合成细胞治疗产品(CTPs)的基础。
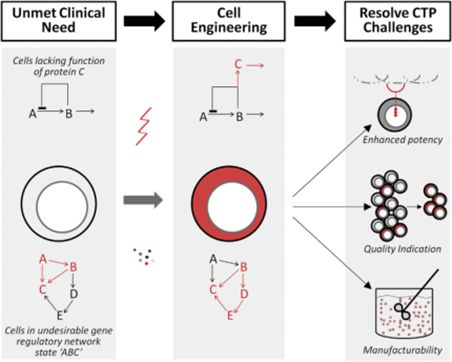
图
1.
用现有的细胞类型设计的治疗方法不能解决未实现的临床需求
治疗可能缺乏所需的功能(蛋白质的“c”功能)或存在于一个不良的基因调控网络的状态(状态“ABC”)。工程细胞工具包括基因操作(如将基因C插入细胞)或细胞状态操纵(细胞因子诱导的转换到基因调控网络的“BCDE”)。这些策略可以解决的挑战包括新的CTP功能设计(如针对肿瘤特异性抗原免疫细胞的一个新受体),简化质量评估,在混杂培养中指示或选择所期望的细胞群,通过产生通用供体或强大扩增的细胞群来增强细胞的可制造性。这些更改用红色表示。
蛋白质生产商已经设计了细胞系和蛋白质的生产来提高蛋白质产量,包括通过控制关键基因的开关机制、使细胞适应最小生长因子的要求、以及策划蛋白质以简化下游处理(如图2)。在细胞治疗中,这些解决方案在概念上很少适用,可能是由于对治疗细胞的基础生物学控制行为缺乏了解,以及担心“人造”细胞的建立不适合当前的监管框架。在生物制药、细胞工程中,当设计的细胞产生治疗蛋白时,细胞工程至少是从产品中去除的一步
。
然而,在细胞治疗中,工程化细胞本身将直接与患者相互影响
,
表明额外的安全考虑是必要的。
近来细胞工程的最新进展和临床促动了重新审视这种模式以加速CTP的发展。在此,我们讨论了与用户自定义属性相关的新细胞类型设计的进展、机遇和监管视角以增强治疗功能、简化质量评估并提高生产工艺
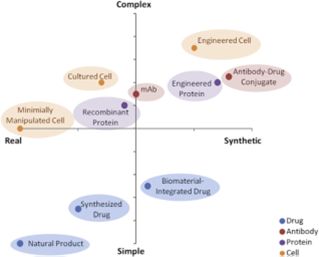
图
2.
与其他疗法相比,细胞治疗产品的(
CTPs
)复杂性和合成特性的范围
通过细胞工程合成的细胞治疗,代表合理的下一步,其他治疗类型已经取得进展。正如小分子药物从天然产物通过合成药物发展到合成的、生物的集成药物的进展一样,因此细胞治疗也从最小操作细胞发展到培养的细胞,现在又发展到工程化细胞。这些策略的一个关键区别是相对于小分子药物和大多数生物制品而言,工程细胞的复杂性增加了。然而,合成疗法发展的充足先例,体现在其他先进疗法中,包括各种抗体药物偶联物和工程蛋白产品。
CTPS大多设计为“同源性”使用,来实现与体内类似的功能。增加或提高CTPS自然功能以产生针对未满足临床需要的细胞已经成为一个令人兴奋的机会。
最近使用嵌合抗原受体的T细胞(CAR-T)的临床进展,由几个生物科技公司包括凯特制药,诺华,和其他公司强调了一个范例,工程性增强或新功能产生具有意向性设计功能的CTP。在这一领域开拓性的工作表明,T细胞可以被策划成表达定制设计的受体,用于靶向破坏对化疗耐药患者的复发性B细胞癌。从那时起,合成生物学技术已被用于产生大量的下一代CAR-T:协同刺激域增强了T细胞对癌细胞的信号转导;组合抗原识别可以产生更多的肿瘤选择性细胞;药物诱导开关切换控制CAR-T的活性和生长((June等,2015)。另一种CTP,间充质干细胞,其免疫调节特性正被广泛的研究,最近被设计成特定功能的增强,如归巢功能。
工程细胞功能的建立可以基于起始细胞类型的特性。由于红细胞可被设计表达特定的基因并在体内持续存在,并作为一种无核细胞类型,其安全性受目标基因整合的影响较小,所以红细胞正在作为有效的基质在细胞中构建新的功能。(Shi等人,2014年)。Rubius Therapeutics和Kanyos Bio已经发布了基于红细胞平台在代谢性疾病,自身免疫性疾病和肿瘤中的应用。enGene采取了同样独出心裁的方法治疗Ⅰ型糖尿病。通过工程肠道葡萄糖敏感的K-细胞分泌胰岛素,除了分泌正常的激素外,胰岛素可以在一种细胞类型中产生,而不是由这种自身免疫性疾病的潜在病理结果引起的(Cheung等,2000)。人们甚至会考虑在其他幼稚细胞中全面设计胰岛素传感器响应系统。
创造性地选择修饰的起始细胞类型可以简化或增强CTP独特功能的逆向工程。当使用CTP治疗疾病,重要的是保证移植细胞对抗原发病,尤其是当原发病的病因未知或可能是全身性时。例如,肌萎缩性侧索硬化症和额颞叶痴呆的特征是神经元和神经胶质细胞中形成不断扩大的重复RNA转录物,通过各种可能的机制导致神经退行性改变。因此下调SUPT4H1可能是有利的,这样可以控制这些重复序列的转录,在工程神经CTP治疗后防止移植细胞疾病的复发。(Kramer等,2016)。然而对于CTP功能增强的反应,长期的安全性和耐久性等还有待证实,丰富的工程策略使得用创新的方法来合成细胞疗法成为希望。
细胞工程应当实现简化所要评估的复杂特征并确保CTP的安全性和有效性(统称为“质量”)。目前正在使用多种分析技术来测量。细胞的特征、纯度和效力。然而,合成生物学工具为同时测量和控制多种细胞状态决定因素提供了可能性。 “分类器”系统已被描述的可能性,可以整合多种细胞因子来确定当前电池状态,按照预编程的行为测量。
“分类器”系统已被描述为能集成多个细胞因子的测量,以确定当前的细胞状态及随后的预编程行动。这些系统具有极大的潜力,简化了细胞质量参数指征的评估,因为多个可调的输入提供了当前状态的可靠评估,合成网络可以对适当、精确的输出作出响应。例如,荧光报告输出或快捷测量的蛋白质或代谢分泌物可以实时跟踪细胞状态(特性),凋亡开关可以消除不必要的细胞类型(纯度)(例如,Xie等人,2011),并且合成系统控制网络可以保证分化细胞的功能(潜能)(例如,Saxena等,2016)。这种策略在临床前CTP开发的早期应用已证明用miRNA表达鉴定和纯化PSC衍生的心肌细胞(Miki et al,2015)。分化细胞的质量也可以通过使用合成生物学方法来提高,这种方法绕过了基于细胞因子定向分化内在试剂活性的复杂性和变异性。例如,通过直接触发Ngn3,Pdx1、MafA以一个可控和可预见的方式,合成信号级联反应可以从祖细胞群生成功能分泌胰岛素的胰岛细胞(Saxena 等,2016)。
在设计合成网络之前,需要更好地理解支配某一命运的基因调控网络,包括这些网络的扰动来源。对先进的系统认识是支持质量源于设计(QbD)制造的基本概念;因此,基于合成生物学的质量评估工具的发展必然会提高CTP质量。细胞工程将补充QbD方法,通过产生与细胞质量相关的、可靠及时的关键参数的读数。快速存取细胞状态传感器将很好地描述的设计空间,量化不同系统参数对产品质量的影响,从而使CTP制造商能够适应变化的条件。基于2016年Lipsitz等描述的国际(药品注册)协调会议指南,在QbD框架内使用统计工具设计CTPS空间开发。无论合成细胞是如何发展的,其新的成分必须在患者几十年的生存期中,在体内保持稳定。一旦产品被生产出来,应有策略包含消除系统的元素,或者作为一种安全机制,一旦系统停止按计划运行的话就被消除掉。
虽然QbD方法可以指导工艺设计人员突破目前制造的挑战,但是CTP的稳定性,效率和成本(“
可制造性
”)然是一个关键的挑战(Lipsitz等人,2016)。细胞状态和基因表达工程工具可以用来创造更多的可制造性,因此高性价比的产品,应纳入QbD工具箱。
例如,可以实现各种基因和状态操作,以提高CTP的生产效率。提高可制造性的一个新兴战略是从患者特定型(自体)产品转向通用(异体)型产品,无需匹配,使他们顺应大规模制造所固有的经济效益。Cellectis公司利用TALEN技术创建一个“通用”的CAR-T,通过去除细胞的αβ T细胞受体,从而消除了移植物抗宿主反应,并结合公司的自杀开关和其他编辑元素。通用细胞采用类似的策略来设计HLA表达,以产生可以用于许多CTPs的通用供体细胞系(June等.,2015)。
类似于抗体生产的高产克隆选择,PSCs可以而且应该选择生存率与扩增稳定高的克隆。除了选择克隆外,细胞状态转换可以用来产生“高产”细胞。将PSC转成生长速度快,细胞间粘附力低的状态,或脱离昂贵的生长因子可能导致具有潜在的高制造性的细胞类型。这样的转换是生成一个发育较早的“幼稚”PSC状态,其中细胞具有优先的扩增特性:较高的单细胞克隆效率和更快的增长率及其它所需的性能(Hackett and Surani,2014)。我们可以通过转换技术控制关键基因来维持和退出不同的多能状态从而平衡高效细胞生长和有效定向分化的能力。
在许多分化计划中,PSC衍生细胞是唯一强大和可靠的细胞源。例如,心肌细胞在培养过程中不分裂,通常只能通过分步分化过程产生。最近,心脏祖细胞的状态外源性myc基因表达稳定,以创造一种人造细胞类型。可以被扩大培养并一步直接分化成功能性心肌细胞(Birket等,2015)。绕过漫长而昂贵的PSC状态分化策略可能证明
对其他细胞类型是有价值的,这取决于稳定性、牢固性与人造细胞状态和PSC状态靶向细胞的接近性之间的平衡。使用这些或其他人造细胞状态设计CTP可能会产生一种更有效的治疗方法,这是因为改进了悬置的可制造性问题。
在制造过程中增加的细胞工程步骤,增加了大量数据和信息,要求这些数据和信息呈报给国家监管机构(NRA)用于临床试验和市场授权。国家监管机构(NRA)的关键要求是要表明产品的整体风险是可以接受的(尽管在每个管辖区立法和监管的基础不同) 。例如,加拿大卫生部有权根据《食品和药品法和条例》决定细胞治疗的临床试验是否有可接受的风险收益状况,保证受试者最大利益并有可能达到试验的目标,然而责任在于发起人(即,CTP制造商)决定如何生产细胞。(见网站资源)在加拿大没有法律或法规禁止意欲大量生产与销售不安全有效的健康产品的措施。此外,在加拿大监管框架下仍有可能引入这样一个生产步骤,如果总体利益继续大于风险,它也可能减损安全性或有效性。像其他的国家监管机构NRAS一样,加拿大卫生部不倾向于拒绝细胞工程举措:整体风险效益状况授权保持老的可接受阈值。在CTP监管部门批准的其他方面,证据必须表明,细胞工程保持或转换风险效益至同位评估。此外,注册申报受
得到每个清晰合理的生产措施的最好支持。特别是当细胞被设计为简化评估或提高质量时,由此产生的工程化的CTPS将被设计为较之起源细胞质量更安全的细胞。因此,整体风险效益平衡将被转移到有利于细胞工程的过程中。例如,基本的凋亡开关都被纳入CTPS走向临床,开发更先进的凋亡开关(Xie等,2011),从而直接降低治疗风险。在这些系统中,小分子的存在诱导了工程化半胱天冬酶蛋白的激活,从而触发了移植细胞的凋亡。















