
鼻咽癌是中国南方和东南亚地区常见的恶性肿瘤。每年全世界约有86000人发病和50000人死于此病,其种族和地理分布差异很大。在高水平证据的基础上,放射治疗或放化疗已成为早期或局部晚期鼻咽癌患者的主要治疗方法,5年生存率约85%。然而,肿瘤扩散仍然是这些患者治疗失败的主要原因。而且大约15%的鼻咽癌患者在初次诊断时发生了远处转移。复发性或原发转移性鼻咽癌患者的预后非常差,中位总生存期大约20个月。
鼻咽癌具有高度的化疗敏感性。含铂双联化疗通常被认为是复发性或转移性鼻咽癌患者的标准治疗方法,但是从来没有直接与支持治疗相比。到目前为止,尚无随机试验确定最佳治疗方案。接受不同治疗方案的患者之间是否存在生存差异仍然未知。目前,顺铂联合连续静脉滴注氟尿嘧啶广泛应用于复发性或转移性鼻咽癌患者,其反应率为40%-65%。然而,短期反应,常见的粘膜并发症和深静脉导管插入术的要求仍然是氟尿嘧啶联合顺铂方案的主要限制。因此,发现新的具有可接受毒性的联合化疗方案以延长复发性或转移性鼻咽癌患者的生存期非常重要。由张力教授主导的一项大型随机试验对此给出了答案,这项研究于2016年8月在线发表于柳叶刀杂志1。下面是本研究的具体内容。
吉西他滨是具有广谱抗肿瘤活性的嘧啶类似物和核糖核苷酸还原酶抑制剂。体外观察到的吉西他滨和顺铂之间的协同细胞毒效应使其成为肿瘤治疗中有希望的治疗方案。几项2期试验【2-4】表明吉西他滨在鼻咽癌患者中具有令人满意的疗效和可耐受的毒性。然而,这些研究中招募的患者数量太少,无法得出明确的结论。因此,我们进行了这种头对头,随机,3期试验,以比较吉西他滨联合顺铂与氟尿嘧啶联合顺铂在一线治疗复发性或转移性鼻咽癌患者中的疗效和安全性。
这是一项多中心,随机,开放标签的3期临床试验,在我国22家医院进行。参与中心的研究者们招募了患有组织学或细胞学证实的鼻咽癌患者。根据WHO的肿瘤分类对鼻咽癌的组织学亚型进行分类:I型是角化鳞状细胞癌,II型是分化的非角化癌,III型是未分化的非角化癌。
其他入选标准是患者在治愈性放疗后具有转移性疾病,或在治愈性放疗后局部复发,不适合局部治疗的患者;先前尚未接受任何系统性化疗的复发性或转移性患者;ECOG PS评分为0或1的患者;年龄在18岁或以上;具有完善的器官功能(白细胞计数为4.0×109 / L或更高);预期寿命估计为12周或更长; 已提供书面知情同意并适于定期随访。
把362名符合条件的患者按1:1的比例随机分配到吉西他滨联合顺铂(吉西他滨)组和氟尿嘧啶联合顺铂(氟尿嘧啶)组。
分配到吉西他滨组的患者在第1天和第8天以1 g/m2接受吉西他滨静脉滴注超过30分钟,并且在第1天以80 mg/m2接受顺铂治疗4小时。分配到氟尿嘧啶组的患者以4 g/m2通过持续静脉滴注氟尿嘧啶超过96小时,并且在第1天以80 mg/m2静脉滴注顺铂4小时。两组中的患者每3周均接受一次分配治疗,最多6个周期,或直到疾病进展,死亡,不可耐受的毒性发生或患者要求停止。 在研究方案规定的疾病进展之前不允许使用任何其它抗癌药物。
如果患者患有进展性疾病,发生研究方案中指定的不可接受的副作用,或者开始另一抗肿瘤治疗,或者其指定的治疗延迟超过2周,研究者将把这些患者从研究中移除。对于需要两次以上剂量调整的患者,则永久停止治疗。
本实验将无进展生存期做为主要研究终点(从患者随机化入组到出现疾病进展或者任何原因导致的死亡这段时间定义为无进展生存期)。次要研究终点包括客观反应率,疾病控制比例,以及总生存期(从患者随机化入组到出现死亡的时间定义为总生存期)。对接受至少一个周期研究药物的患者进行安全性分析。为了探索基线特征和治疗效应之间的联系,研究者还进行了亚组分析。
这项研究的主要目的是为了证明吉西他滨联合顺铂与氟尿嘧啶联合顺铂相比在无进展生存期方面更具有优势。患者招募期为2年,随访期为1年。
2012年2月20日至2015年10月30日,362名符合条件的患者在中国22个地点被随机分配接受吉西他滨联合顺铂(n=181)或氟尿嘧啶联合顺铂(n=181)治疗。
362名患者中,有353名(98%)接受指定研究药物的治疗。 分配到吉西他滨组的1个患者由肿瘤学家错误地给予氟尿嘧啶联合顺铂治疗,另有3个分配到氟尿嘧啶组的患者选择接受吉西他滨联合顺铂治疗方案。吉西他滨组的3名患者和氟尿嘧啶组的6名患者在分配治疗前撤销同意。
治疗组之间的人口基线特征和疾病特征是平衡的。患者中位年龄为47岁,大多数为非吸烟患者,ECOG PS为1,组织学类型为WHO III型。超过三分之二的患者出现复发性疾病,大多数患者接受了诱导和同步化疗。
无进展生存期数据分析的截止日期是2016年4月10日,总共分析329例患者(吉西他滨组156名,氟尿嘧啶组173名)。无进展生存的中位随访时间为19.4个月(IQR 12.1-35.6)。吉西他滨组(中位生存期7.0个月,IQR 4.4-10.9; 95%CI 6.3-7.6)的中位生存时间明显长于氟尿嘧啶组(中位生存期5.6个月,IQR 3.0–7.0; 95% CI 4.9–6.2), HR为0.55 (95%CI0.44-0.68; p < 0.0001)。Kaplan-Meier评估吉西他滨组患者的无进展生存期均高于氟尿嘧啶组,分别为6个月(66% vs 45%),12个月(20% vs 6%),18个月(11%vs 2%),如下图。
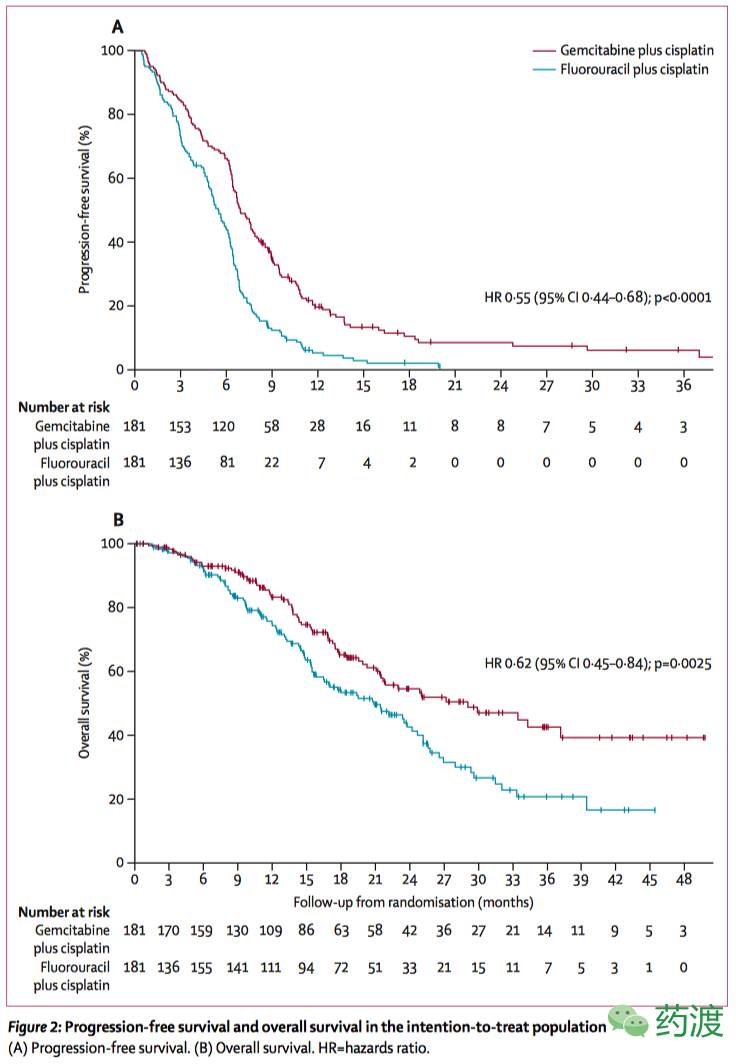
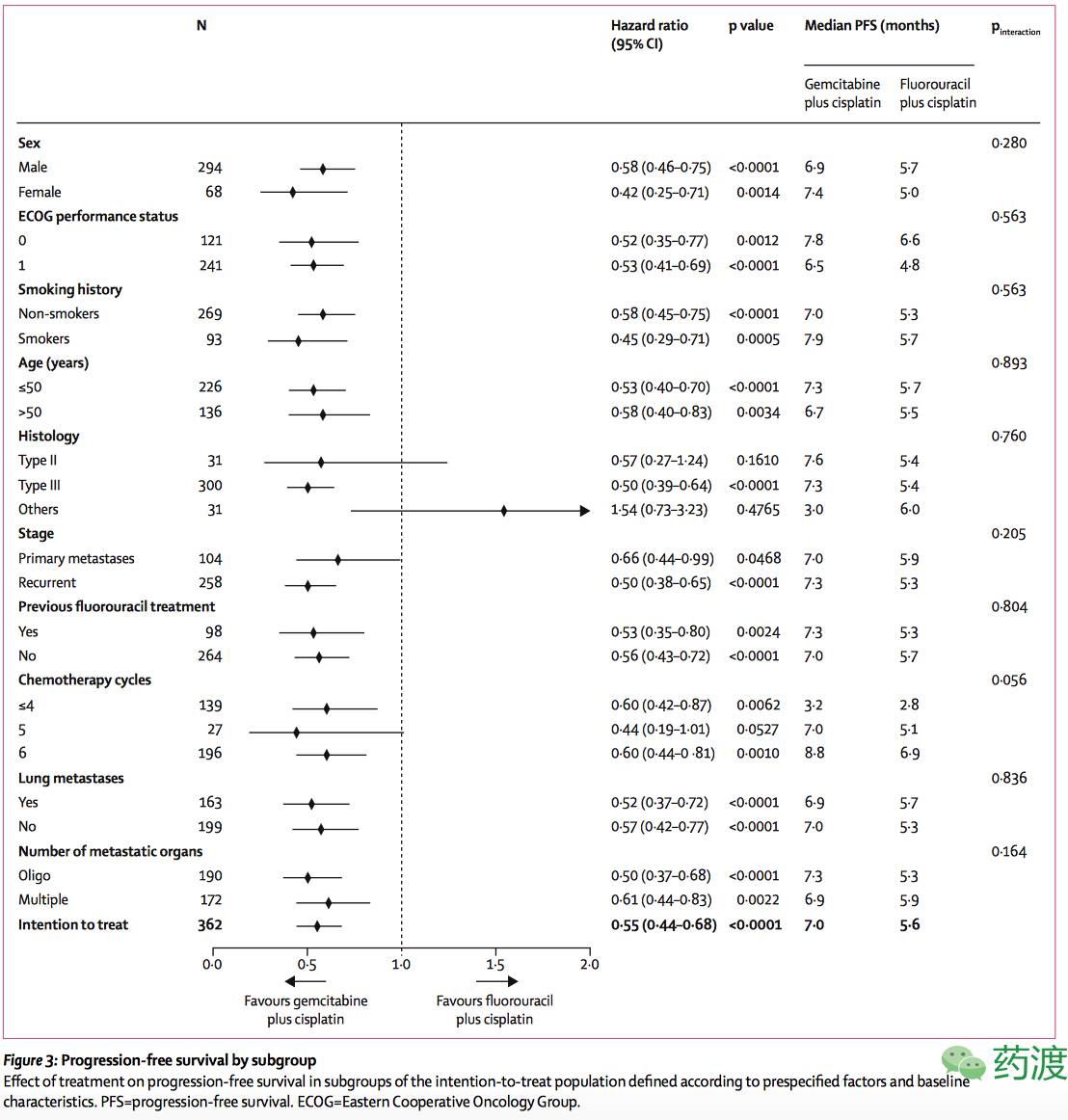
无进展生存期的改善在所有预先指定的亚组中是一致的,除了非III型和具有五个周期化疗的亚组患者。总体生存的中位随访时间为22.0个月(IQR 13.0-33.5)。 在随访期间,吉西他滨组的66名患者和氟尿嘧啶组的95名患者死亡。 吉西他滨加顺铂组的中位总生存期为29.1个月(IQR 12.0-31.5; 95%CI 18.7-39.5), 氟尿嘧啶加顺铂组的中位生存期为20.9个月(IQR 14.6-未达到;95%CI 16.0-25.8,HR 0.62 [95%CI 0.45-0.84];p = 0·0025)。在吉西他滨组中,15名患者达到完全缓解,101名患者部分缓解,46名患有疾病稳定,3名患有进行性疾病,16名患者无法评价。在氟尿嘧啶组,5名患者达到完全缓解,71名患者部分缓解,80名患者疾病稳定,12名患者有进行性疾病,13名患者无法评估。在吉西他滨组,达到客观反应的患者的比例显著高于氟尿嘧啶组(116[64%] vs 76 [42%]);相对危险度为1.5 [95%CI 1.2-1.9 ];p <0.0001)。 两组的疾病控制率相似(162 [90%] vs 156 [86%])。
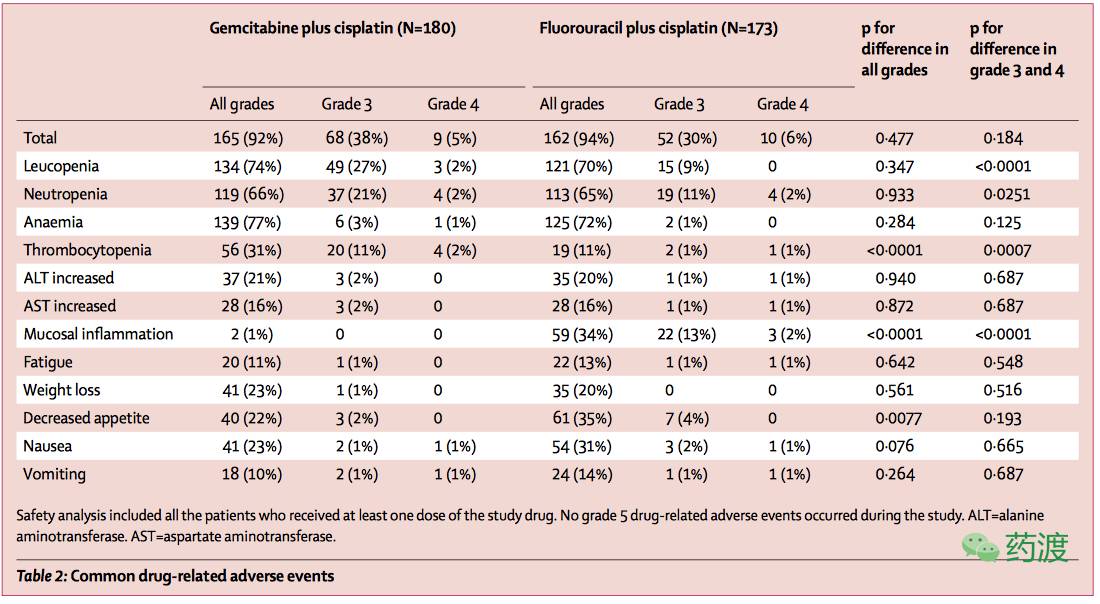
吉西他滨组的180名患者和氟尿嘧啶组的173名患者均进行了安全性分析。包括血液学和非血液学毒性在内的治疗相关的不良反应在吉西他滨组和氟尿嘧啶组之间是相似的。但是对于观察到的3级或更高级不良反应,如白细胞减少,中性粒细胞减少,血小板减少症和粘膜炎症在两组之间则有显著性差异。吉西他滨组的45名(25%)患者和氟尿嘧啶组的18名(10%)患者在3级或更高级别的血液学不良事件中接受粒细胞集落刺激因子治疗。接受吉西他滨联合顺铂的180名患者中有10名(6%)报道了严重不良事件,接受氟尿嘧啶联合顺铂的173名患者中有15名(9%)报道了严重不良事件。吉西他滨组中有7名患者发生严重不良反应,氟尿嘧啶组中有10名患者发生严重不良反应。吉西他滨组中由于药物相关不良反应导致的停药率为3%(6/180名),氟尿嘧啶组为8%(14 /173名)。吉西他滨组中有18名(10%)患者发生剂量减少,氟尿嘧啶组中有20名(12%)患者发生剂量减少。两组中均没有与药物相关的致命不良事件发生。
复发性或转移性鼻咽癌对化疗高度敏感,但反应持续时间短,总生存期较差。由于3期临床试验缺乏,复发或转移性鼻咽癌的一线治疗尚未建立。 在这一随机3期,头对头试验中,达到主要研究终点。与传统的氟尿嘧啶联合顺铂方案相比,吉西他滨联合顺铂显著延长无进展生存期,同时在反应率和总生存期方面也有显著改善。总体而言,两种治疗方案都具有良好的可耐受性,具有可预测的毒性特征和低停药率。
吉西他滨是具有广谱抗癌活性的核苷类似物。一些小规模研究【5-7】显示吉西他滨无论是单独使用还是与其他药物联用,对鼻咽癌患者均有效,并且具有可耐受的毒性。两项2期试验6,8报道了吉西他滨单药用于未经治疗或预处理过的复发或转移性鼻咽癌患者的结果。在这些试验中,客观缓解率范围为28%-48%,中位无进展生存期为3.6-5.1个月,中位总生存期为7.2-16.0个月。两项研究调查了吉西他滨加长春瑞滨对铂类耐药晚期鼻咽癌患者的疗效。Chen和同事9报告的反应率为37.7%,中位无进展生存期为5.2个月,中位总生存期为14.1个月。而Wang和同事10报告的反应率为36%,中位无进展生存期为5.6个月,中位总生存期为11.9个月。
2期试验研究了吉西他滨加S-1(替加氟,吉美嘧啶和氧嗪酸)作为铂治疗失败的鼻咽癌患者补救疗法的疗效,报告的反应率为43%,中位无进展生存期为5.8个月,中位总生存期为14.8个月。考虑到吉西他滨和顺铂在体外的协同作用,吉西他滨和顺铂或奥沙利铂的组合也已经在用于复发性或转移性鼻咽癌的三项小规模2期试验中进行了研究。然而,到目前为止,还没有随机试验将含有吉西他滨的治疗方案与另一种药物进行头对头比较研究。这些数据提供了探索吉西他滨联合顺铂在一线治疗复发转移性鼻咽癌患者在随机试验设计中的疗效的理由。
在该试验中,我们发现吉西他滨组中无进展生存期显著改善,与氟尿嘧啶组相比,疾病进展(或死亡)的风险降低45%。吉西他滨联合顺铂组的中位无进展生存期为7.0个月,而氟尿嘧啶联合顺铂组为5.6个月。目前,含氟尿嘧啶的治疗方案被广泛应用于一些局部晚期鼻咽癌患者的诱导化疗和辅助化疗中。在这项研究中,超过三分之二的患者在放疗后复发,约三分之一的患者以前接受过氟尿嘧啶治疗。然而,在亚组分析中,对于不同治疗背景的患者(原发转移或放化疗后复发;先前接受过或未接受过氟尿嘧啶治疗),吉西他滨联合顺铂与氟尿嘧啶联合顺铂相比,在无进展生存期方面均表现出一致的优势。吉西他滨联合顺铂与氟尿嘧啶联合顺铂相比,在客观反应率方面有22%的提高。这些结果意味着吉西他滨具有比氟尿嘧啶更有效和持久的抗癌活性。据我们所知,这是针对转移或复发性鼻咽癌患者的第一次大规模随机试验。结果可为这一人群的一线治疗提供有力证据。
初步数据表明,与氟尿嘧啶加顺铂相比,吉西他滨加顺铂也可能提高复发或转移性鼻咽癌患者的总生存期。吉西他滨联合顺铂和氟尿嘧啶联合顺铂的不良事件概况与预期一致。与吉西他滨联合顺铂相比,白细胞减少,中性粒细胞减少和血小板减少的药物相关不良事件更频繁,并且粘膜炎与氟尿嘧啶联合顺铂治疗方案相关。由于不良反应的发生,氟尿嘧啶组与吉西他滨组相比,有更高比例的患者停止了该研究试验。由于病发部位的特殊性,鼻咽癌患者放疗后口腔健康状况一般较差。此外,氟尿嘧啶联合顺铂方案可以加重这些患者的粘膜炎症。氟尿嘧啶输注所需的深静脉导管插入也增加了导管相关感染和血栓栓塞的风险。所有这些因素都限制了氟尿嘧啶的应用。然而,对于吉西他滨联合顺铂治疗方案,最常见的血液学毒性可以更容易地鉴定,预防和治疗。此外,吉西他滨联合顺铂方案的施用相对更简单,化疗计划可以作为门诊治疗,从而降低患者的住院费用和压力。
这篇文章中报道的数据有一定的局限性。首先,这项研究是在鼻咽癌高发地区完成的,这个地区鼻咽癌主要的组织学特征是未分化的、非角化癌。该结果是否可应用于鼻咽癌发病率相对较低的欧洲和北美等西方国家仍有待阐明。第二,在本分析时,总生存期的终点不够成熟,不能进行全面评估。然而,关于总生存期的初步结果还是令人鼓舞的。第三,研究者们没有调查EBV DNA在吉西他滨联合顺铂和氟尿嘧啶联合顺铂方案中的预测作用。众所周知,EBV感染是流行地区鼻咽癌发病机制的重要病因学因素。血浆EBV DNA可用于早期疾病的检测,预后预测,以及治疗反应和复发的监测。然而,当试验开始时,并非所有的研究中心都进行EBV DNA检测。因此,在这项研究中,EBV DNA水平检测不是必须的。最后,开放标签试验设计可能会对某些终点引入偏差。
总之,本文报道的数据总体显示了吉西他滨联合顺铂方案能够改善疗效并且具有可预测的耐受性。研究者认为,这些数据在临床实践变化和在选择一线治疗复发性或转移性鼻咽癌的治疗方案时具有重要的参考作用。
本文链接:https://www.ncbi.nlm.nih.gov/pubmed/27567279
参考文献:
1. Li Zhang,Yan Huang,Shaodong Hong,et al. Gemcitabine plus cisplatin versus fluorouracil plus cisplatin in recurrent or metastatic nasopharyngeal carcinoma: a multicentre,randomised,open-label,phase 3 trial. Lancet 2016; 388: 1883–92.
2. Ma BB,Tannock IF,Pond GR,Edmonds MR,Siu LL. Chemotherapy with gemcitabine-containing regimens forlocally recurrent or metastatic nasopharyngeal carcinoma. Cancer 2002; 95:2516–23.
3.Wang J,Li J,Hong X,et al. Retrospective case series of gemcitabine plus cisplatin in the treatment of recurrent and metastatic nasopharyngeal carcinoma. Oral Oncol 2008; 44: 464–70.
4. Ngan RK,Yiu HH,Lau WH,etal. Combination gemcitabine and cisplatin chemotherapy for metastatic or recurrent nasopharyngeal carcinoma: report of a phase II study. Ann Oncol 2002;13: 1252–58.
5. Hsieh JC,Hsu CL,Ng SH,et al. Gemcitabine plus cisplatin for patients with recurrent or metastatic nasopharyngeal carcinoma in Taiwan: a multicenter prospective phase II trial. Jpn J Clin Oncol2015; 45: 819–27.
6. Foo KF,Tan EH,Leong SS,et al.Gemcitabine in metastatic nasopharyngeal carcinoma of the undifferentiated type. Ann Oncol 2002; 13: 150–56.
7. Jiang Y,WeiYQ,Luo F,et al. Gemcitabineand cisplatin in advanced nasopharyngeal carcinoma: a pilot study. CancerInvest 2005; 23: 123–28.
8. Zhang L,Zhang Y,Huang PY,et al. PhaseII clinical study of gemcitabine in the treatment of patients with advanced nasopharyngeal carcinoma after the failure of platinum-based chemotherapy.Cancer Chemother Pharmacol 2008; 61: 33–38.
9. Chen C,WangFH,Wang ZQ,et al. Salvage gemcitabine- vinorelbine chemotherapy in patients with metastatic nasopharyngeal carcinoma pretreated with platinum-based chemotherapy. Oral Oncol 2012; 48: 1146–51.
10. Wang CC,Chang JY,Liu TW,Lin CY,Yu YC,Hong RL. Phase II study of gemcitabine plus vinorelbine in the treatment of cisplatin-resistant nasopharyngeal carcinoma. Head Neck 2006; 28: 74–80.
声明:
本文由药渡头条投稿作者撰写,观点仅代表作者本人,不代表药渡头条立场,欢迎交流补充。联系方式:010-82826195 转8048
如需转载,请务必注明文章作者和来源
投稿详情请点击“3月-4月 | 王牌写手获奖名单”



















