今年年初全球流感爆发,日本
Shionogi的新型抗流感病毒药物Xofluza(Baloxavir marboxil)仅四个月就获批上市,小编借此梳理一下抗流感病毒的药物及其进展。
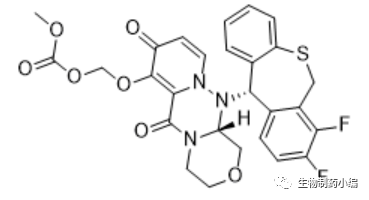
背景介绍
流感病毒由脂双分子层和蛋白质外壳(envelop)和反义RNA组成。外壳蛋白主要包括凝血素HA和神经氨酸酶NA,这两种蛋白又各自有不同的亚型,可用来区分流感病毒种类,如H1N7,H1N5等。反义RNA携带11种基因:血凝素(hemagglutinnin, HA)、 (neuraminidase,NA)、(matrix 1,M1)、(matrix2,M2)、(nucleoprotein,NP)、非结构蛋白1 (non-structural protein 1, NSP1)、 非结构蛋白2(non-structural protein 2, NSP2 或者出核蛋白NEP) 、聚合酶蛋白(PA)、基础聚1(polymerase basic protein1, PB1)、基础聚合酶2(polymerase basic protein 2,PB2)。
病毒复制过程:
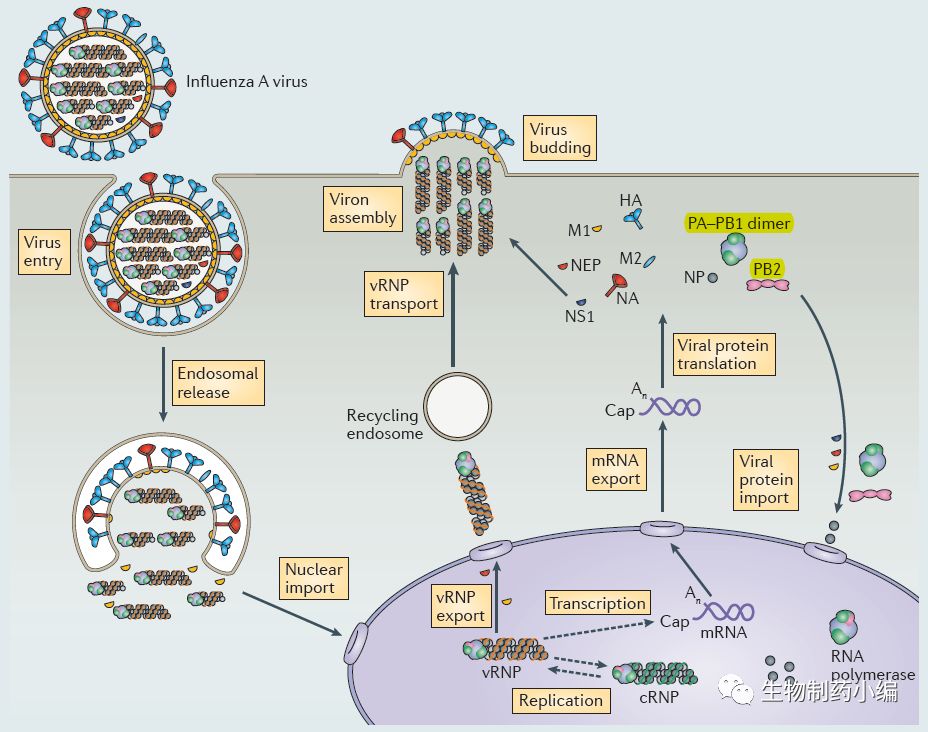
病毒与宿主细胞膜表面受体结合,被吞入endosome进入宿主细胞,由于endosome的PH值较低(5-6)导致病毒HA0蛋白结构发生改变,导致HA2 fusion肽段暴露嵌入endosome膜,并打开M2离子通道,讲病毒的vRNP释放进入细胞质。vRNP包含NP,PA,PB1,PB2蛋白和反义RNA,这些蛋白中都有细胞核定位信号(NLS)。vRNP进入细胞核之后首先需要将反义RNA转换成正义RNA,形成cRNP,再以此作为模板进行复制形成vRNP。同时vRNP的另一个重要任务是转录生成mRNA,病毒自带的RNA-依赖型RNA聚合酶(RdRp)用自带的RNA作为引物,RdRp由PA,PB1和PB2结构组成。但用于翻译的病毒mRNA没有5’帽子,这时RdRp中PB1与宿主细胞mRNA的5‘端的甲基化帽子结合,由具有核酸内切酶功能的PA进行剪切。病毒进一步抢占宿主细胞的剪切机器对自己的基因进行剪切拼接,从而产生M2,NEP。携带反义RNA的vRNP通过CRM1依赖的通路出细胞核。病毒颗粒的囊泡来自由极性细胞的表层(如上皮细胞分为apical side和basal layer side),主要蛋白有HA,NA和M2。病毒的HA与宿主细胞膜表面的唾液酸相连接,神经氨酸酶以唾液酸为作用底物催化唾液酸水解,释放病毒。又开始下一轮侵染。
已成药的经典靶点
早期的抗流感药物主要集中在三个靶点,分别对应病毒侵染到离开宿主细胞过程中的三个重要步骤。
-
M2离子通道抑制剂,阻止病毒从endosome进入细胞质:金刚烷胺amatadine,甲基金刚烷胺Rimantadine。
-
聚合酶抑制剂,阻止病毒复制:法匹拉韦 favipira。
-
神经氨酸酶NA抑制剂,阻止病毒离开细胞:奥司他韦oseltamivir,扎那米韦zanamivir, laninamivir,帕那米韦paramivir。
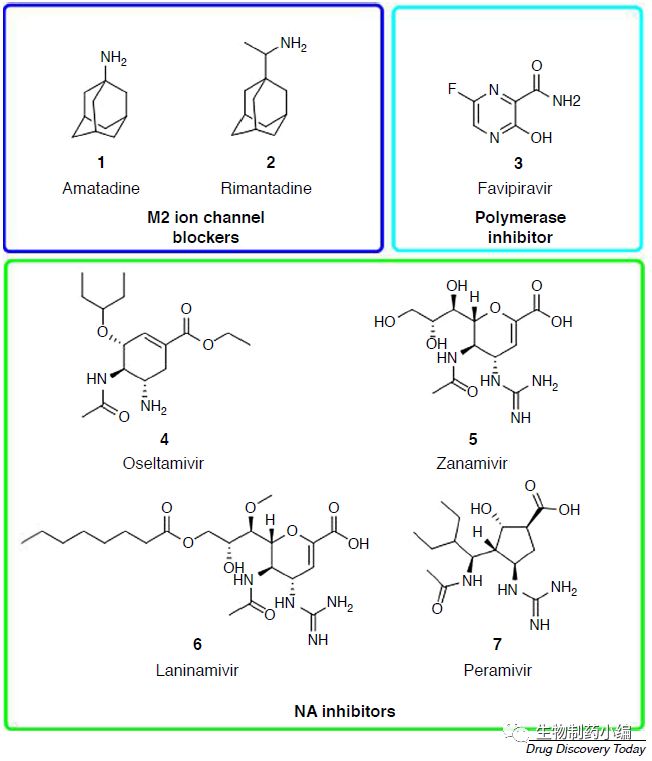
中国市场主要是被金刚烷胺、甲基金刚烷胺及奥司他韦占据。由于M2蛋白转膜区的突变(涉及26、27、30、31和34位),使阻断剂金刚烷胺和甲基金刚烷胺在体内外均可迅速产生耐药。奥司他韦相对高效低毒,正在慢慢取代金刚烷胺市场。预计2017年东阳光药(港股HK1558)的奥司他韦(可威)销售额有13-14亿人民币,2018年初爆发的流感使其今年Q1销售额可能已经达到2017年下半年的水平。但病毒也会对奥司他韦产生耐药性,由Biota Pharmaceuticals和Daiichi Sankyo公司研发的Laninamivir就是用于治疗对奥司他韦具有抗药性的流感病毒感染,目前还没有在中国上市。
新的热门研发位点:RdRp(PA-PB1-PB2)

PdRp目前是抗流感病毒药物研发中相对较新的一个点,分为两个策略。一是就这三个蛋白结构(PA,PB1,PB2)的不同功能来划分,如阻断PB2与宿主细胞的mRNA结合位点,阻断vRNA的结合位点,抑制PA的核酸内切酶活性位点等。二是基于PdRp需要三个蛋白结构相互连接配合才能完成复制、转录及复制-转录两个过程的切换,抑制PA、PB1、PB2之间的interface也是一个很好的策略。
除了
Xofluza之外,
由Vertex研发的VX787在2013年就进入二期临床试验,机制是通过吲哚基团与第323位的苯丙氨酸形成 π-stacks(两个苯环平行堆叠),占据PB2帽子结合位点从而阻止病毒mRNA的转录。2014年转手给Janssen,小编暂时没有查到音讯。
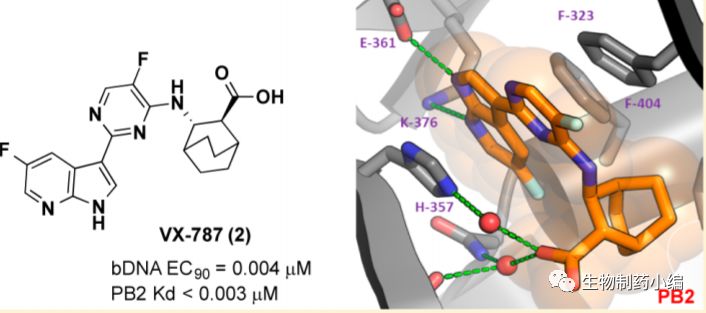
参考文献
-
Aartjan J.W.te Velthuis and Ervin Fodor. Influenza virus RNA polymerase: insights into the mechanisms of viral RNA systhesis. 2016. Nature review.
-
Zhongxia Zhou, Tao Liu, Jian Zhang, Peng Zhan and Xinyong Liu. Influenza A rirus polymerase: and attractive target for next-generation anti-influenza therapeutics. 2018. Drug discov Tody.
-
Michael P. Clark., etc. Discovery of a Novel, First in Class, Orally Bioavailable Azaindole inhibitor (VX-787)of influenza PB2. 2014. JACS.
附:分别以PA,PB1,PB2为靶点的抑制剂
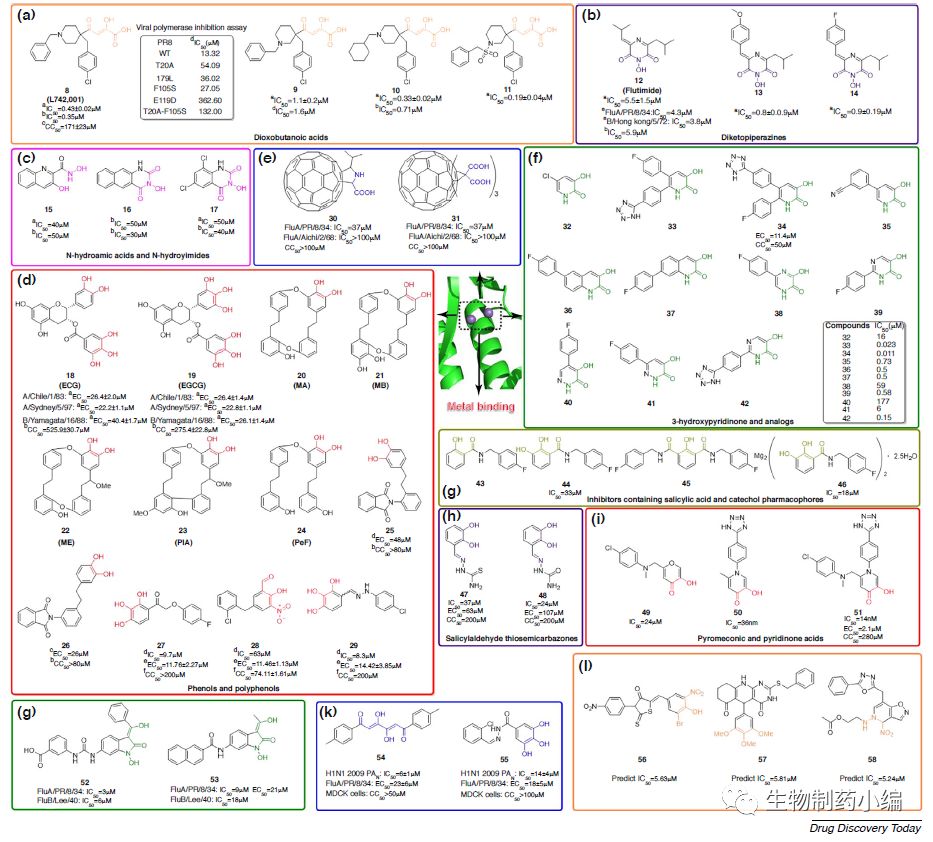
PA抑制剂
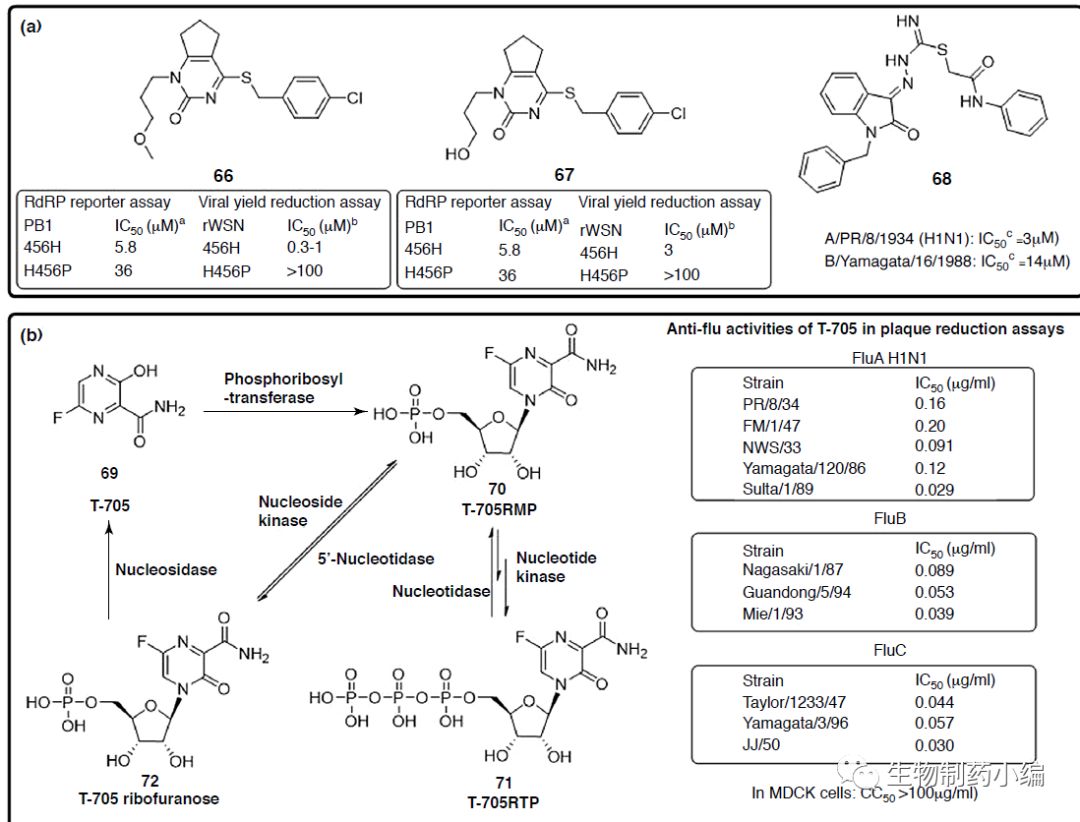
PB1抑制剂
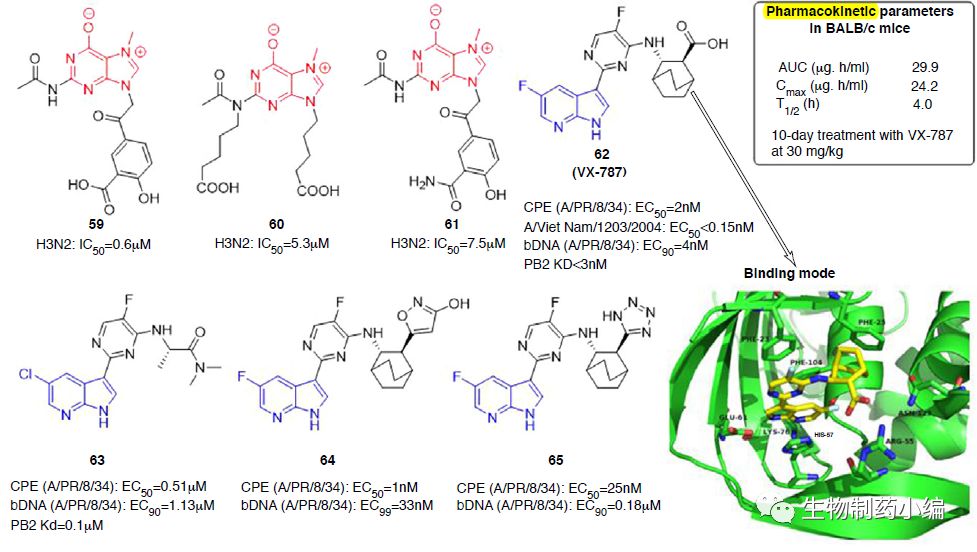
PB2抑制剂
欢迎加入小编团队成为小编一员
请加 小编微信号:wuwenjun7237
如有技术解读、行业洞见愿意分享
欢迎投稿到小编邮箱:
[email protected]

版权为生物制药小编所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:生物制药小编”。













