申请成为专栏作者,或原创投稿
请联系:[email protected]
本文由HEROIV根据公开信息整理,如有疑问,欢迎留言交流。
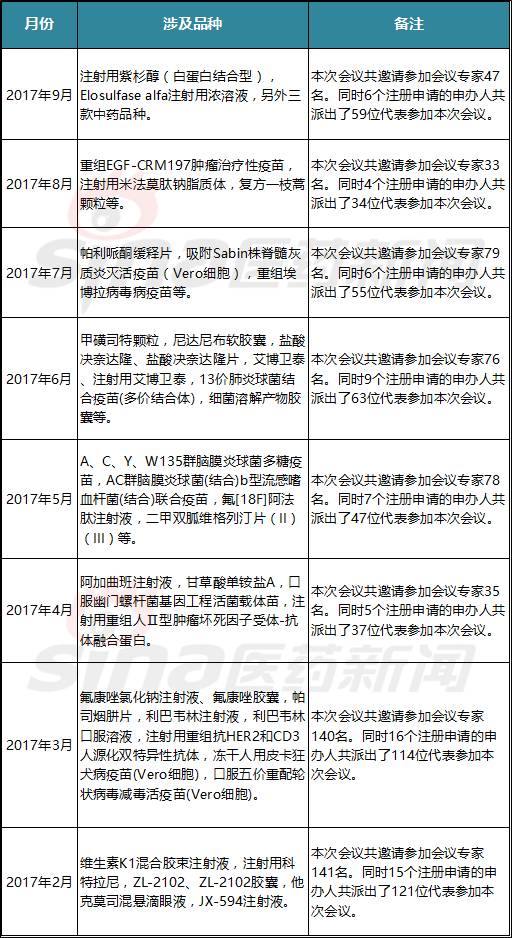
今年2-9月,CDE每月召开了药审咨询会。
品种盘点:
本品来自于兆科药业(合肥)有限公司申报的一类生物制品,抗肿瘤药物,今年7月获批临床,为特殊审评品种。兆科代理SillaJen,Inc. 公司申报,拟在中国开展国际多中心III期临床试验,验证其与索拉菲尼序贯治疗用于未接受过系统疗法治疗的晚期肝细胞癌患者的有效性和安全性。JX-594注射液是一种经过基因改造修饰的溶瘤重组牛痘病毒,尚未在国内外上市,对于其由于基因重组和牛痘疫苗本身带来的风险尚不明确。
ZL-2102胶囊为PGD2合成酶抑制剂,慢性呼吸性疾病(哮喘和COPD),2017年4月批准临床,国内由再鼎医药申报。该品种从赛诺菲获得授权。
注射用科特拉尼在中国进行新药注册的药品注册分类为原化学药品1.1类, 获批的临床适应症为皮肤伤口祛瘢痕愈合及增生性瘢痕治疗。注射用科特拉尼的作用机理清晰,主要针对炎症反应和瘢痕生成过程的抗瘢痕生成治疗靶点,通过抑制TGF-β1和COX-2两个因子的表达,具有独特的治疗优势。2017年4月,香雪制药与苏州圣诺生物医药合作研发的产品注射用科特拉尼获得了CFDA核准签发的《药物临床试验批件》。本品为核酸干扰药物。
本品由武汉友芝友生物制药有限公司申报,针对肿瘤的新一代治疗性双靶向抗体药物。除本品之外,友芝友pipepline中还包括靶向EpCAM/CD3、CD20/CD3、EGFR/CD3等双特异抗体。本品为特殊审批品种,2017年9月30日显示的状态为制证完毕-待发批件(IND)。截止发稿,该产品已批准临床。
本品由百傲万里(上海)生物医药(Biomarin)国内申报IND。一款罕见病用药,首只被FDA批准的治疗粘多糖沉积症IVA型的药物。粘多糖病Ⅳ型(Morquio氏病)有两个亚型。其病因为ⅣA为半乳糖-6-硫酸酯酶(GALNS)缺乏,ⅣB为β-D半乳糖酶缺乏。该病为常染色体隐性遗传,其临床特点为明显的生长迟缓,步态异常和骨骼畸形且逐渐显着,病人寿命多为20~30岁。本品为优先审评品种,目前仍处于临床试验申请阶段。
本品为治疗用生物制品1类,2015年7月申报,目前处于在审评审批中。来自于上海惠盾生物技术有限公司申报。相关专利:白喉毒素突变体CRM197的制备方法,CN104140972A,公开了高效表达白喉毒素突变体CRM197的表达载体、工程菌及制备方法等。本发明构建的重组白喉毒素突变体CRM197表达工程菌具有表达量高,表达稳定等优点,所采取的纯化工艺稳定可靠,得率高,利于大规模生产。
本品来自于武田制药。此前纳入优先审评程序药品注册申请第十批,申请事项:新药临床试验,入选理由:儿童用药;临床急需(2016.9.14)。本品用于治疗骨肉瘤。
9月底,Boehringer Ingelheim 重磅新药乙磺酸尼达尼布软胶囊(Nintedanib)的上市申请(JXHS1700020,JXHS1700021)获得CFDA批准,用于治疗特发性肺纤维化(IPF),商品名-维加特。2016年国外Ofev的销售额翻倍达到6.13亿欧元,2017年上半年达到4.29亿欧元。尼达尼布是勃林格殷格翰2017年继阿法替尼、恩格列净之后在中国上市的第3款新药。
撰文:HEROIV
编辑:Holly
*声明:本文由入驻新浪医药新闻作者撰写,观点仅代表作者本人,不代表新浪医药新闻立场。
▷ 华润双鹤:转型升级,引领民族制药企业品质提升
▷ 人福医药吡格列酮片的ANDA获美FDA审评批准
▷ 孤儿药从认定到批准,这个距离到底有多长?















