诺华CAR-T获得FDA批准上市,世界为之欢呼雀跃,一时之间溢美之词不绝于耳,人们为其冠以“划时代”、“历史性”之名,诚然,CAR-T确实凝结了众多辛勤劳作,只是局限依然巨大。
在关注度上能够与CAR-T平分秋色的应该是PD-1/L1免疫抑制剂,二者同样是基于人体免疫细胞,通过强化或防止正常免疫功能受限而达到治疗目的。但当我们还沉浸于响应率、治愈率时,我们的敌人却不断在升级自己,肿瘤细胞已经在它的微环境中伫立了厚厚的围墙,策划着它的阴谋,而人类目前几乎束手无策。
不久前,《Science》杂志上报道了科学家针对癌症的最新研究成果,魏兹曼研究所的Ravid Straussman教授及其领导的团队发现,胰腺癌组织内存在某种可以在肿瘤微环境中生存的微生物,该微生物可以“消化”化疗药物吉西他滨,在这种情况下,即便使用10倍剂量的吉西他滨,肿瘤细胞也会安然无恙。
肿瘤细胞与微生物实现共生,共同构建了这样的肿瘤微环境,二者相互提供保护或生存环境。微生物通常以二分裂形式繁殖,平均每20-30分钟完成一次分裂,微生物可以以惊人的速度繁殖,例如在资源充足、环境允许的情况下大肠杆菌繁殖48小时后的总重量可达到4000个地球的质量,这样快速的繁殖带来的是极强的变异能力,以及极强的环境适应能力。与人类平均花费许多年(7-15年不等)才能上市一款新药相比,微生物快速的实现自身种群的迭代,用生命为代价实现后代的生存,一代代前仆后继,只为遗传信息的延续。
而人类在又如何能逃过这样的处心积虑?
发现过程:吉西他滨在上市之后提高了患者生存率,但是经过长期临床应用之后出现了耐药性,使得吉西他滨的临床应用价值越来越低,作者便试图阐释这种耐药性的产生原因及机理。
研究者将人类皮肤纤维细胞(经皮肤复位手术)与大肠癌和胰腺癌肿瘤细胞系共同培养后,发现此时的肿瘤细胞表达了极强的耐药性。
在花费多年时间却一无所获之后,偶然间,研究者使用0.45um过滤器过滤该培养液后发现肿瘤细胞的耐药性竟然消失了,而0.45um过滤器可以过滤大部分微生物,结合以上两点,研究者推测培养液中可能含有某种微生物,并且这种微生物就是肿瘤细胞耐药性的罪魁祸首。
研究者也确实在培养液分离出一种支原体(猪鼻支原体;Mycoplasma hyorhinis),它是类似细菌但不具有细胞壁的原核微生物,于是研究者认为支原体就是肿瘤耐药性的主要来源。为了验证这种推测,研究者在原始培养液中加入抗生素,在消灭了微生物的同时肿瘤抗药性也消失了。
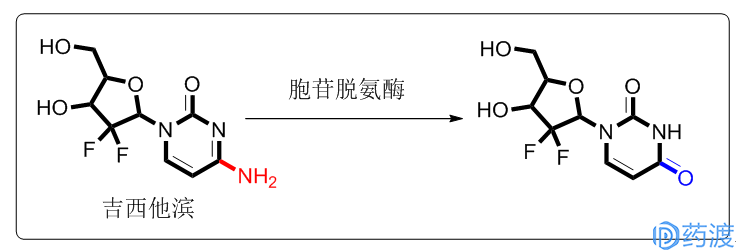
但是,研究到这一水平并不能透彻的阐述耐药性产生的具体原因,因为不同肿瘤微环境中可能包含微生物种类必然不同,因此从基因水平考察这些微生物的共性是一种行之有效的研究方向,研究者通过对比之后,发现这些微生物都含有特定的基因组可以表达出酶胞苷脱氨酶(enzyme cytidine deaminase),在该酶的作用下,吉西他滨直接发生脱氨基作用,进而失去药效。
微生物可以帮助肿瘤产生耐药性还是首次报道,然而人们对肿瘤微环境的研究却从未停歇过,之前许多研究者曾报道过肿瘤微环境中包含的非恶性细胞可以帮助肿瘤实现耐药性,此次的研究成果无疑为我们认识肿瘤微环境提供了良好的视角和全新的思路。
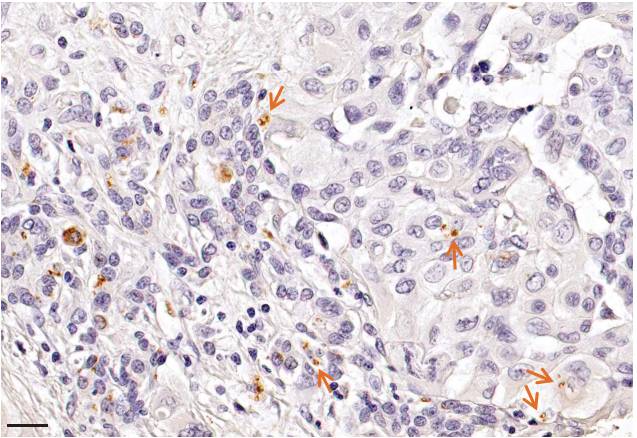
(细菌脂多糖抗体标记的肿瘤组织,箭头所指为被标记的细菌)
在肿瘤微环境中,肿瘤细胞,其他有机体共同组建了这一系统,它们在内部相互协作,使得目前针对单一目标的肿瘤药物很难起到卓有成效的效果。而更为棘手的,微环境的结构复杂性使得其变化的可能极具增加,倘若肿瘤细胞与微生物形成了有效的共生组合,以微生物繁殖变异的速度,仅需很短的时间就可能实现对已有药物的耐药。
我们暂且不考虑微生物变异的绝对速度,仅仅考虑微生物变异与新药研发的相对速度,似乎这根本不是一场势均力敌的较量,仿佛我们刚刚在肿瘤免疫中看到的希望迅速的湮灭了。
不过,我们也可以换个角度思考问题,论变化、变异的速度,我们肯定不是微生物的对手,毕竟这场以“快”为规则的战场上,他们是主宰。
生命在地球上已经进化了数百万年,这期间出现了无数的生命形式都是以细胞为基础,这也为以细胞为基础的一系列疾病创造了基础,但是,谁又能说以细胞为基础的生命形式是最终的生命形式呢?
参考来源:Potential role of intratumor bacteria in mediating tumor resistance to the chemotherapeutic drug gemcitabine