关于发布《预防性使用质子泵抑制剂及处方精简专家指导意见》的通知
粤药会〔2019〕82号
本目录已在中国知网优先出版,引用格式为:
[1]广东省药学会.预防性使用质子泵抑制剂及处方精简专家指导意见[J/OL].今日药学[2019-07-01].
http://kns.cnki.net/kcms/detail/44.1650.R.20190701.1517.002.html.
各医疗机构:
“处方精简”是指对可能导致患者损害或患者不再获益的用药,减少该药剂量或停用该药的计划和管理过程;其目标是减少用药负担和损害,同时维持或提高患者生活质量。该定义由本会于2017年引入国内,并在《今日药学》杂志发表国内第一篇专论,现已广泛传播。
质子泵抑制剂(proton pump inhibitor,PPI)目前广泛用于治疗胃食管反流病、消化性溃疡、幽门螺杆菌感染、上消化道出血、卓-艾综合征等酸相关性疾病。PPI不合理使用主要表现在预防性用药指征不明确及预防疗程过长。这在其他国家,如加拿大,也是一个广泛存在的问题。
为规范PPI的使用,广东省药学会组织专家制定了《预防性使用质子泵抑制剂及处方精简专家指导意见》,
现予以印发,供各医疗机构参考。
各单位在执行过程中遇到任何问题,请及时向本会反映。
联系地址:广州市东风东路753号东塔701室 广东省药学会 510080
联系电话:(020)37886326,37886321
传 真:37886330
电子邮箱:[email protected]
网 址:http://www.sinopharmacy.com.cn
附件:
1、
《预防性使用质子泵抑制剂及处方精简专家指导意见》
起草专家组
2、
《预防性使用质子泵抑制剂及处方精简专家指导意见》
(请在本会网站“下载专区”下载)
广东省药学会
2019年7月1日
附件1:
《预防性使用质子泵抑制剂及处方精简专家指导意见》
起草专家组
预防性使用质子泵抑制剂及处方精简专家指导意见
(广东省药学会2019年7月1日发布)
质子泵抑制剂(proton pump inhibitor,PPI)通过抑制胃壁细胞上的H
+
/K
+
-ATP酶,强而持久地抑制胃酸分泌,目前PPI广泛用于治疗胃食管反流病、消化性溃疡、幽门螺杆菌感染、上消化道出血、卓-艾综合征等酸相关性疾病。
然而,随着PPI的广泛使用,其潜在风险和不合理应用问题逐渐凸显。IMS数据显示,2008年我国PPI总销售金额约为54.1亿元(其中口服16.8亿元,针剂37.3亿元),2017年为235.6亿元(其中口服占67.9亿元,针剂为167.7亿元),仅次于抗生素。一项国内研究显示从2004年到2013年10年间PPI处方量增长10.4倍,PPI支出增长10.1倍
[1]
。PPI不合理使用是一个全球性问题,一项对欧美国家PPI使用的文献分析显示,平均PPI不合理使用率高达57%
[2]
。
国内相关报道显示,77%以上使用PPI的住院患者属于预防性用药
[3]
,门诊处方中符合PPI适应证者亦不足40%
[4]
。国内一项针对住院患者进行的研究结果显示,在759例接受PPI药物治疗的患者中,预防性使用的的比例高达67.98% ;其中,296例未合理使用PPI药物的患者中,无适应证用药最为常见,占67.23%;其次为用法用量不适宜、溶剂选择不当、存在药物相互作用、用药疗程过长等
[3]
。
目前PPI的不合理使用主要表现在预防性用药指征不明确和预防疗程过长。为此,广东省药学会组织药学及临床专家特制定本指导意见,为规范临床预防性使用PPI提供参考。
正常的胃黏膜屏障能够保护胃黏膜结构和功能的完整性。胃黏膜屏障的保护机制包括黏膜表面富含碳酸氢钠的黏液保护层、黏膜上皮的不断更新、跨黏膜的酸碱交换,以及正常的黏膜微循环。胃黏膜结构和功能的完整性依赖于正常的黏膜保护机制和胃酸分泌之间的平衡。胃黏膜防御功能减弱(如胃黏膜缺血、缺氧等)和胃黏膜损伤因素的相对增强是急性胃黏膜病变的主要机制。临床上最常见的引起胃黏膜病变的原因包括:急性应激反应、药物、创伤以及物理因素等。临床预防性使用PPI,可迅速控制并减少胃酸的分泌,明显降低胃酸对黏膜的进一步损害作用。
近期发表于《Lancet Gastroenterology Hepatology》的荟萃分析,纳入了580项预防溃疡病的临床研究,整体受试者超过11万人,其结果证实预防性使用PPI可减少5倍内镜下溃疡发生风险,也显著减少上消化道出血的发生(
OR
0-40,0.32-0.50;
P
<0·0001)
[5]
。在预防效果上,PPI优于前列腺素或H
2
受体拮抗剂(H
2
RA)。一项针对重症患者的网状荟萃分析,纳入57项试验共7293例患者,相比硫糖铝、H
2
RA,PPI预防应激性溃疡更有效
[6]
。
预防性使用PPI应严格掌握使用指征,一次只需使用一种PPI。根据患者病情变化,可由静脉用药序贯调整为口服用药。不同PPI批准的适应证有所差异,适应证掌握不当与PPI过度处方密切相关
[3]
。
不同PPI的说明书推荐剂量不同,表 1汇总了目前国内常用PPI的每日常规剂量。
表1 口服/注射用PPI常规剂量
|
PPI
|
常规剂量(口服)/d
|
常规剂量(注射用)/d
|
|
奥美拉唑
|
40 mg
+
|
40 mg
|
|
兰索拉唑
|
30 mg
|
30 mg
*
|
|
泮托拉唑
|
40 mg
|
40 mg
|
|
雷贝拉唑
|
20 mg
|
20 mg
#
|
|
艾司奥美拉唑
|
40 mg
+
|
40 mg
|
|
艾普拉唑
|
10 mg
|
10 mg(首剂加倍)
|
注:
+
为有MUPS剂型,可溶于水服用(或胃管入);
*
为未在中国上市原研注射剂型;
#
为无进口原研针剂。
从1842年Curling首次报道严重烧伤后的急性十二指肠溃疡
[7]
,到1932年Cushing报道了颅内肿瘤、创伤或其他占位病变引起的颅内高压导致的胃十二指肠溃疡
[8]
,人们发现胃粘膜对危重疾病中的血液动力学变化和炎症信号都极其敏感,当个体遭受异常增加的生理需求会诱导急性胃粘膜损害,发生糜烂,溃疡,出血等病变,严重者可导致消化道穿孔,危及患者生命。
SRMD常见于急诊,重症监护病房(ICU),神经外科,普通外科等。我国一项多中心回顾研究显示,神经外科重症患者14 d内消化道出血发生率高达12.9%, 出现应激性上消化道出血的平均时间为2.9 d
[9]
。
预防性用药指征:
临床应根据疾病情况结合危险因素判断患者是否需要使用PPI预防SRMD。危险因素汇总见表2
[10-13]
。
用药建议:
预防目标是控制胃内pH≥4,可选择H
2
RA和PPI
[14]
。PPI静脉滴注,常规剂量,用药疗程一般3~7 d,当患者病情稳定,可逐渐停药
[15-16]
。
表2 SRMD的危险因素
|
危险因素
|
证据级别
|
预防建议
|
|
-呼吸衰竭,机械通气超过48 h
-凝血机制障碍:国际标准化比值(INR)>1.5,血小板<50×
10
9
/L或部分凝血酶原时间(PTT)>正常值2倍
|
A
|
独立危险因素
(具有一项即可使用常规剂量PPI预防SRMD)
|
|
-严重颅脑、颈脊髓损伤(Glasgow昏迷指数≤10)
-严重烧伤(烧伤面积>30%)
-严重创伤、多发伤(创伤程度评分>16)
-急性肾功能衰竭或急性肝功能衰竭
-多器官功能不全或衰竭
-休克或持续低血压
-急性呼吸窘迫综合征(ARDS)
-全身感染、脓毒症、败血症
-心脑血管意外(Glasgow昏迷指数≤10)
-颅内感染(Glasgow昏迷指数≤10)
-严重心理应激,如精神创伤、过度紧张等
|
B
|
严重危险因素
(具有一项即可使用常规剂量PPI预防SRMD)
|
|
-ICU住院时间>1周
-粪便隐血持续时间>3d
-大剂量使用糖皮质激素(剂量>氢化可的松250 mg﹒d
-1
或等效剂量的其它糖皮质激素)
-合并使用非甾体类抗炎药(NSAIDs)
-长期大剂量使用免疫抑制剂
-长期禁食或行胃肠外营养
-男性
-年龄>65岁
-(1年内)有消化道出血病史
-(1年内)有消化性溃疡史
-使用抗凝剂
|
C
|
潜在危险因素
(符合两项者可使用常规剂量PPI预防SRMD)
|
|
复杂手术,如复杂肝脏手术、器官移植、
手术时间较长(>3 h)等
|
C
|
择期外科手术
(结合疾病本身选择使用PPI预防SRMD)
|
注:A为多项随机对照试验或Meta分析;B为单项随机对照试验或大型非随机对照试验;C为专家意见或回顾性研究。
2.2.1预防NSAIDs相关的消化道黏膜损伤非甾体抗炎药(non steroid anti-inflammatory drugs,NSAIDs)是一大类具有抗炎、镇痛、解热作用的药物。消化道黏膜损伤是使用NSAIDs最常见的不良反应。在长期口服NSAIDs的患者中,约40%的患者发生内镜下消化性溃疡
[17]
。PPI可有效降低NSAIDs引起的上消化道黏膜损伤
[18]
。
幽门螺杆菌(
Helicobacterpylori,
Hp)感染是NSAIDs相关消化道溃疡的独立风险因素,增加服用NSAIDs患者发生上消化道并发症的风险。一项随机研究显示,开始长期NSAIDs治疗前筛查和根除Hp显著降低溃疡并发症风险。因此,针对高危患者,在接受长期NSAIDs和阿司匹林治疗前应检查并根除Hp
[19]
。
预防性用药指征:
临床应综合评估患者发生NSAID相关的消化道黏膜损伤的危险因素和风险等级,判断是否需要预防性使用PPI,见表3。
用药建议:
(1)
PPI是预防NSAIDs相关上消化道损伤的首选药物。(2)说明书推荐剂量的H
2
RA可预防十二指肠溃疡发生,但不能预防胃溃疡发生,双倍剂量的H
2
RA能有效降低NSAIDs诱导的内镜下胃溃疡的发生
[21-23]
。
表3 NSAIDs溃疡并发症的风险等级及预防建议
[20]

2.2.2 预防抗血小板药物消化道损伤心脑血管疾病是致死致残的最常见原因,抗血小板治疗能够显著减少心脑血管事件,尤其对于急性冠脉综合征(ACS)和支架植入术后患者。但抗血小板药物同时也会显著增加消化道出血发生率,尤其双联抗血小板治疗(DAPT)和联合抗凝治疗时
[24-25]
。消化道出血会增加心血管不良事件和死亡率
[26]
,预防消化道损伤及出血对长期应用抗血小板药物患者至关重要。高质量RCTs研究证实
[27-28]
PPI能显著降低抗血小板药物致上消化道出血的发生率,临床应基于患者出血风险给予预防。
预防性用药指征:
抗血小板药物消化道损伤风险及具体预防建议见表4。
用药建议:
服用抗血小板药物12个月内为消化道损伤的多发阶段,3个月时达高峰
[37-38]
。具有消化道损伤危险因素的患者在初始抗血小板药物治疗的前6个月应联合使用常规剂量PPI,6个月后可改为隔天服用PPI或H
2
RA
[39]
。
表
4 抗血小板药物消化道损伤风险及预防建议
[29-36]
|
危险因素
|
预防建议
|
|
有消化道出血或溃疡病史
双联抗血小板
合用抗凝药物
合用NSAIDs
合用大剂量糖皮质激素
|
具有1项即可使用常规剂量PPI预防消化道损伤
|
|
年龄>65岁
Hp感染
有消化不良或有胃食管反流症状
长期饮酒
|
具有2项即可使用常规剂量PPI预防消化道损伤
|
随着我国内镜技术的快速发展,胃黏膜病变内镜黏膜下剥离术(endoscopic submucosal dissection,ESD),已成为早期胃癌等胃黏膜病变内镜下微创治疗的标准方法。ESD术中因直接剥离深度超过黏膜层,符合“溃疡”的定义,又称为人工溃疡或医源性溃疡
[40]
。人工溃疡部位的血管可在各种理化因素作用下破裂出血,促进溃疡尽快愈合可降低迟发性出血风险。
预防用药指征:
(1)我国2017年ESD指南建议术后使用PPI,降低迟发性出血和促进溃疡愈合
[41]
。
(2)胃内ESD术后应常规使用抑酸剂,术后用药剂量及疗程,需考虑两方面问题:是否存在再出血发生风险;是否存在延迟愈合风险
[42-46]
。
用药建议:
(1)常规剂量,1日2次,3~5 d。若发生术后迟发性出血,高危患者推荐大剂量方案:如艾司奥美拉唑 80mg静注,8mg﹒h
-1
维持72h。
(2.)当考虑出血停止后,继续口服维持
4~8
周。
表
5 ESD所致人工溃疡出血预防建议

多重用药及无适应证用药不仅增加药物不良反应风险,还会增加患者的医疗负担。研究显示,约60%从ICU转出的患者,以及约35%出院的患者,均无适应证使用抑酸剂
[47]
。随着PPI的全球性广泛使用,长期安全性备受学术界关注,大量非随机对照研究得出的异质性结论让临床医师倍感困惑。
2017美国胃肠病学会(AGA)组织专家综述了长期使用PPI的风险和获益,需长期使用 PPI 治疗的疾病主要有胃食管反流病(GERD)、Barrett’s 食管炎和预防非甾体类抗炎药(NSAIDs)引起的溃疡相关出血等。目前可以减轻长期PPI使用潜在风险的最佳方案仍是严格掌握用药指征,确需用药时最好能减到最小效应剂量。临床上需权衡长期使用PPI的利弊,合理使用
PPI
[48]
。
处方精简(Deprescribing),是指对可能导致患者损害或患者不再获益的用药,减少该药剂量或停用该药的计划和管理过程;其目标是减少用药负担和损害,同时维持或提高生活质量。处方精简是良好处方行为的一个组成部分,减少过高的用药剂量,或停用不再需要的药物。处方精简的主要方式包括停药、换药和减少用药剂量
[49]
。2017年加拿大多个学会联合发布了1项PPI处方精简指南,为临床治疗性使用PPI提供精简流程和指导,用于帮助临床医师何时、如何对PPI进行减量或停药
[50]
。本指导意见根据前文所述预防性使用PPI给予处方精简流程推荐,以帮助临床医师对预防性使用PPI进行评估,最大限度减少不必要用药,见图1。
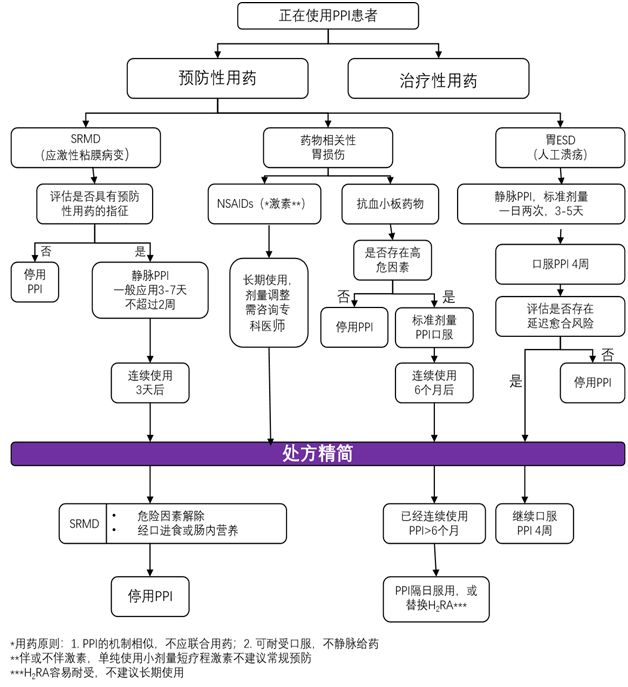
图1预防性使用PPI处方精简流程
PPI主要通过特异性作用于胃壁细胞分泌膜上的胃酸分泌的最终环节H-K-ATP酶(即质子泵),不可逆地与其结合,使其失去活性,从而抑制胃酸分泌。
从药理学角度,可把PPI 分为两大类:
第一代PPI 包括奥美拉唑、兰索拉唑和泮托拉唑,
第二代(新一代)PPI 如雷贝拉唑、艾司奥美拉唑。
相比第一代,第二代PPI起效更快,抑酸效果更好,能24 h持续抑酸,个体差异少
[51]
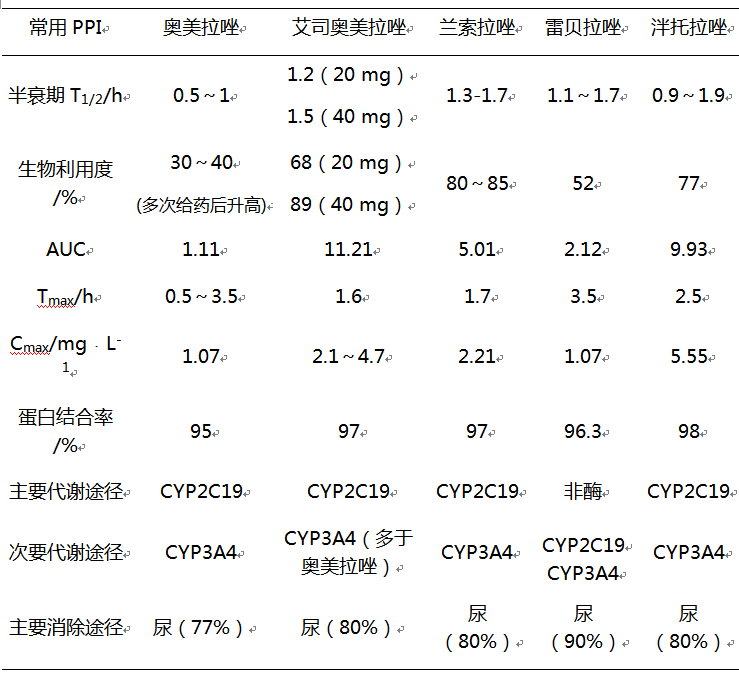
。常用PPI的药代动力学特点比较,见表6。
表6 PPI的药理学特点比较
PPI抑酸作用强大而持久,故用药期间不宜再使用其他抗酸剂或抑酸剂。抗酸剂(硫糖铝、氢氧化铝、氧化镁、碳酸氢钠)需要在酸性条件下发挥作用,与PPI具有药效拮抗作用。
PPI与其他药物合用时,可能对药物代谢产生影响。主要包括两个方面:(1)抑酸影响药物的吸收:抑酸可减少左旋甲状腺素、酮康唑、伊曲康唑、阿扎那韦等吸收,也可增加硝苯地平、地高辛、阿仑膦酸钠等吸收。(2)影响经CYP450酶代谢的药物:例如苯妥英钠、华法林、卡马西平、他汀类、氯吡格雷等。
PPI与氯吡格雷联用的相互作用存在争议,确需与氯吡格雷联用时,建议使用争议较小的PPI
[38]
。
质子泵抑制剂水溶液不稳定,在酸性溶液中可快速分解而出现聚合、变色,故要避免与酸性药物同用。静脉滴注适宜选用0.9%氯化钠注射液,避免使用5%葡萄糖注射液等偏酸性溶媒。PPI对pH值的依赖性很强,因此药品必须按照说明书指导应用。禁止与其他溶剂或药物溶解和稀释,配置的溶液不能与其他药物混合或在同一注射器中合用。
口服制剂一般为肠溶制剂,服用时应以整片(粒)吞服,不得咀嚼、压碎和溶解。原研的奥美拉唑和艾司奥美拉唑拥有MUPS剂型(多单位微囊系统),鼻饲管患者可以将药品溶于水后经鼻饲管注入。
常见PPI注射剂型的配置方法略有差异,奥美拉唑、艾司奥美拉唑和泮托拉唑既可静脉注射也可用于静脉滴注。其中奥美拉唑冻干制剂存在静脉滴注和静脉推注两种配方,前者为避免与大量氯化钠注射液或葡萄糖注射液稀释时发生氧化变质而加入了EDTA(1.5mg/支);而供静脉推注用的制剂因稀释剂用量小,推注时间短而不必加入EDTA,但配有助溶剂聚乙二醇400和pH调节剂枸橼酸的专用溶剂。临床使用中不可互相混用。
表7 常见PPI注射剂型使用方法

PPI常见的不良反应包括:
头痛、胃肠道症状(腹泻、恶心、胃肠胀气、腹痛、便秘)、口干、关节痛、肌痛、肌无力、间质性肾炎、视力模糊、过敏症、全血细胞减少、血小板减少、粒细胞缺乏症、肝功能障碍等。
长期使用PPI(通常定义为 6个月以上),应警惕PPI可能相关的潜在不良影响,包括肾脏疾病、痴呆、骨折、心肌梗死、小肠细菌过度生长、自发性细菌性腹膜炎、萎缩性胃炎、低镁血症、艰难梭状芽孢杆菌感染、肺炎、维生素B
12
和铁吸收不良、肿瘤等。长期使用PPI,应采取处方精简原则,使用最低有效剂量,确保用药安全、有效、经济。
4.5.1肝、肾功能减退患者PPI在人体内主要经肝脏代谢,经肾脏排泄。在肝、肾功能减退时,PPI的选用及剂量调整需要考虑肝、肾功能减退时对药物在体内代谢、排泄的影响程度,按照说明书选择合适的PPI。
4.5.2老年患者老年人胃内酸度与青年人类似,酸相关性疾病可以用PPI治疗。一般情况下,老年人肾功能不全和轻中度肝功能不全者的PPI药代动力学与青年人相似,无需调整剂量。但由于老年患者的用药特点,应在处方时候尽量考虑低剂量,短疗程的治疗方式。

















