
各位朋友大家好啊,很多从临床/实验方向转来生信“试试水”的生物大佬和小白们是不是“试试水”都偏爱简单的思路,此时单基因研究简单高效,显然极具有性价比!那么现在都把单基因分析 “卷出花儿”来了,单基因分析还如何做出创新性呢?`馆长看见一篇让人眼前一亮的文章,南京医科大学大佬的这篇《An integrated investigation of mitochondrial genes in COPD reveals the causal effect of NDUFS2 by regulating pulmonary macrophages》,选题上文章选择了巨噬细胞/线粒体双热点,具有一定的创新性,文章采用了联合思路,机器学习+MR分析+单细胞测序分析+实验验证这套组合拳更是层层助力,令人眼花缭乱,现在让咱们来看一看,这究竟有何奥妙之处?
1、
本研究利用
机器学习和MR分析
相结合这一热门研究方法,系统、多维度地反映了COPD与线粒体之间潜在的因果关系。
2、
本研究通过GEO数据库挑选出COPD相关DEGs,联合MitoCarta3.0数据库线粒体相关基因挑选出了达
353个MitoDEGs,
构建并可视化了MitoDEGs的蛋白质互作(PPI)网络
筛选出32个hub MitoDEGs。机器学习和MR分析进一步筛选出NDUFS2、CAT和MRPL2 这3个COPD的因果相关MitoDEGs。
3、
在生物信息学分析的基础上,结合单细胞测序分析构建nomogram 模型,并通过体外实验验证了生信分析的结果。“干湿结合”进一步增强了结果的可靠性。
Ps:
还在为错过了最新的实验热点而焦急吗?还在为联合思路不会设计而发愁吗?想简单高效发表高分生信文的朋友,直接滴滴馆长吧,专业团队很靠谱哦~
定制生信分析
生信服务器
加好友
备注“99”
领取试用

题目:一项慢性阻塞性肺疾病线粒体基因的综合研究
揭示了NDUFS2通过调节肺巨噬细胞的因果作用
杂志:Biol Direct
影响因子:IF=5.9
发表时间:2025年1月
研究背景
慢性阻塞性肺疾病(COPD)是一种异质性肺部疾病,许多其他与慢性阻塞性肺病相关的遗传变异已被
确定。然而它们与COPD的因果机制研究尚不清晰。人体肺组织由多达40多种细胞组成,但是以往关于线粒体功能障碍的研究多数集中在上皮细胞上,而鲜少有COPD背景下其他细胞类型的线粒体动力学以及它们潜在的相互作用的相关报道。本文意在通过生物信息分析结合实验探究线粒体功能障碍与COPD之间的因果关
系。
数据来源
|
数据集/队列
|
数据库
|
详细信息
|
|
GSE103174
|
GEO
|
321例COPD样本和
164例正常对照样本
|
|
GSE106986
|
GEO
|
|
GSE151052
|
GEO
|
|
GSE38974
|
GEO
|
|
GSE47460
|
GEO
|
|
GSE57148
|
GEO
|
|
|
MitoCarta3.0
|
353个MitoDEGs
|
研究思路
从公共存储库NCBI GEO收集了COPD患者和对照个体的大量人类肺组织转录组数据集鉴定挖掘了COPD相关DEGs,联合MitoCarta3.0数据库线粒体相关基因相交挑选出了MitoDEGs。
构建并可视化了MitoDEGs的蛋白质互作(PPI)网络,用于探索hub MitoDEGs,随后对其进行机器学习和MR分析,筛选出COPD的因果相关MitoDEGs。COPD人肺组织单细胞RNA测序(scRNA-seq)数据集证实了肺内各因果MitoDEGs的细胞表达分布构建nomogram模型进行COPD影响因素风险预估。结合功能分析和体外实验来验证生信分析结果。
Ps:还在为生信分析的速度发愁吗?别慌!“工欲善其事,必先利其器”,联系馆长可免费试用服务器,更多优惠欢迎来询~
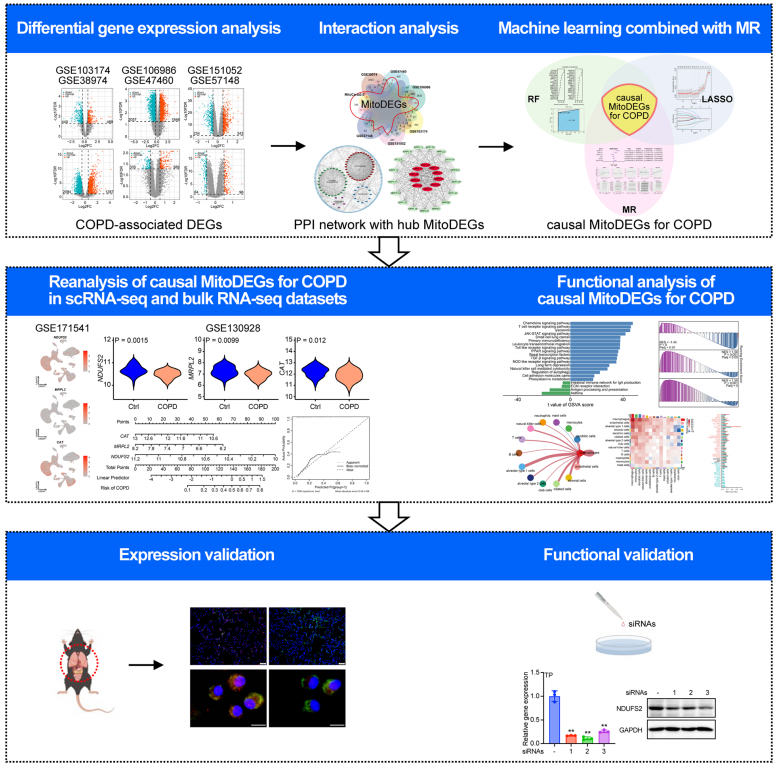
研究结果
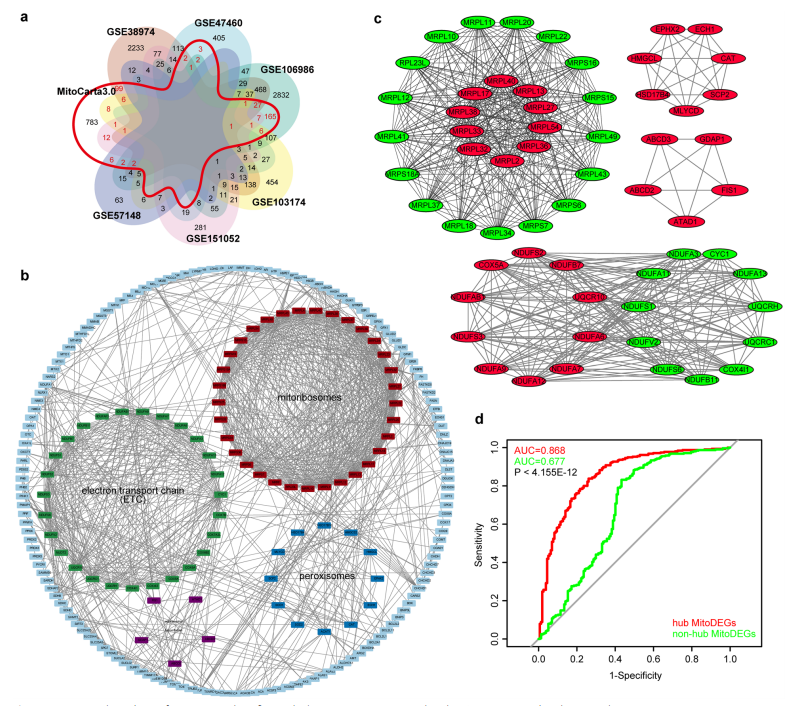
差异基因筛选+PPI网络的构建与分析
从公共存储库NCBI GEO收集了COPD患者和对照个体的大量人类肺组织转录组的6个数据集鉴定挖掘COPD相关DEGs,将每个数据集的COPD相关基因与MitoCarta3.0数据库线粒体相关基因取交集,共挑选出了353个
MitoDEGs
。对这些MitoDEGs进行了PPI网络分析,其中组成线粒体糖体、过氧化物酶体和电子传递链(ETC)的基因以及参与线粒体融合/裂变的基因自动聚集在一起(图b)。随后,使用MCODE插件从4个显著模块中鉴定出32个与COPD相关的hub MitoDEGs,分别是MRPL2、MRPL13、MRPL27、MRPL17、MRPL36、MRPL32、MRPL33、MRPL38、MRPL40、MRPL54、NDUFS2、NDUFS3、NDUFB7、NDUFAB1、NDUFA9、NDUFA7、NDUFA12、NDUFSA6、COX5A, UQCR10, EPHX2, ECH1, CAT, SCP2, MLYCD, HSD17B4, HMGCL, ABCD3, ABCD2, ATAD1, GDAP1, and FIS1。
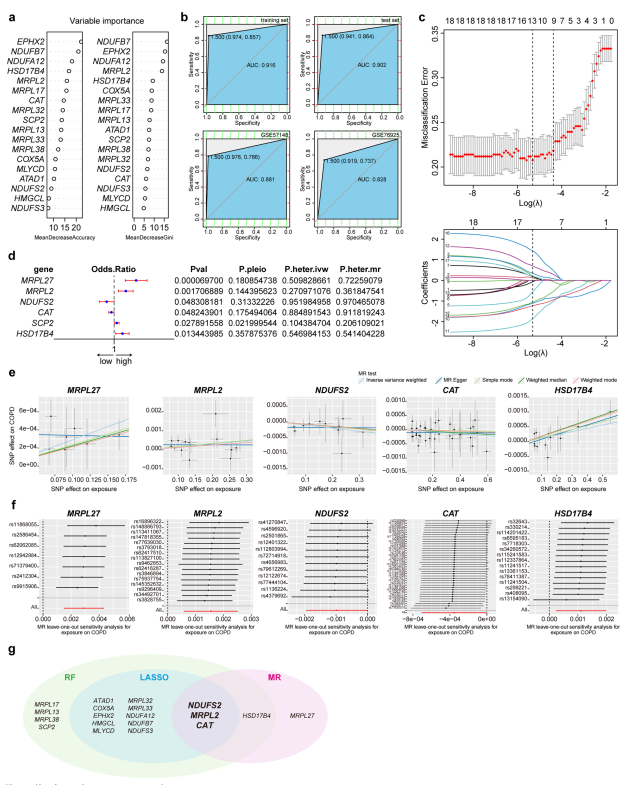
机器学习+MR分析
通过RF分析(图
a)首先从32个
hub
MitoDEGs
挑选出的18个基因作为特征基因,通过LASSO回归将18个特征基因进一步减少到13个(图c)。结合这32个
hub
MitoDEGs的eQTL数据,通过双样本MR分析推断枢纽MitoDEGs(暴露)与COPD(结果)之间的因果关系,相关基因即:MRPL2、MRPL2
7、CAT、NDUFS2和HSD17B4(图e)。其中NDUFS2和CAT对COPD可能存在保护作用,而MRPL2、MRPL27和HSD17B4这三个基因可能在COPD机制中是有害的。本文将MR分析的5个COPD因果
MitoDE
Gs
与通过RF分析和LASSO回归先后确定的13个特征
MitoDEGs
相交进一步减少到3个,即 NDUFS2、MRPL2和CAT(图4),进一步提高了分析结果的可靠性。
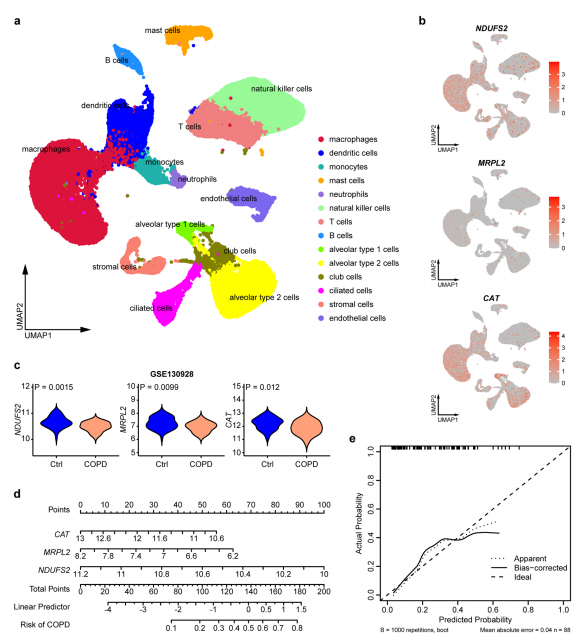
MitoDEGs单细胞测序分析
分析在之前发表的具有不同吸烟史的COPD患者和对照个体人类肺组织的单细胞RNA测序数据(GSE171541),发现NDUFS2、MRPL2和CAT在单核吞噬细胞系统(尤其是在巨噬细胞)中富集(图b)。然而,MRPL
2的整体表达水平不如NDUFS2和CAT,但CAT在肺泡Ⅱ型细胞也显著丰富。由于巨噬细胞在COPD发展中协调肺部炎症的关键作用,以及MR分析确定这些基因在COPD发病机制中具有因果作用,其表达变化情况被进一步证实。结果显示在COPD患者中,与MR分析预测的保护作用相一致, NDUFS2和CAT巨噬细胞中表达水平下降,而
潜在的有害致病基因
MRPL2也先下降了。研究肺巨噬细胞中NDUFS2、MRPL2和CAT的表达水平,通过logistic回归构建了COPD的
nomogram 模型
(图de),结果随着肺巨噬细胞中NDUFS2、MRPL2和CAT的下调,COPD风险增加,再次揭示MR分析结果与MRPL2表达关于COPD风险的不一致。值得注意的是,NDUFS2被认为是COPD的一个保护因子,不仅在MR分析中其下调被预测与COPD可能存在因果关系,在nomogram 模型预测中也对COPD风险影响最大。
功能分析提示NDUFS2在巨噬细胞功能和互作中的调节作用
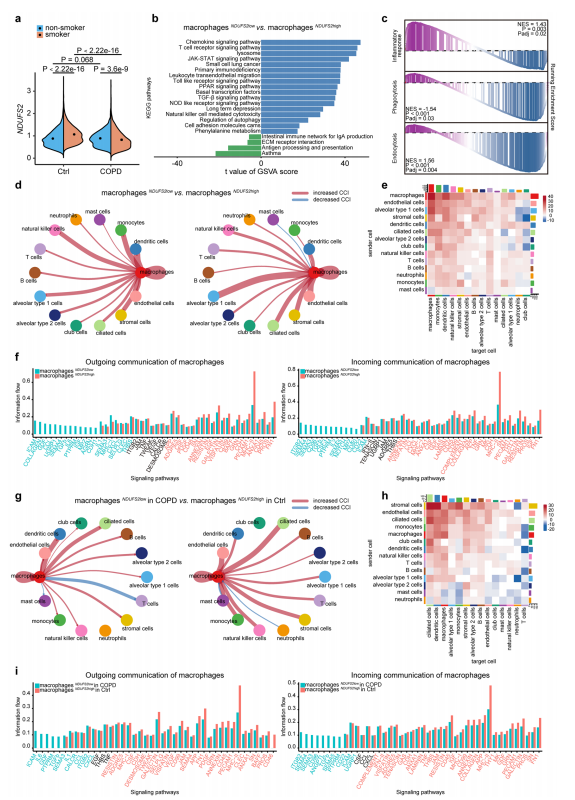
在非COPD患者中,与非吸烟者相比,吸烟者肺巨噬细胞中的NDUFS2在表达升高;但在COPD患者中,与非吸烟者相比,吸烟者NDUFS2却表现为显著的下降(图a)。NDUFS2低表达的巨噬细胞(
macrophages
NDUFS2low
)相对于高表达的(
macrophages
NDUFS2high
)显示出炎症相关通路的激活、生理免疫功能的抑制(图b)
和细胞之间的互作(CCIs)显著增加
(尤其是与固有免疫细胞和结构细胞之间的相互作用增强)。巨噬细胞中NDUFS2表达水平的变化可能在COPD的炎症核心机制中发挥关键作用,而不是COPD发展的结果。这与通过MR分析和nomogram模型推测的结果相一致。
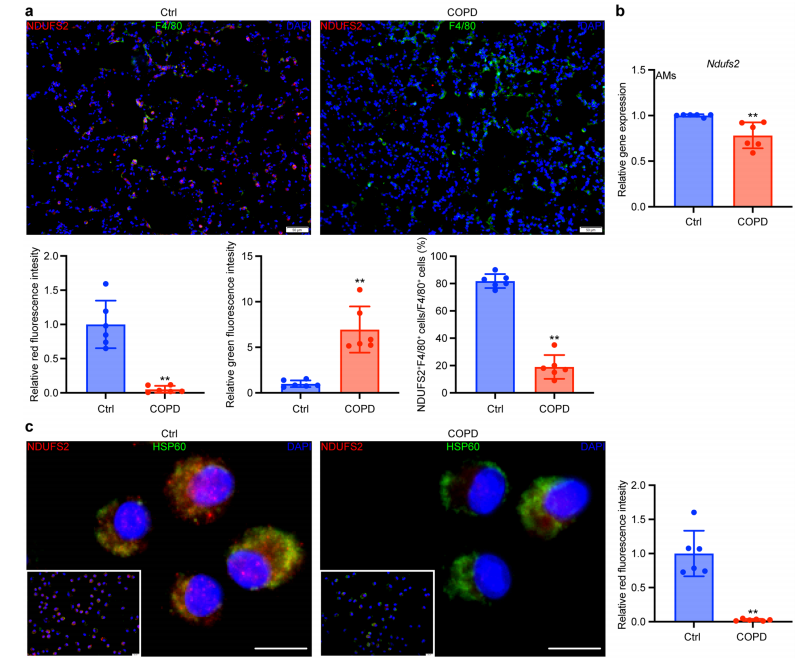
COPD小鼠AMs中NDUFS2表达降低
基于人肺组织scRNA-seq数据集分析发现,仅COPD吸烟者的肺巨噬细胞中NDUFS2的表达水平显著下降。该结论在香烟烟雾诱导的COPD小鼠模型中得到了验证。组织病理学证实COPD小鼠肺部的变化后
,免疫荧光染色显示与对照组相比,COPD小鼠F4/80标记的肺部巨噬细胞中NDUFS2显著减少。qPCR结果显示,与对照相比,COPD小鼠肺泡巨噬细胞中NDUFS2转录水平同样呈现出了显著下降趋势。
沉默NDUFS2可导致巨噬细胞的促炎表型和吞噬功能紊乱







