2017年7月7-8日,中国临床肿瘤学会(CSCO)联合美国临床肿瘤学会(ASCO)在上海成功举办了“临床肿瘤学新进展学术研讨会——Best of ASCO(BOA)event in China”。会议期间,同时召开了“2017 Best of ASCO 肺癌精准医学进展卫星会”。本场卫星会由吴一龙教授和陆舜教授担任主席,周清教授总结《ASCO靶向治疗新进展》,范云教授分享《优化T790M耐药患者临床实践》,多位肺癌领域专家就“如何优化 EGFR M+患者临床实践”展开专题讨论。会场座无虚席,现场讨论热烈,以下分享会议精彩内容。2017 ASCO 靶向治疗新进展——EGFR突变篇

周清教授
周教授从以下4个方面展开介绍:
(一)TKI用于辅助治疗
外科临床研究的生命周期接近10年,是远长于晚期肺癌的临床研究周期(中位时间位4.3年)。因此,开展围术期的临床研究,对于研究者而言是一个非常大的挑战。在众多的历史背景下,我们终于在今年的ASCO会议上来自中国的CTONG1104研究,取得了令人鼓舞的研究结果。周教授指出,一个研究的成败,与研究设计有着至关重要的关系。CTONG1104研究在2009年开始研究设计,2011年研究正式开始,这是早于BR19和RADIANT研究结果公布的,这充分说明了研究者前瞻的眼光和大智慧。CTONG1104研究设计如下,完全性切除术后的患者,一组随机接受吉非替尼,另一组接受证据级别最高的VP化疗。
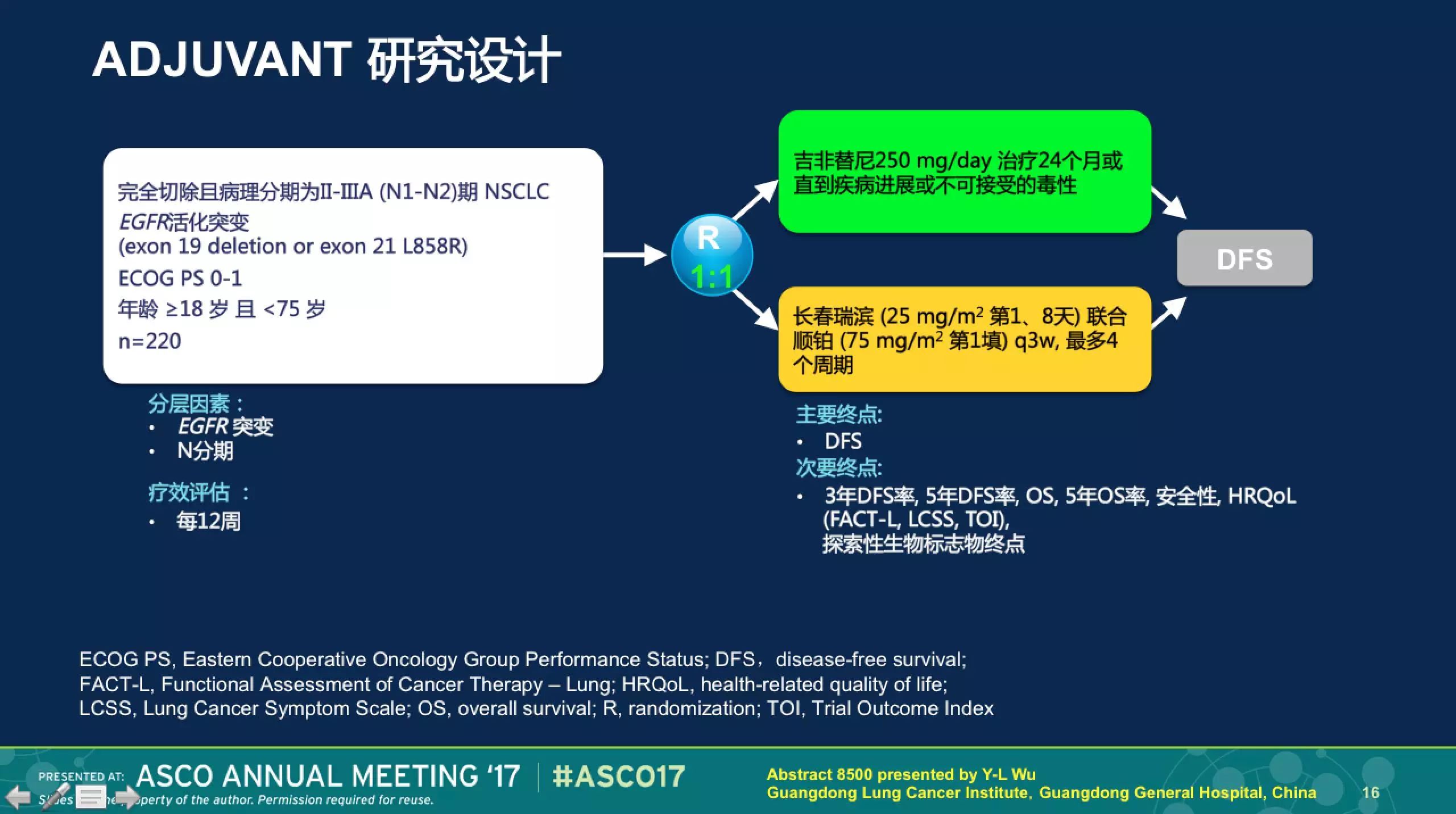 虽然两组在随机之后都有一些患者未按照方案完成试验,但最终两组的基线特征还是非常均衡的。入组人群中2/3左右的病人是N2,这也是临床上从术后辅助化疗中获益最多的患者。研究的主要终点为DFS,这也是今年ASCO会议上跨时代意义的两条曲线,吉非替尼组显著延长DFS达10个月。
虽然两组在随机之后都有一些患者未按照方案完成试验,但最终两组的基线特征还是非常均衡的。入组人群中2/3左右的病人是N2,这也是临床上从术后辅助化疗中获益最多的患者。研究的主要终点为DFS,这也是今年ASCO会议上跨时代意义的两条曲线,吉非替尼组显著延长DFS达10个月。
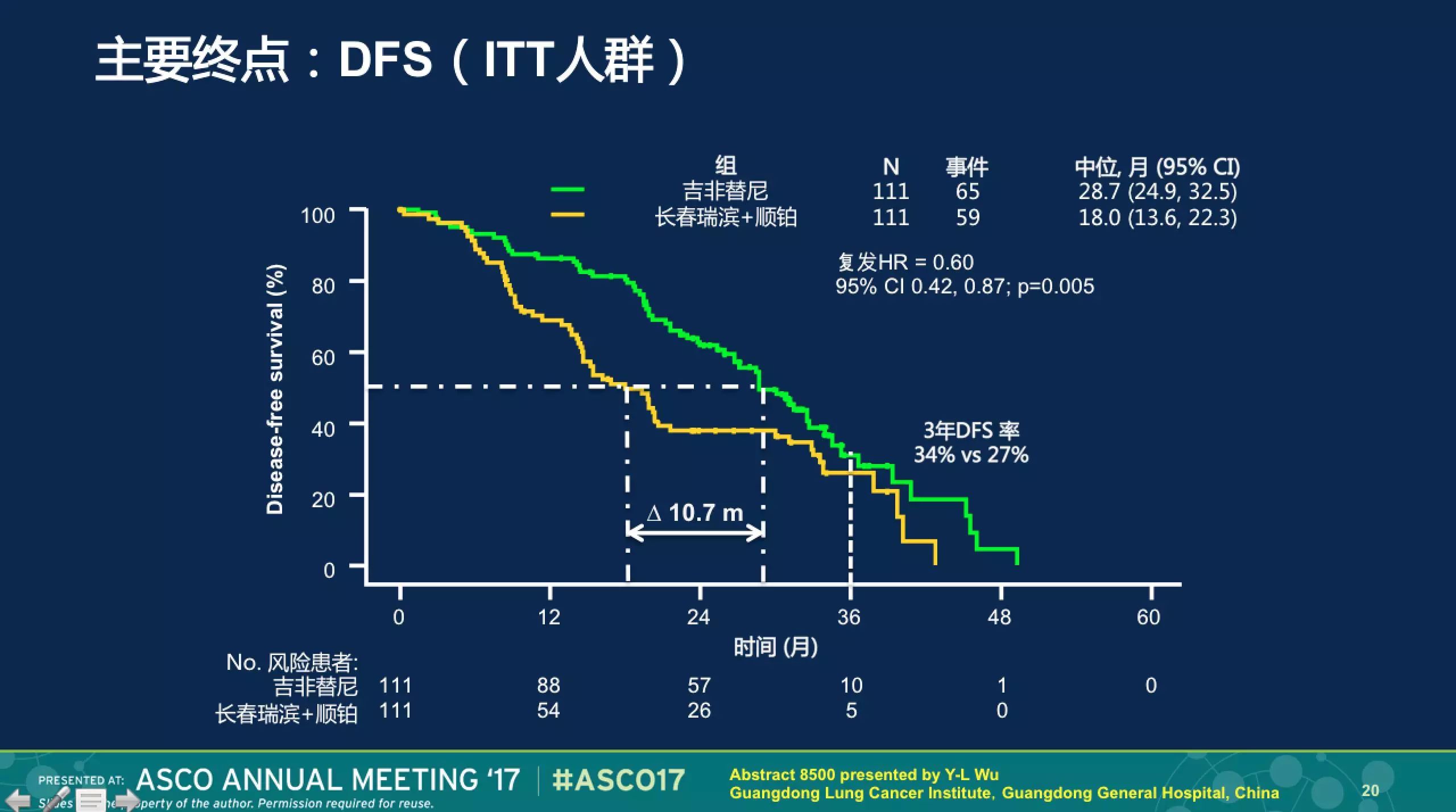 亚组分析显示,对于N2的病人获益更为显著,HR为0.52,也就意味着吉非替尼对比化疗降低了接近一半的疾病进展风险。毒性对比,吉非替尼族和化疗组有着不同的副作用,总体而言,吉非替尼组的3度或以上的不良事件发生率显著低于化疗组(12.3% vs. 48.3%)。生活质量对比,靶向治疗组也显著优于化疗组。
亚组分析显示,对于N2的病人获益更为显著,HR为0.52,也就意味着吉非替尼对比化疗降低了接近一半的疾病进展风险。毒性对比,吉非替尼族和化疗组有着不同的副作用,总体而言,吉非替尼组的3度或以上的不良事件发生率显著低于化疗组(12.3% vs. 48.3%)。生活质量对比,靶向治疗组也显著优于化疗组。
结论:ADJUVANT 达到主要终点,吉非替尼DFS显著优于VP。吉非替尼不良事件与既往报道一致吉非替尼2年的辅助治疗时间是合理安全的;吉非替尼辅助治疗或可成为可切除N1 / N2 EGFR突变NSCLC患者的首选治疗方案。OS是该研究报道以来非常热议的话题,周教授提出了3种可能:1. 如果OS延长,那么术后辅助靶向的地位,毫无疑问是"YES";2. 如果靶向组的生存比化疗组要差,那么辅助靶向的挑战可能会减化,我们希望患者能获得更长;但根据晚期大量临床试验的经验,这种情况出现的可能性不大3. OS相当,那么患者DFS的获益可称之为“获益提前”,这种提前获益,显著延缓了患者的疾病复发事件,同时改善了生活质量,也减轻了患者的心理负担。如果是这种情况,我们对术后辅助靶向的地位仍然是"YES"。
(二)奥希替尼CNS数据
AURA3研究的主要结果在去年的WCLC会议上报道,今年的ASCO会议上报道了奥希替尼治疗脑转移的疗效。AURA3研究的入组人群中,约30%的患者合并脑转移,依据脑转移病灶是否可以测量, CNS全分析集和CNS可评估疗效集。根据基线CNS的影像学评估,分为CNS全分析集(cFAS,包括至少有≥ 1个可测量和/或不可测量的中枢神经系统转移灶的患者)和CNS可评估疗效集(cEFR,仅包括≥ 1个可测量CNS转移灶的患者)。
在CNS可评估疗效集中,奥希替尼CNS的ORR为70%,显著高于化疗组的31%, 奥希替尼组的DCR分别为93%,从以上数字可以看出,奥希替尼颅内的疗效是毫不逊色于颅外的,血脑屏障对于奥希替尼而言,几乎可以忽略。在CNS全分析集中,奥希替尼组CNS的中位PFS显著优于化疗组,分别为11.7m vs. 5.6 m,HR= 0.32; 95%CI:0.15-0.69,P= 0.004。此外,我们还关注到奥希替尼用于脑膜转移也是非常有效的。过去,对于脑膜转移,几乎束手无策,全脑放疗效果不佳;但在AURA3研究中,我们看到新希望,7例软脑膜转移患者中,4例软脑膜病灶得到缓解,其中2 例CR,2 例PR。
(三)一代 VS. 二代
二代对比一代EGFR TKI的临床研究ARCHER 1050也是今年的关注热点。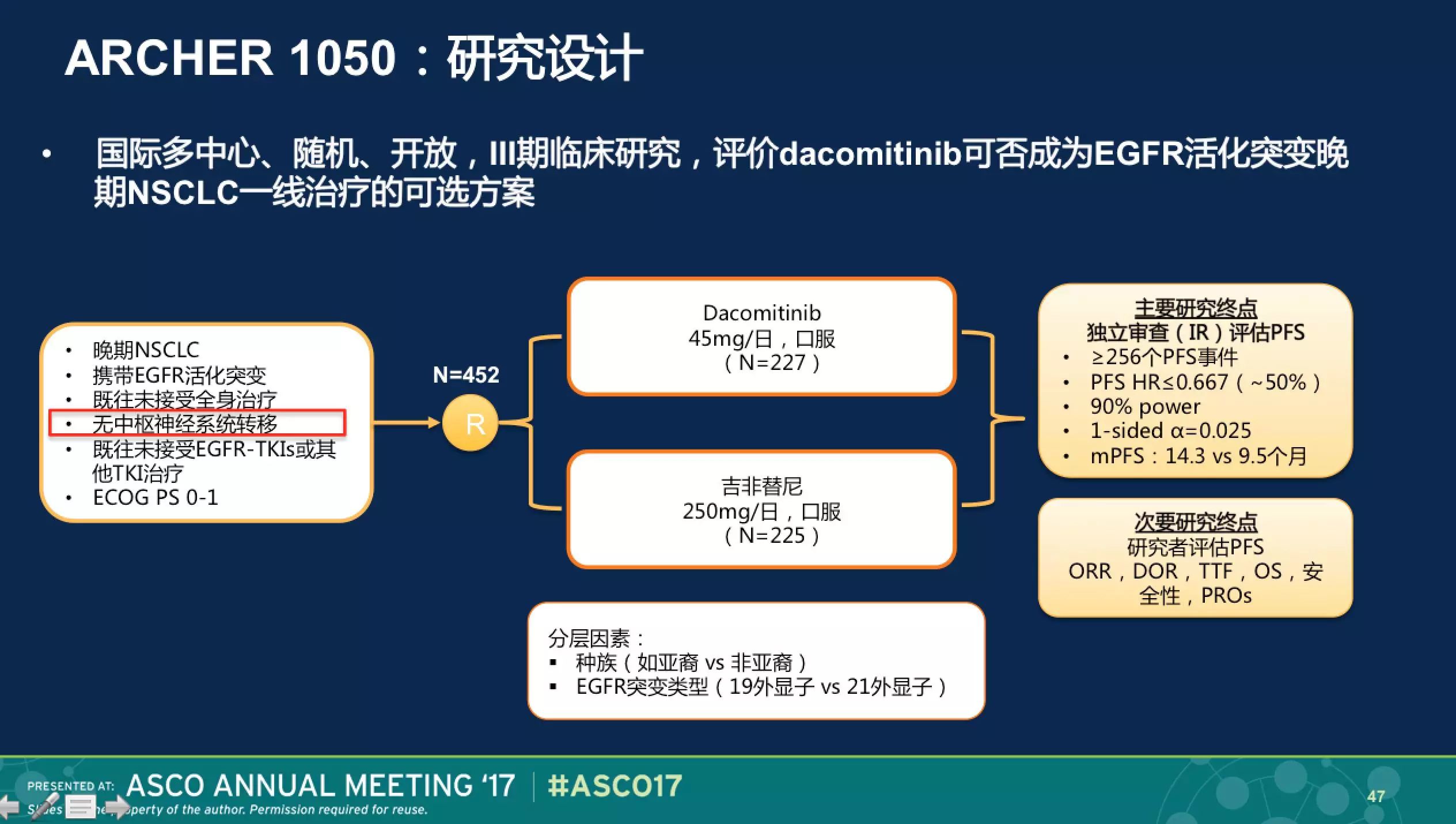 这个研究与Lux-Lung7的研究设计是相似的,但在入排标准中有一些细微差别,ARCHER 1050研究不允许CNS转移患者入组。在疗效对比上,Dacomitinib组的PFS获益明显(14.7m vs. 9.2m),但毒性值得关注,Dacomitinib组有高达66%的患者需要进行剂量调整。Dacomitinib组在腹泻,甲沟炎,皮炎痤疮的发生率上,均显著高于吉非替尼组。因此,在这一次二代对比一代的较量上,因为显著的毒副作用,Dacomitinib在一线的应用仍需慎重。从Lux-Lung7和ARCHER 1050研究的生存曲线对比上,我们也看到阿法替尼和Dacomitinib是不同的二代TKI,PFS疗效存在差异,ARCHER 1050研究中,Daco在第5个月PFS曲线分开,显示获益趋势;而Lux-Lung 7研究中阿法替尼中位PFS仅提高0.1月(11m vs. 10.9m),PFS曲线在第12个月分开。未来,我们很快会看到FLAURA研究数据的结果。未来,我们很快会看到FLAURA研究数据的结果。对于EGFR突变型患者,哪一种治疗策略能取得最长的总生存呢?期待奥希替尼一线治疗的数据。
这个研究与Lux-Lung7的研究设计是相似的,但在入排标准中有一些细微差别,ARCHER 1050研究不允许CNS转移患者入组。在疗效对比上,Dacomitinib组的PFS获益明显(14.7m vs. 9.2m),但毒性值得关注,Dacomitinib组有高达66%的患者需要进行剂量调整。Dacomitinib组在腹泻,甲沟炎,皮炎痤疮的发生率上,均显著高于吉非替尼组。因此,在这一次二代对比一代的较量上,因为显著的毒副作用,Dacomitinib在一线的应用仍需慎重。从Lux-Lung7和ARCHER 1050研究的生存曲线对比上,我们也看到阿法替尼和Dacomitinib是不同的二代TKI,PFS疗效存在差异,ARCHER 1050研究中,Daco在第5个月PFS曲线分开,显示获益趋势;而Lux-Lung 7研究中阿法替尼中位PFS仅提高0.1月(11m vs. 10.9m),PFS曲线在第12个月分开。未来,我们很快会看到FLAURA研究数据的结果。未来,我们很快会看到FLAURA研究数据的结果。对于EGFR突变型患者,哪一种治疗策略能取得最长的总生存呢?期待奥希替尼一线治疗的数据。
(四)一代TKI re-challenge
来自宋勇教授的CTONG1304研究也在今年的ASCO会议上报道。研究的设计比较复杂。该研究定位的是三线治疗,在二线间隔化疗后,再行易瑞沙治疗的疗效。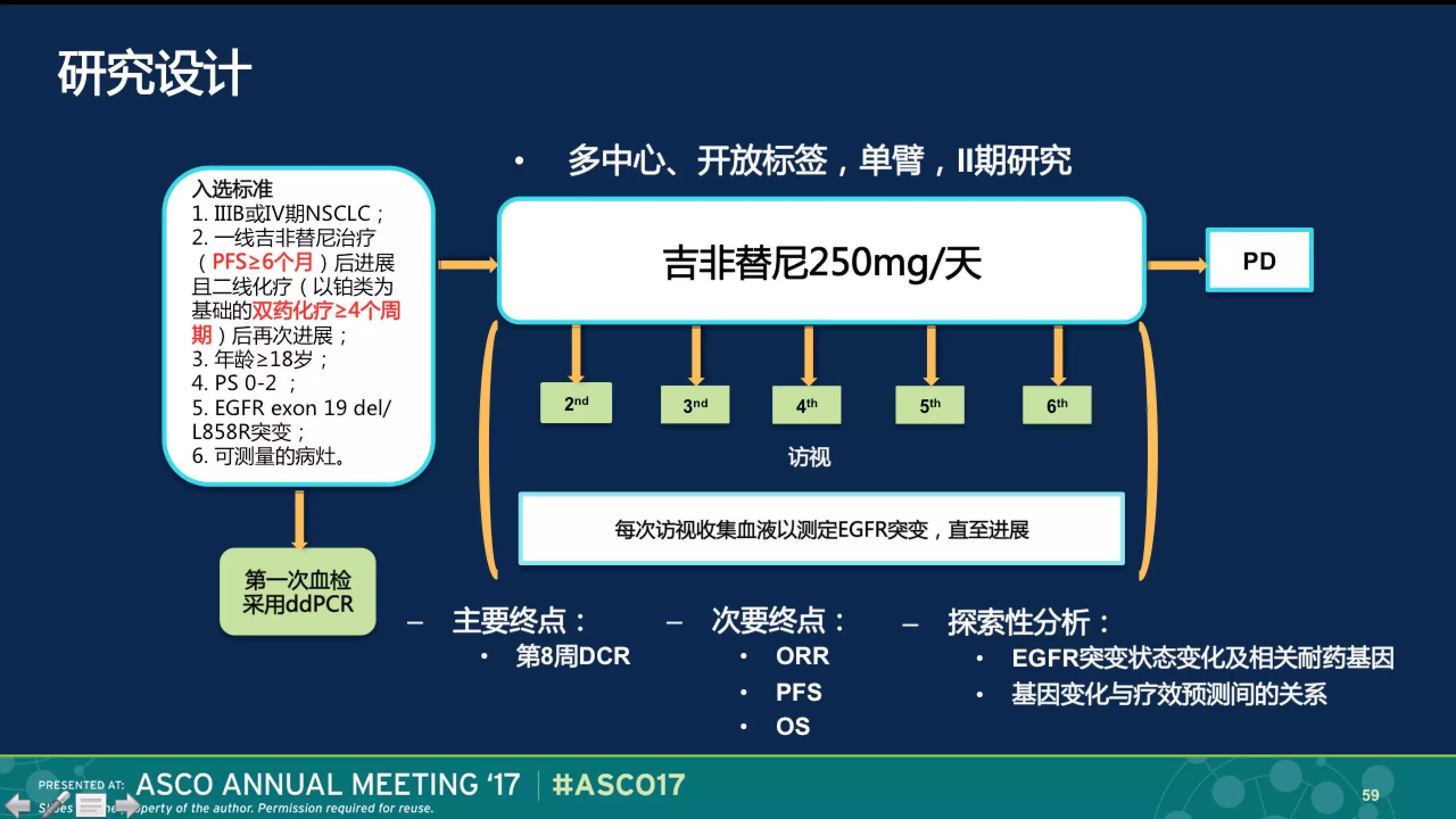
接受吉非替尼再挑战的患者,第8周的DCR为 69.8%,ORR 为4.7%。研究者看到一个非常有趣的现象,基线时T790M阴性亚组的DCR高于T790M阳性亚组(78.1% vs. 45.4%,p=0.0418);此外, T790M阴性患者从吉非替尼再挑战中取得的PFS和OS也优于T790M阳性患者。该研究提示,吉非替尼再挑战或可成为EGFR突变NSCLC三线治疗的一种有效治疗选择; T790M阴性患者更能从吉非替尼再挑战中获益。
2017年ASCO EGFR-TKI靶向治疗主要进展总结:
1.TKI用于辅助治疗:吉非替尼可作为已行切除术的N1/N2 EGFR阳性NSCLC患者的优选术后辅助治疗选择之一。
2.二代vs. 一代:Dacomitinib一线治疗EGFR M+患者PFS优于吉非替尼,但一线选择还需要考虑不良反应,价格等因素
3.奥希替尼CNS数据:奥希替尼具有很高的CNS活性,是脑转移患者的新希望。
4.一代TKI rechallenge:吉非替尼再挑战或可成为EGFR突变NSCLC三线治疗的一种有效治疗选择。
对EGFR突变型NSCLC的管理正在快速的改变着,越来越多的新药出现,如何通过全程管理,使患者获得最大获益,是我们需要努力的方向。
优化T790M耐药患者临床实践

范云教授
范教授主要从以下4个方面展开介绍:
(一)泰瑞沙克服EGFR-TKI耐药
EGFR突变是晚期NSCLC最重要的驱动基因之一,但非常遗憾的是,TKI获得性耐药总是不可避免,T790M突变是一代EGFR TKI最常见的获得性耐药机制,约占50%患者。在克服耐药的探索中,开发出了一系列的三代EGFR-TKI,然而,最终只有奥希替尼拔得头筹,获批上市,这与其独特的药理学特征是密切相关的。奥希替尼选择性针对EGFR敏感性突变(L858R和外显子19缺失)以及T790M突变,对野生型EGFR和IR/IGFR的亲和力很低。在AURA的系列研究,奥希替尼用于T790M突变的患者表现出高效、低毒、对脑转移有效的特征,成为T790M突变NSCLC患者治疗的“新高度、新标杆”。其中,AURA3研究深刻改变了临床实践,相比于化疗,奥希替尼显著延长PFS达5.7个月。基于AURA 17的研究数据,2017年3月,泰瑞沙获中国CFDA批准上市。目前,NCCN,ESMO和CSCO指南均作为I类证据,推荐泰瑞沙用于T790M阳性NSCLC患者。
(二)T790M检测标本与方法的选择
目前,国内外权威指南均强调,EGFR-TKI一旦耐药,应进行T790M突变检测。AURA的系列研究显示,血液与组织检测T790M对于奥希替尼具有相似的疗效预测作用。那么,组织检测优先还是血液检测优先成为关键问题。首先,我们查阅目前国际国内的权威指南推荐:2017NCCN非小细胞肺癌指南(V6版)再次强调TKI耐药患者应组织活检先行、血液检测补充;2017年CSCO肺癌临床指南,也推荐先行组织检测;2016 IASLC EGFR突变型晚期NSCLC管理共识中指出,TKI耐药患者,组织活检先行、血液检测补充;2015年NSCLC血液EGFR基因突变检测中国专家共识也推荐,对于TKI耐药患者,组织活检先行、血液检测补充。为什么上述指南和共识均推荐组织先行呢?这是因为,对于TKI耐药的患者,仅做血液检测是不足以判断T790M突变状态的,目前血浆检测的灵敏度相对较低。因此,对于EGFR TKI耐药的患者,应先采用组织检测;如果患者先进行了血浆检测,推荐采用灵敏度相对较高的数字PCR或NGS平台,对于血浆检测T790M阴性的患者,应该再行组织检测进行验证。
(三)泰瑞沙在脑转移患者中的疗效
奥西替尼对脑转移的病人同样有非常好的疗效,这与其药理学特征相关,既往研究显示,在EGFR突变型NSCLC脑转移模型中,泰瑞沙相比于其他EGFR-TKIs能更好的通过血脑屏障。其中有代表性的研究之一是BLOOM研究。在本次的ASCO会议上,报道了BLOOM研究中,奥希替尼用于脑膜转移患者的疗效,入组患者的T790M突变状态未知,结果显示,奥希替尼用于LM患者的ORR为43%,中位缓解持续时间为18.9月(5.6-19.3月,95% CI 11.1, NC)。此外, 10例患者基线时神经系统检查异常, 其中7例患者治疗后评估改善。
(四)再次耐药后该如何处理
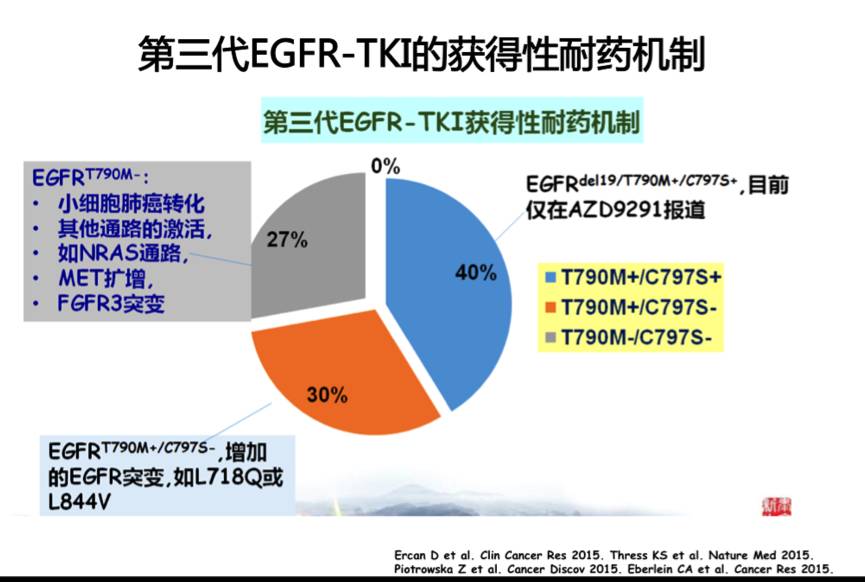
目前,第三代EGFR-TKI的获得性耐药机制总结如下,其中EGFR依赖的耐药机制主要包括:EGFR基因三重突变;EGFR扩增和T790M消失。EGFR非依赖的机制包括:旁路激活,SCLC转化。对于奥希替尼耐药后的患者,目前推荐的治疗模式如下,但很多方法在临床上仍然不可及。
 总结:
总结:
1.泰瑞沙克服T790M耐药,已成为T79M突变阳性患者的标准治疗方案。
2.T790M检测:推荐组织活检先行、血液检测补充(高敏感方法),不错过任何阳性患者。
3.泰瑞沙对伴脑转移、尤其是脑软膜的患者观察到疗效令人鼓舞的疗效。
4.三代TKI耐药机制复杂,需要充分整合临床耐药模式和耐药分子机制。
从发现EGFR突变至今已10年余,EGFR突变可以称之为“老靶点”,但我们关注到,这一老靶向不断演绎新故事,成为NSCLC精准治疗的典范。中国人群的EGFR突变率远高于西方人群,中国研究者对EGFR突变型NSCLC患者的治疗做出了很大贡献:IPASS,AURA3,ADJUVANT研究,体现了中国研究者的前瞻眼光和大智慧,使得精准医学从晚期肺癌走向早期患者。期待更多的中国研究唱响世界舞台
版权属肿瘤资讯所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:肿瘤资讯"













