新媒体管家
最近几年,颠覆性的研究结果不停刷新我们的认知:科学家们观察到DNA复制后发现根本就与原先所想的不同!居然有不需要引物的DNA聚合酶被发现!没有Y染色体也可以繁殖后代……。
小伙伴们纷纷表示这种颠覆力度,让人怎么读得进去教科书!

然而认知刷新是无上限的!
请执着于基因工程手艺【比如换个启动子、做个融合表达什么的】的小伙伴千万要抗住打击了:这些手艺在生物体内本来就有!而且切换自如!
新西兰梅西大学等单位的研究人员发现细菌可以通过两个基因的融合产生新特性的机制来适应环境变化!相关文章发表在近期的Nature Ecology & Evolution上。
基因是会产生各种变化的,比如:突变可以使生物体具有新的特征;重复基因和插入额外的DNA片段也可以增加有机体的适应性;转座子的发现刷新了人们对基因组状态的概念而获得诺贝尔奖。但是生物体内会出现象基因工程操作那样快速和彻底的变化在绝大多数人的意料之外。这项研究证明通过拼接、融合而创造出全新的基因,并不是人类首创的。我们所做的一切本来就在自然界存在。
1基因融合的蛛丝马迹

两个基因的融合,这么微观的现象是如何观察到的呢?这种可能性的蛛丝马迹是通过比较不同生物的基因组而获得的。这些引人注目的数据来自不同类型的生物体,包括细菌和多细胞生物。假定的蛋白质域交换后的产物还有一定的功能,比如果蝇中的新基因:sphinx(斯芬克斯,狮身人面——看这名字就知道是拼接的), jingwei(这是华裔青年发现的基因,从山海经里给它起了个名叫“精卫”,取精卫溺死而又重生之意——昭示着这个基因是“回炉重造”的)和Sdic。它们对求偶行为,乙醇脱氢酶底物特异性和精子活力有影响。这三个基因有可能来源于逆转录转座效应或者是临近基因的复制融合。
2用易突变的细菌做研究对象
生物信息学的数据分析提出了科学问题,但是如何找到实例来证实基因融合确实存在呢?进化通常都是很慢的,怎么样观察到这种实时的变化?因此,研究人员把重点放在细菌上,细菌的繁殖速度极快,而且可以在实验室里大量培养。这使得研究人员能够研究基因组中的结果变化,并观察到进行中的进化。
荧光假单胞菌P. fluorescens(SBW25)是研究环境适应的良好模式生物。因为它在不同的环境下快速进化,产生大量不同的突变;并体现了不同的菌落形态,很容易被观察到。

不同环境下的荧光假单胞菌
3发现两种基因融合的现象
原始的荧光假单胞菌菌落是光滑的,环境诱导突变体中表面有褶皱的菌落形态(WS)是由于调控双鸟苷酸环化酶(di-guanylate cyclases,DGC)的多种基因活性改变引起。研究人员通过16种改变环境调节的突破途径让DGC活化,增加cyclic-di-GMP的产量。cyclic-di-GMP是广泛存在于细菌中的第二信使,会促使纤维素产生和生物膜的形成,这样菌落就有了褶皱。
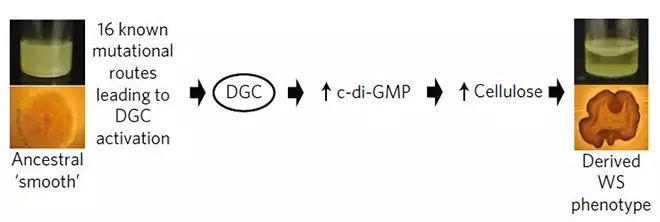
褶皱菌落(WS)突变原理
在这16种环境变化的褶皱菌落中,科学家们观察到了不同的基因融合现象。一种融合具有启动子捕获的特征,就是说两个基因融合后导致基因受到新启动子的控制,从而合成更多由融合基因编码的蛋白质。融合后,双鸟苷酸环化酶基因处在不同的启动子的控制下,从而增加了该酶的生产。
然而,在一些褶皱菌落中,该基因的活性没有变化。在这些细胞中的突变分析表明,这些突变中的双鸟苷酸环化酶基因和邻近基因形成融合基因。后者编码的蛋白质通常在细胞膜中活跃。这造成新的蛋白质具有膜结构域,并嵌入细胞膜中,激活了蛋白质,导致纤维素产量增加。
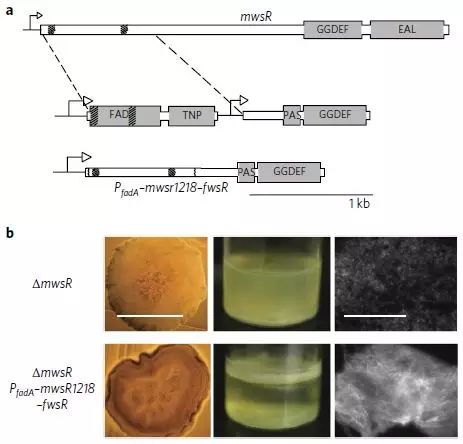
膜结构域和的双鸟苷酸环化酶基因融合形成褶皱菌落
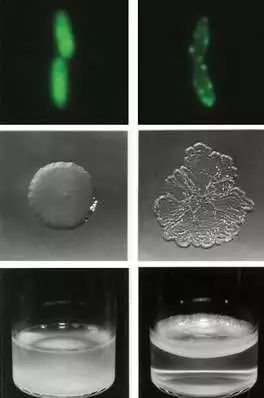
原始菌落(左)和膜定位融合褶皱菌落(右)
4通过融合产生新基因应该是个较普遍的机制
在细菌中找到了基因融合的鲜活例子可不止意味着该现象只有细菌中有哦!要知道生物信息分析处理的基因拼接现象有很多,比如在人体中的KUA-UEV基因,是KUA脂肪酸羟化酶基因和肿瘤易感基因UEV 通过可变剪接机制的融合。和所发现的假单胞菌基因融合改变蛋白在细胞内的位置一样,UEV定位核内,KUA在内膜上,而KUA-UEV在胞质中执行功能。人体中,64%的线粒体蛋白包含了在细胞其它地方起作用的基因蛋白。可见通过融合产生新基因的机制应该是一个比较普遍的现象。

参考资料:1)New gene evolution: little did we know
2)Evolving protein functional diversity in new genes of Drosophila
3)Adaptive radiation in a heterogeneous environment
4)Adaptive evolution by spontaneous domain fusion and protein relocalization
5)Experiments with bacteria show that genes can fuse together, leading to the production of novel proteins
本文系生物探索原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源生物探索。