▎药明
康德/报道
今日,罗氏(Roche)宣布美国FDA批准Hemlibra(emicizumab-kxwh)作为常规预防、防止或减少具有因子VIII抑制剂的A型血友病成人和儿童患者的出血事件。
在两项针对这类患者的关键临床试验中,Hemlibra可显著减少成人和儿童患者的出血。

A型血友病是一种严重的遗传病,患者的血液不能正常凝固,导致不受控的自发性出血。A型血友病影响全球大约32万人,其中50-60%的人具有该病的严重形式。
A型血友病患者缺乏一种叫做因子VIII的凝血蛋白。
在健康人中,当发生出血时,因子VIII会将因子IXa和因子X聚集在一起,这是凝血的关键步骤,可以帮助止血。根据病症的严重程度,A型血友病患者可能会经常出血,特别是在关节或肌肉中,引起疼痛、慢性肿胀、畸形、行动不便和长期关节损伤等严重健康问题。A型血友病的一个严重并发症是患者会发展出针对因子VIII替代治疗的抑制剂,它是由机体免疫系统发展而来的抗体,能够结合并阻断替代因子VIII,使它不能达到足以控制出血的水平。大多数A型血友病患者发展出因子VIII抑制剂后,会间歇性或预防性输注旁路制剂(BPA)疗法来控制出血。这一患者群体还有巨大的医疗需求未被满足。
Hemlibra是双特异性因子IXa和因子X定向抗体。它可以将激活天然凝血级联所需的蛋白质——因子IXa和因子X聚集在一起,恢复A型血友病患者的凝血过程。
Hemlibra是一种预防性治疗,可通过每周一次即用溶液皮下注射来进行。它有望为发展出因子VIII抑制剂的A型血友病患者提供新的治疗选择。
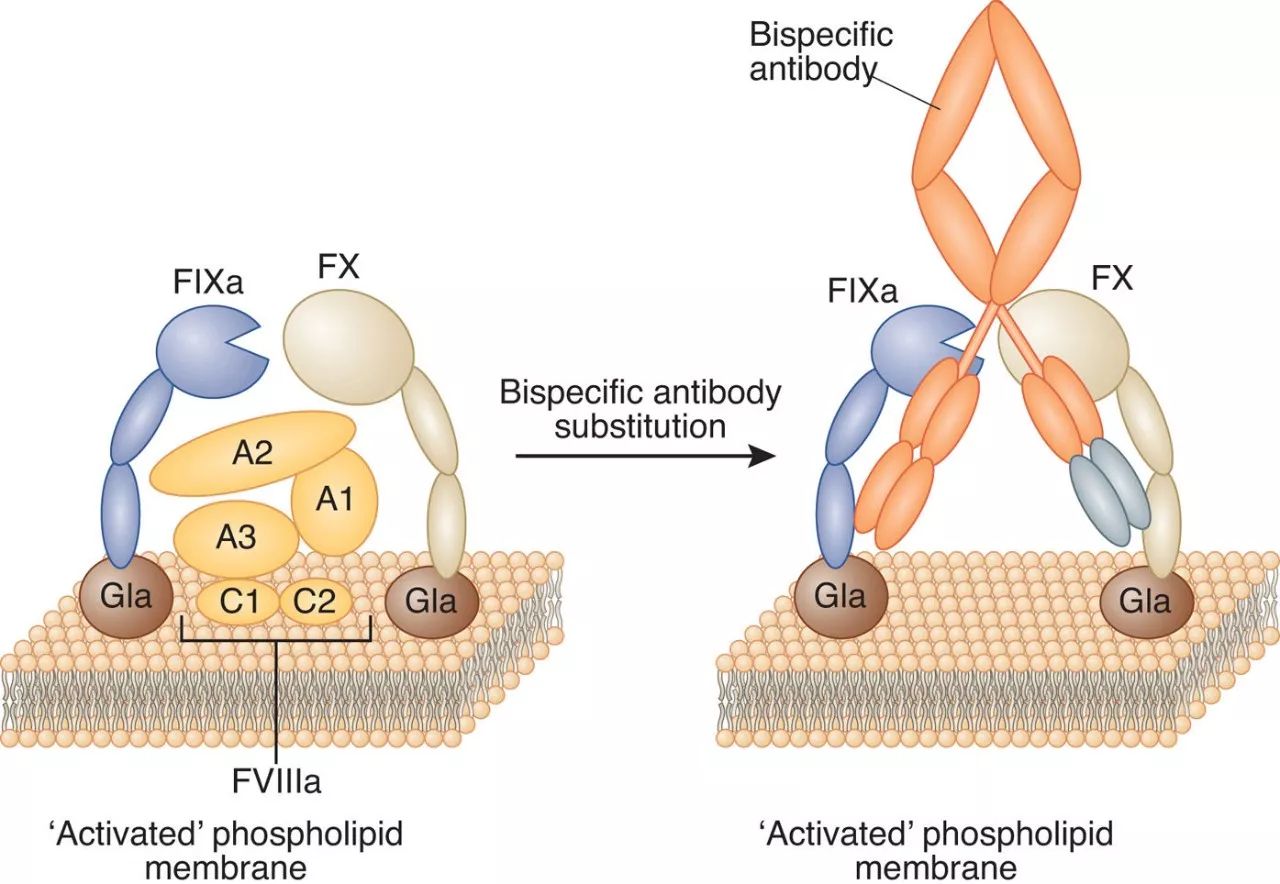
▲
双特异性因子IXa和因子X定向抗体的作用机理(图片来源:《自然》)
Hemlibra的效果在临床试验中得到了证实。在3期HAVEN 1研究中,
与没有接受预防治疗的患者相比,接受Hemlibra预防治疗的12岁以上A型血友病患者的出血率降低87%(95%CI: 72.3, 94.3, p <0.0001)。
在同类首个患者内分析中,与非介入性研究(NIS)中接受BPA 预防治疗的患者相比,接受Hemlibra预防治疗的患者的出血率降低79%(95%CI: 51.4, 91.1, P = 0.0003)。
HAVEN 2研究的中期结果显示,87%接受Hemlibra预防治疗的发展出因子VIII抑制剂的12岁以下A型血友病儿童患者未出现出血(95%CI: 66.4, 97.2)。
在13名参加过NIS的儿童患者的患者内分析中,Hemlibra预防治疗与BPA治疗相比降低出血率99%。使用Hemlibra治疗最常见的不良事件(AEs)是注射部位反应、头痛和关节痛。
“降低出血频率或预防出血事件是血友病患者疾病管理的重要组成部分。
今天的批准提供了一种新的预防性治疗方法
,已被证明可显著减少具有因子VIII抑制剂的A型血友病患者出血事件,”FDA药物评估与研究中心的血液学和肿瘤学产品办公室代理主任、FDA肿瘤卓越中心主任Richard Pazdur博士说:“此外,接受Hemlibra治疗的患者的生理功能也有所改善。”

“发展出
因子VIII
抑制剂的A型血友病患者面临预防出血的重大挑战,他们通常需要每周多次输注药物,这对于年幼的儿童及其家庭来说尤其困难,”南加州大学凯克医学院儿科教授、洛杉矶儿童医院止血和血栓项目主任Guy Young博士说:“这种新药已被证明与现有药物相比可减少出血的频率,而且每周只需注射一次。这会为这些孩子带来有意义的改变。”

















