虽然药品研发能力很强,但美国仍然是全球最大的仿制药市场,据IMS统计,2013年全球仿制药市场规模达1600亿美元中,美国就占到了500亿美元。中国现存的17万个药品批文绝大多数是仿制药,中国仿制药市场规模接近5000亿元。
一、通过仿制药降药费国际经验
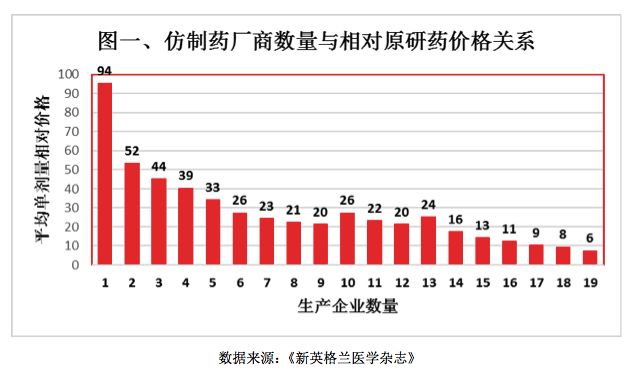
仿制药的价格将随着参与仿制药生产企业数量的增多而相应下降,当处于2-5家竞争时,价格迅速下滑到33%-52%,竞争厂家多了,则价格将降得更低。
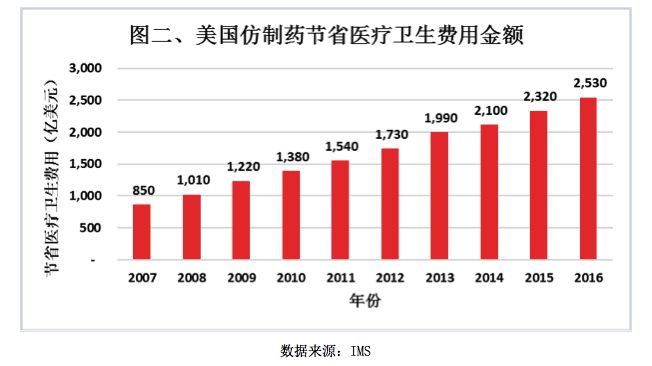
据IMS统计,过去10年,仿制药为美国医疗卫生体系共计节省了1.67万亿美元。
二、中国的仿制药因何没能降药费
1、质量差异
长期以来,我国的仿制药质量与原研药有着巨大的差距,也就不可能像国外仿制药那样来替代原研药,从而降低药费支出。以扶他林(双氯芬酸钠)为例,国产仿制药的生物利用度与原研药存在较大差异。
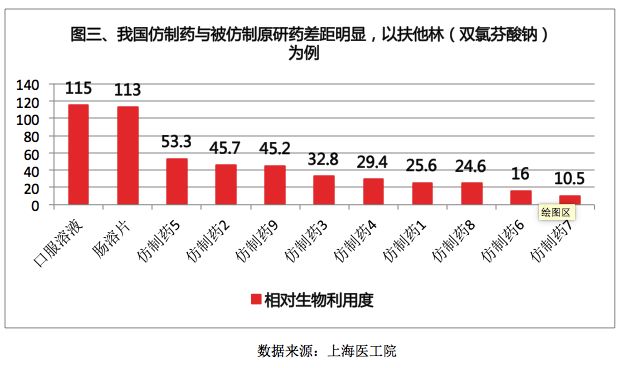
从图三可以看出,国产药与原研药生物利用度差异明显。
2、招标层次
招标时,国产药与原研药及过期专利药不能在同一质量层次,原研及过期专利药价格也就难以降低。

三、中国将如何通过仿制药降药费
发展仿制药的途径基本有两个,首先对存量批文进行一致性评价,同时加速仿制药的研发。
(一)一致性评价
1、已通过了一致性评价的品种
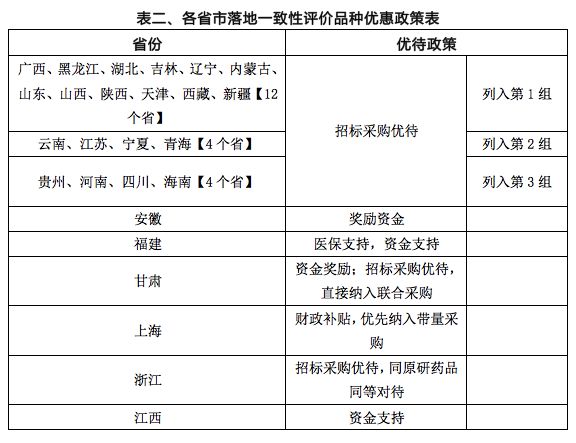
截至目前,已通过一致性评价的共15个品种(22个品规),其中289目录之外的品种达10个(17个品规),可见企业看到了一致性评价的市场潜力,主动加速了一致性评价的进程。国务院和CFDA在多个重磅文件中都提出对通过一致性评价的品种给予医保支付、招标采购、资金支持三个方面的优待,目前绝大多数省市也已出台了落地一致性评价优惠政策。
2、注射剂一致性评价
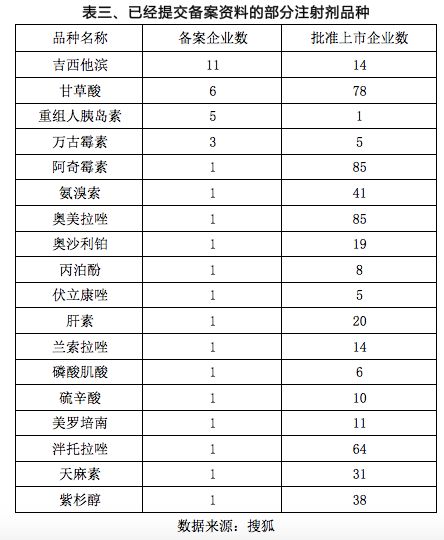
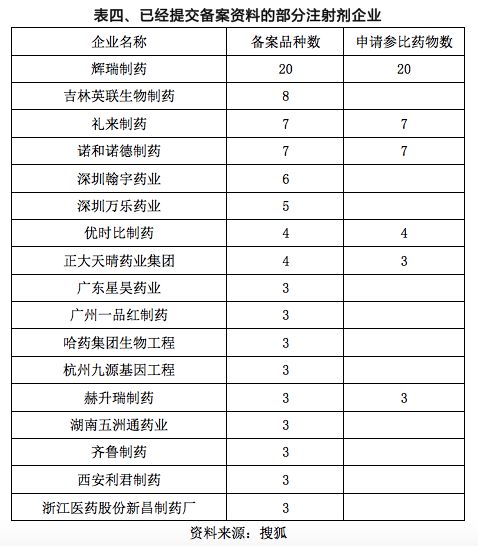
2017年12月22日,CDE发布了《已上市化学仿制药(注射剂)一致性评价技术要求(征求意见稿)》、2018年3月13日CDE又发布了《药物注射剂研发技术指导意见》,随将注射剂一致性评价提上了议事日程,和口服固体制剂相比,注射剂覆盖范围更广,涉及企业也更多。2016年我国注射剂用药规模达7577亿元,而临床使用的西药中注射剂超过了70%,其实,已有多家企业提前在做相关准备工作。截至2017年11月20日,拟进行一致性评价的注射剂品种有66个(表三),提出注射剂参比制剂备案的企业已有52家(表四)。
(二)仿制药
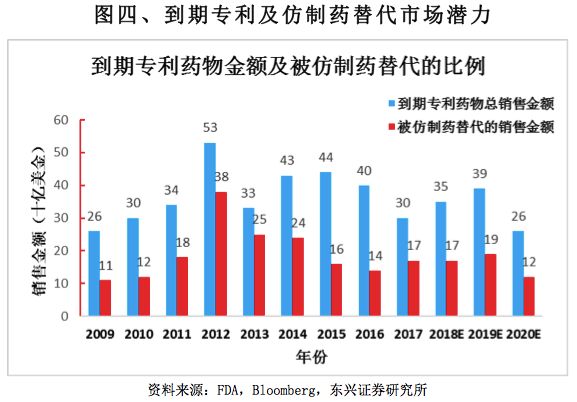
今后一段时间,将有多个药品专利到期,有巨大的市场空间供仿制药替代。
对尚未上市的在研仿制药而言,完善专利制度是关键,2017年10月8日中办国办发布的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(42号文),提出了完善专利制度的具体措施,具体包括建立上市药品目录集、探索建立药品专利链接制度、开展药品专利期限补偿制度试点、完善和落实药品试验数据保护制度等。
1、建立上市药品目录集
通过列出专利和独占信息,保护专利权人合法权益,降低专利侵权风险,从而促进仿制药研发的积极性。
2017年12月29日,首版《中国上市药品目录集》发布,共收录了131个品种,203个品种规格,其中包括通过仿制药质量和疗效一致性评价的13个品种(17个品规)。CFDA将对新批准上市的新注册分类药品以及通过仿制药质量和疗效一致性评价的药品直接纳入《中国上市药品目录集》,实时更新。
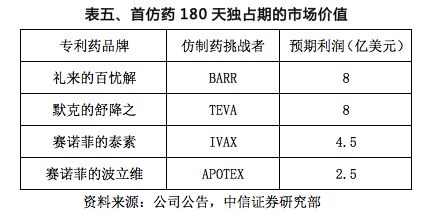
在美国,第一个向FDA递交ANDA、并含有PIV声明的仿制药,如果专利挑战成功,则FDA将给予180天的市场独占期。在这180天内,FDA不再批准其他的ANDA持有人上市,独占期期间,该仿制药将迅速抢占市场,并获取高额利润。