▍来源:赛柏蓝 作者:郑瑶
近日,辽宁省卫计委药品器械处,对于省内短缺药品发起了新一轮的大调查。
共有33种药品在列,如茶碱缓释片、硫酸阿托品注射液、硝酸异山梨酯片等。
在33种药品中,有不少来自于国内的知名药企,如广州白云山光华制药股份有限公司、中美上海施贵宝制药有限公司、国药集团容生制药有限公司、江苏恒瑞医药股份有限公司、哈药集团制药总厂等。

其中比较引人注意的是,由上海禾丰制药有限公司生产的重酒石酸间羟胺注射液,共有多达8家医疗机构上报出现短缺情况。
此外,赛柏蓝经过查询发现,自今年7月份以来, 辽宁省卫计委已经对短缺药开展了多轮调查,看来辽宁省在对付短缺药方面是“火力全开”。
附:关于对9月份医疗机构上报药品短缺原因进行调查的通知
各有关药品生产、配送企业:
依据辽宁省短缺药品监测预警和供应保障系统数据,9月份省内各医疗卫生机构上报的短缺药品信息经各市卫生计生委初步核查后,共33种药品需进一步调查。
请各有关药品生产和配送企业对信息表内对应药品的供应情况进行说明,并填写“药品供应情况说明”(附件2),于10月24日17:00点前发送电子邮件至指定邮箱。
联系人:周海霞 联系电话:024-23371079
电子邮箱:[email protected]
附:2017年9月份辽宁省医疗机构上报短缺药品汇总表
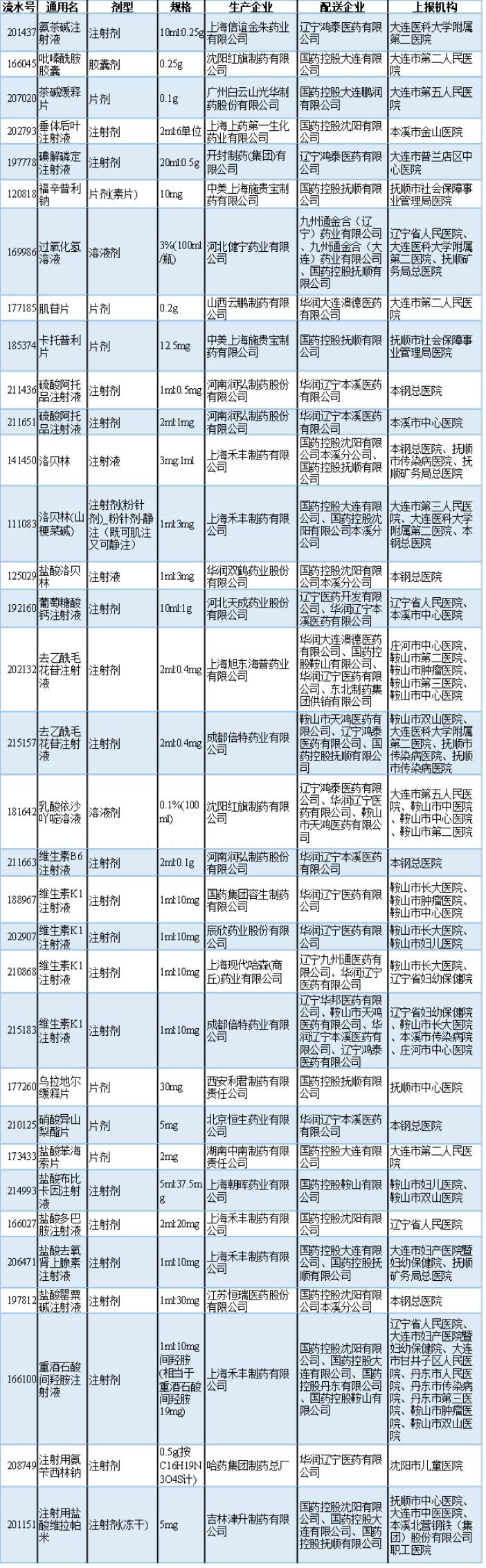
(图表制作:赛柏蓝)
▍赛柏蓝推荐
营改增无票可找、无处找票,票据处理怎么办?佣金如何提现?10月26-27日,上海,药企营销财税策略与CSO风险防控,帮助企业完美布局CSO合规落地,保留业务证据链,从执法者角度应对税务稽查。详情咨询:400-1000-198。

十九大召开前夕(10月8日),中共中央办公厅、国务院办公厅联合发布《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》。第十一条规定:严格药品注射剂审评审批。严格控制口服制剂改注射制剂,口服制剂能够满足临床需求的,不批准注射制剂上市。严格控制肌肉注射制剂改静脉注射制剂,肌肉注射制剂能够满足临床需求的,不批准静脉注射制剂上市。大容量注射剂、小容量注射剂、注射用无菌粉针之间互改剂型的申请,无明显临床优势的不予批准。第二十五条规定:开展药品注射剂再评价。根据药品科学进步情况,对已上市药品注射剂进行再评价,力争用5至10年左右时间基本完成。上市许可持有人须将批准上市时的研究情况、上市后持续研究情况等进行综合分析,开展产品成份、作用机理和临床疗效研究,评估其安全性、有效性和质量可控性。通过再评价的,享受仿制药质量和疗效一致性评价的相关鼓励政策。医药行业格局或将巨变?
众多中药注射剂品种无亮点、无精准定位、无新增适应人群、无高端文章、无专家共识、无大数据等,如何通过临床再评价实现品种价值描述、获得市场通行证?如何通过完善符合产品特点的评价标准、精准定位优势病种、明确临床优效诊疗方案、凸显临床价值?
十九大即将召开,将怎样改变中国,亦将怎样改变医药行业?企业如何紧跟国家发展的时和势,作出全局性的谋划部署?11月27-28日中国医药企业管理协会将在广州召开“第三十二届中国医药产业发展高峰论坛”。
拟邀嘉宾:协会将邀请国家食品药品监督管理总局、国家中医药局相关领导、国内中医药院士等专家,在中药注射剂高度监管的情势下,医药企业中药注射剂如何通过上市后安全性再评价实现产品价值、扩大市场份额?
电话:400-1000-198

赛柏蓝-医药移动新媒体传播首选平台!
微信新媒体矩阵:赛柏蓝、赛柏蓝器械、三甲传真、基层医师公社、药店经理人,帮助药械企业树品牌、建渠道、拓网络、找客户!

长按二维码>>识别图中二维码>>添加好友
在线咨询产品高效招商
(2017年10月-12月黄金版位征订中)
详询13810136605















