▍
来源:网络综合 整理:赛柏蓝
在21日爆出的中国作者107篇论文因学术造假被国际期刊撤下事件中,125家全国著名医院被牵涉其中,数据和研究造假再次刺痛医药行业
▍
107篇文章造假
当地时间20日,世界著名学术出版机构施普林格自然出版集团发布声明,撤销《肿瘤生物学》(Tumor Biology)期刊所刊登的107篇论文——此次被撤稿论文的作者全部来自中国,撤稿原因为论文作者编造审稿人和同行评审意见。
此次震惊全球的撤稿事件也成为了正规学术期刊单次撤稿数量最多的一次,复旦大学附属华山医院、中国医学科学院北京协和医院等127家全国著名医院被牵涉其中,数据和研究造假再次刺痛医药行业。
根据21日中国科学技术协会发布的信息显示,关于此次撤稿事件,早在4月18日,中国科协就在北京与施普林格自然出版集团大中华区总裁安诺杰等人进行了沟通。对于此次撤稿事件,安诺杰表示,这只是2015年撤稿事件的延续。
2015年8月,施普林格自然出版集团曾撤回旗下10个学术期刊已发表的64篇中国作者的论文——这些论文因学术造假被撤。
“调查发现,‘第三方’投稿时推荐的评审人,有些姓名、职务和工作单位是真的,而联系所用的邮箱全都是‘第三方’所注册的。”黄伯云当时曾表示,如此一来,待评审的论文实际上返回到“第三方”手里,投稿者冒充评审人评审自己的论文,让自己的论文获得录用。
根据安诺杰的介绍,最新发生的这107篇撤稿事件是《肿瘤生物学》杂志利用2015年撤稿事件掌握的虚假同行评审信息反查了2012年—2016年发表的所有论文,从而发现这批伪造同行评审的论文。因此,此次撤稿事件实际上与2015年所撤稿件的情况相同,只是此前施普林格自然出版集团并未查出这些虚假论文。
这两起撤稿事件的确暴露了一些科研人员违反学术道德的造假行为,揭露了论文代发的“第三方”灰色产业链,同时也折射出这些撤稿期刊同行评审制度不够严谨的问题。
▍
造假产业链
近年来,不断有媒体报道显示,中国学术界论文造假事件近年呈高发态势,而这背后早已形成一条庞大的产业链。
2016年7月,央视报道的论文造假中,全国500多所高校被牵涉其中。
央视记者调查发现,很多期刊出版公司在论文造假一项业务中,每天的接单量能创造十几万的纯利润——公司里每个业务员基本上都加了三四百个研究生群,500多业务员几乎渗透进了我国大多数高校的研究生群。
(图片来自:央视)
( 图片来自:央视)
2015年3月中旬开始,英国现代生物出版集团撤回了43篇
SCI
(美国《科学引文索引》的英文简称)医学论文,其中41篇来自中国,这些论文被撤回的理由是“相关文章的学术真实性无法得到保证”。同时,这批被撤回的41篇SCI论文有一个共同的特点,就是全部由第三方机构为文章联系同行评审,并代为投稿。
根据媒体调查显示,在这个灰色产业链当中,2000是起步价,发SCI(科学引文索引(Science CitationIndex))论文15万起价,几乎相当于一个副教授1年的工资。
▍
临床机构背后的药企实验
而特别值得注意的是,
在此次被撤稿的107篇文章背后,是125家医院与研究机构,尽管此次并不是严格意义上的数据造假,但科学论文造假本身,已经使这些医院和机构所作出的实验也蒙上了阴影。
临床试验是新药研发最重要的环节;但长期以来数据造假却屡禁不止。
对此,最高法院近日通过《关于办理药品、医疗器械注册申请数据造假刑事案件适用法律若干问题的解释》,首次将临床数据造假骗取药品批文纳入刑事处罚,这意味着“造假者或将面临最高死刑的刑罚”。
2015年7月,国家启动药物临床试验数据自查核查工作,对待批生产的1622个药物临床试验项目数据真实性、规范性进行核查,并分3批派出20个检查组开展现场核查。截至2016年1月12日,撤回和不通过合计1151个,占自查核查总数的80%,其中企业主动撤回占到77%,剩余待核查项目273个。
以每家药企平均投入300万研发费用算,撤回1151个,则涉及费用34.53亿元。而最新的《药品、医疗器械产品注册收费标准》显示,国产新药注册费标准从原来的3.5万上涨到62.4万元;进口药从4.5万上涨到96.9万元。在此次撤回的新药注册中,以国产为主,若以平均的62.4万计算,撤回和不通过1151个的新药若重新申报则涉及7.18亿元。
附:
此次被《肿瘤生物学》撤稿的研究机构清单
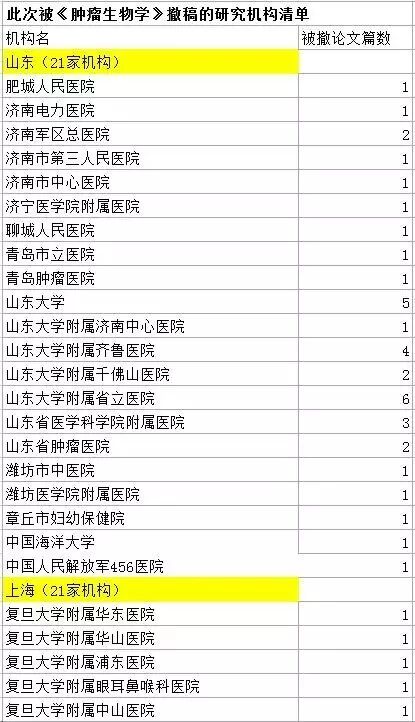
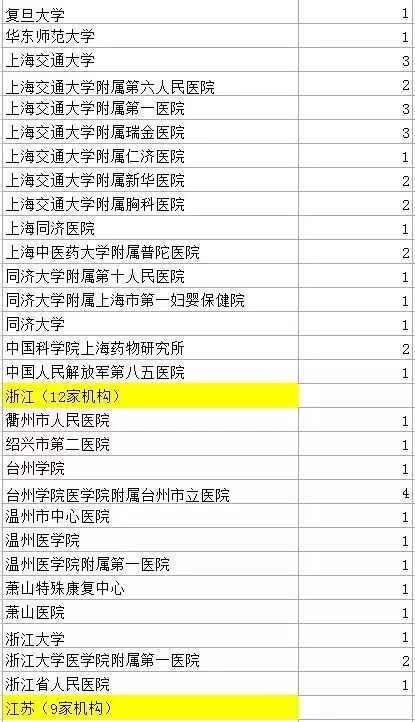
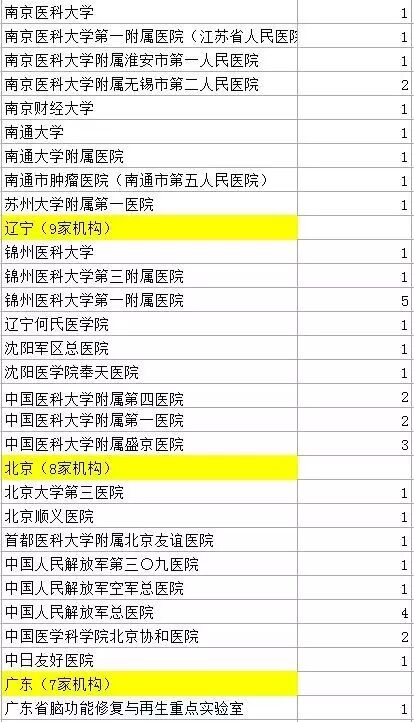
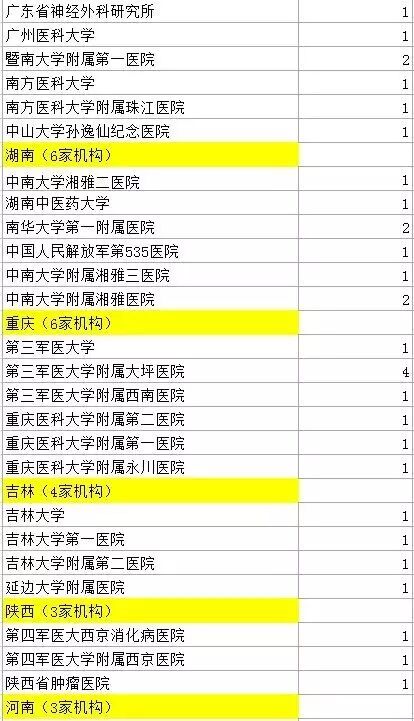
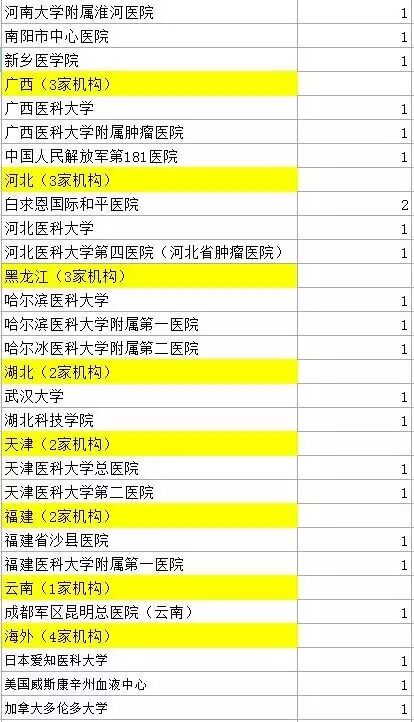
(图片来源:澎湃新闻)
本文为整理,转载请注明来源和作者。投稿、线索等请添加微信saibailan;信息发布:13810647732(柏青),会议合作:13810604246(王谢堂燕)
CSO公司注册地、注册资金、投资人、企业类型、发票数量及开票金额、开票频率等如何合规设计?CSO经营范围如何设计?CSO公司经营范围、发票内容与药企合作如何合规设计?
赛柏蓝















