根据咸达数据,本周(2017.11.6-11.12)灵北制药氢溴酸伏硫西汀片以及豪森药业注射用硼替佐米的上市申请审评完毕;厦门恩成申报1个2.2类新药SOCC-2胶囊;嘉和生物的杰瑞单抗注射液首次登记I期临床;此外,新增2个申报一致性评价的品种。
| 看点一
灵北制药重磅抗抑郁药氢溴酸伏硫西汀片的进口上市申请(5.1类)已审评完毕,处于审批阶段,如无意外即将进口中国。本品2016年12在中国递交上市申请,并纳入第十四批优先审评程序的药品中。氢溴酸伏硫西汀片共4个规格:5mg、10mg、15mg、20mg,均在国内递交上市。
本品英文名Vortioxetine,曾译沃替西汀,于2013年9月获得FDA批准,用于治疗成人重度抑郁症(MDD),同年12月获EMA批准在欧洲上市。本品可抑制五羟色胺再摄取,具有5-HT1A受体激动剂、5-HT1B受体部分激动剂及5-HT3’、5-HT1D及5-HT7受体拮抗剂的作用。伏硫西汀作用的多样性使其在几个系统中的神经传递产生调节作用,主要调节五羟色胺,推测也可调节去甲肾上腺素、多巴胺、组胺、乙酰胆碱、GABA及谷氨酸盐系统。伏硫西汀是第一个具备如此多种药效活性的抗抑郁药物。
根据信狐药讯全球销售额,本品2016年的销售额为428M美金。从2014年广泛投入市场到现在,销售额稳步增长。
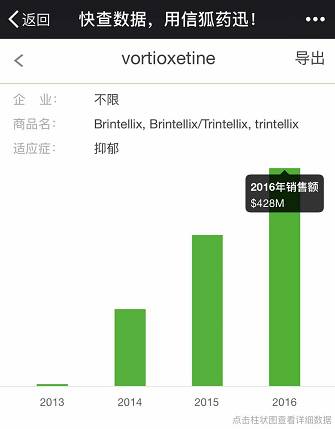
根据咸达数据,目前本品在国内有超过10家企业获得临床批件,还未有国内企业登记本品试验,估计是等着原研上市后做BE试验,不过本品化合物专利2022年10月在国内到期,仿制上市还续等待~
| 看点二
江苏豪森抗肿瘤药注射用硼替佐米的仿制药上市申请三合一审评已完成,处于审批阶段,本品在首批优先审评专利到期品种名单中,如无意外,估计会首仿上市。后续本品排队待审评的企业还有江苏正大天晴、齐鲁制药,南京先声东元,亿腾药业等。
本品由杨森制药持证,于2005年获准进口我国,商品名万珂,目前在我国批准的适应症为:用于多发性骨髓瘤、复发或难治性套细胞淋巴瘤患者的治疗。
| 看点三
厦门恩成制药2.2类新药SOCC-2胶囊的临床申请进入审评中心,2.2类化药为含有已知活性成份的新剂型(包括新的给药系统)、新处方工艺、新给药途径,且具有明显临床优势的制剂。目前未查到本品的活性成分为何物。
| 看点四
嘉和生物的杰瑞单抗注射液(GB224)首次登记I期临床,登记号CTR20170263,拟适应症类风湿性关节炎。试验主要目的:1.评价GB224的安全性和耐受性;2.评价GB224的药代动力学特征。次要目的:1.初步了解GB224的免疫原性;2.初步了解GB224的药效学指标(IL-6)。试验于2017年7月通过北京大学人民医院医学伦理委员会的审查,计划入组58例健康受试者。
本品是嘉和生物申报临床研究的第6个单抗药物,也是第一个创新型治疗用生物制品1类新药,于2016年1月申报临床,2016年12月获批临床,受理号CXSL1500110。本品以白介素-6(IL-6)为靶点,为TNF靶点单抗(类克和修美乐均属于这一类单抗)的下一代产品。
| 看点五
本周新增2个申报一致性评价的品种:
江苏豪森的甲磺酸伊马替尼片和扬子江药业的苯磺酸氨氯地平片,都是大品种啊。
作者| 横颜
编辑| 米琥
❶ 点击订阅号底部菜单,顺手获取更多药品信息
❷咨询或试用数据库,联系QQ 97361509
❸ 长按右侧二维码,关注咸达















