谢老师就职于上海市食品药品检验所,是国内溶出度试验的
“
开拓者和领航员
”
。同时,又是国内率先站出来旗帜鲜明反对
“
抠杂质
”
的体制内人士。此番撰稿,谢老师更是一针见血地指出:那些追求完美、专业妄想出来的杂质都是
“
纸老虎
”
的观点,真是让人意想不到、陡增钦佩。来,让我们一窥究竟
……
严抠杂质背景
据本人所知:
2006~2007
年发生数起较为严重的药害事件后,国家层面专家在总结研讨其根源时一致认为是
“
杂质所为
”
,并同时上升至
“
药物不良反应与杂质息息相关
”
的专业认知。于是,自
2007
年下半年起,整个行业拉开了研究杂质的
大幕
,具体表现为:
1
)国家药品审评中心
(CDE)
作为药物研发的
“
指挥官
”
,要求企业在杂质研究上,一定要穷追不舍、竭尽所能,切勿漏检。
2
)
中检院获得国家科技部专项资金,确立并开展各类杂质研究。
3
)
药典会效仿《欧美药典》,将越来越多的杂质订入药典。
这也是国家局常以
2007
年
10
月为界,作为审评门槛提高、仿制药质量提升的依据所在。随着官方要求的不断加码,全行业掀起杂质研究热潮,并逐渐呈现出上天入地、走火入魔之景象,颇有当年
“
大炼钢铁
”
之态势。
本人并不反对研究杂质,但若研究过度或控制过猛,就会误入歧途、达到
“
抠
”
之境界了。
所谓控制过猛,系指
“
杂质含量越小、质量越好、不良反应越少
”
的谬论。为此,借助蒲公英微信公众号,本人在
2016
年
10
月
10
日发表了
“
【这个可以有!】仿制药杂质含量比原研药多、只要在限度内
”
一文,旨在呼吁众人切莫落入
“
唯低是取
”
的窠臼中。文章推送后,收到多位同仁来电来函,畅谈积压在心中多年的苦闷与专业上的彷徨。
所谓研究过度,系指怀揣追求完美之理想,把
“
做技术变成了做艺术
”
,为避免漏检杂质而展开一网打尽、滴水不漏的研究工作。本文将针对该点进行阐述,以辩证思维和严谨试验劝慰众人根本无需如此疑神疑鬼、谨小慎微,因为那些凭空想象出来的杂质几乎都是
“
纸老虎
”
。

一、《
ICH Q6
指导原则》给出的杂质研究思路
——“
以终为始
”
采用一适当的色谱条件检测规模化生产的
3
批样品,以检出的杂质作为研究的开始,未检出的杂质无需研究。诠释如下:
1. “
适当的色谱条件
”
系指能分离检测出研究者认为最有可能存在于终产品中数个杂质的色谱条件(如起始物和各步反应中间体杂质,因为这些杂质最易残留于终产品中)。
2. “
规模化生产
”
代表工艺稳定,杂质谱在未来样品中将较为固定,质控也具有目的性和持续性。
3. “
检出
”
系指采用笼统法(液相归一化法或主成分自身对照法)检测,结果超出
ICH
原料药鉴定限
0.10%
的杂质。如某杂质检测结果为
0.08%
,则无需研究,也无需改为准确法检测(杂质对照品外标法和主成分自身对照
+
校正因子法),仅报告便是。
4.
所谓研究,系指需知晓结构式,并酌情考虑下一步研究的深度与程度。
以上研究思路针对性强,事半功倍、多快好省。

二、
CDE
给出的杂质研究思路
——“
以源为始
”
自2007年后,CDE对杂质研究的要求陡然升级,具体表现为:杂质与药物不良反应息息相关(在下认为基本无关,呵呵~~),故为保证临床安全性,一定要将所有可能存在于终产品中的杂质研究透彻;而ICH的“适当色谱条件”很有可能存在检出能力有限、杂质漏检的情况发生。
为了不漏检,CDE“开创性”地将ICH仅用于制剂研发、生产和质控的QbD理念应用于了原料药上,于是将以终为始的研究思路改为了“以源为始”,即从源头——合成起始物中含有的杂质作为研究的开始(本人简称“公元前杂质”)。该要求颇有刨根问底、铲草除根之意味;此举引发对起始物出售方化工厂的询问,使该领域朋友一头雾水。随后以“自我合成专业之能事”,构思出一路走来、走到终产品的征程中有可能产生的所有杂质
。
在此导向下,整个行业形成了“以杂质论英雄”的专业认知,各企业间展开“杂质军备竞赛”——纷纷以杂质研究数量的多少作为衡量研发能力强弱的指标,以样品中杂质含量的多寡作为评价药品质量优劣的标准,这些理念的贯彻实施使得合成人员既成为受害者、又成为受益者;同时使得分析人员束手束脚、几乎成为“半精神病”(做液相时不知是基线抖还是杂质抖;索性怀疑成杂质,然后让合成人员继续研究……);而该时期制剂人员颇有些无所事事、百无聊赖,盖因生物等效性(BE)试验没有失败的潜规则所致。
CDE自2012年起在官网上和全国性的多次公开培训强调以上思路,尤以那篇著名的“仿制药研发中的几个关键问题”文章达到了此项要求的顶峰(CDE网站2014-07-15发布;其实全文仅阐述了1个问题——就是将杂质研究进行到底),文中有这样一段论述:
3.1
杂质研究与控制的基本思路
杂质谱分析的思路与策略实际上是QbD理念在杂质研究中的具体实践。杂质谱被认为包括药物中各种潜在杂质的种类、来源、含量、结构及活性等的信息总和。
杂质谱概念的引入进一步厘清了药品杂质研究与控制的基本思路,由传统的“以终为始”的被动思维上升到“以源为始”的主动控制模式,即不是仅仅局限于从得到的分析结果-色谱图开始分析产品杂质情况,而是从杂质来源的分析入手,结合产品的实际生产工艺、结构特点等分析可能存在于产品中的中间体、副产物、降解物、反应物料等各种潜在杂质,通过杂质谱分析全面掌握产品的杂质概貌,根据各类潜在杂质的风险级别,有针对性地建立合适的分析方法,以确保各种潜在杂质的有效检出和确认;跟踪杂质谱对安全性试验或临床试验结果产生的影响,并结合相关指导原则、文献信息等评估杂质的可接受水平,确立上市产品的杂质控制限度。
同时,通过杂质谱分析明确可能的杂质来源和去向,在制备工艺设置相应杂质的针对性控制措施,并通过产品包装和贮藏条件的研究,有效抑制药品的降解,实现从杂质产生的源头主动性地把控药品杂质。
很多企业遵照CDE要求,用所有文献查询结果和自我“专业妄想出来(可能的、潜在的、副反应产生的,甚至火花碰撞的,还有……)”的大量杂质推翻了既有文献的色谱条件,随后费劲费力地建立起一套崭新的色谱系统,再去国外购买来价格比黄金还昂贵的杂质对照品或自我合成杂质对照品(比合成主成分难多了,故这些年发表了大量合成杂质的文章)开展《全套分析方法学验证》(对对照品纯度和数量均有一定要求),最后测定规模化生产的三批样品,结果呢?
绝大多数均是未检出(
ICH
原料药报告限
0.05%
以下);即便检出,也不会超过
ICH
原料药鉴定限(
0.10%
);再多也不会超过
ICH
制剂鉴定限(通常为
0.2%~0.5%
),而这些限度以下的杂质在临床上不会产生任何安全性问题,且无论何种给药途径!
但为了证明这些几乎不存在的杂质,全行业兴起一场既是“信徒式”、又是“走形式”的浪潮;同时,对起始物和各中间体的质量控制还制订了类似于主成分的质量标准!不夸张地说,过去10年、全行业至少几十亿资金灰飞烟灭、化为乌有,就是为了换取来早已耳熟能详的那三个字“未检出”。

很多同仁之所以推崇
“
以源为始
”
,就是担心采用
ICH
思路会导致杂质漏检。为此,本人通过总结大量案例,归纳出如何验证不漏检的方法,与众人分享:
首先需建立
“
任何分析方法都不是万能的以及完美的科学就是伪科学
”
的辩证思维,这也属于哲学范畴、宏观高度。
其次,要建立起
“
即便漏检,只要该杂质含量不大于制剂鉴定限,在临床上就不会有任何安全性问题
”
的专业认知。
ICH
制剂鉴定限
为:
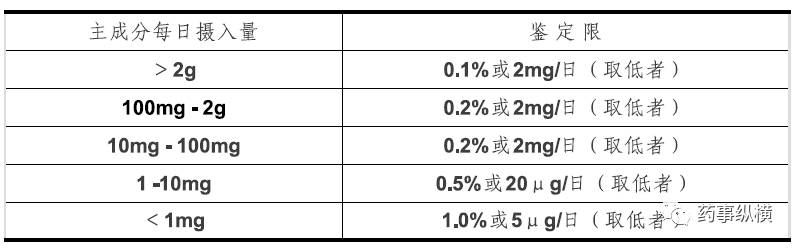
即以通常的主成分每日摄入量
1mg-2g
计,只要笼统法检测结果不大于
0.2%-0.5%
的杂质就不会给临床带来任何安全性问题!即便有数个杂质漏检亦可熟视无睹,但此时主成分含量必然偏低,发生此情况时再去探究原因亦不迟。
如有超过制剂鉴定限的杂质漏检,可采用如下方法予以验证:
1.
采用
DAD
检测器检测主成分峰纯度,验证其中是否包含杂质。此时需注意:积分时应将默认的
190nm-800nm
改为
230nm-400nm
,因末端吸收会干扰纯度检测与判断。
【注】无需验证杂质峰中是否包含杂质,因即便包含,检测结果是对自身的严格要求,故可以。这也再次启迪我们、分析方法无需追求完美。
2.
对于保留时间过长,但仍可被检出的杂质,由于目前均为自动进样装置,自然会在随后的样品中呈现出来,发现后再厘清亦不迟。
3.
对于在所设波长下检测不到的杂质,可通过两种检测法测定
API
主成分含量、观测结果是否殊途同归予以探明。如分别采用液相归一化法和容量分析法(指示剂法或电位滴定法)测定,两者差值不超过
0.3%
,便可证明未包含有含量大于制剂鉴定限的杂质,如此便可高枕无忧。
4.
通过观测稳定性考核
6
个月试验结果(加速试验和长期试验),主成分含量下降量与总杂质增加量间是否具备相辅相成性来判断。如不具备,说明所建立的测定法检测不出主成分降解产生的杂质、属于原则性错误,必须做出调整。
现实工作中,发生以上
4
种情形的案例并不多,概因我国合成高手实在太多,盖因制剂鉴定限的要求其实非常宽松。所以,恳请众人,勿再草木皆兵、杯弓蛇影啦!
至于那些担心漏检的、含量低于制剂鉴定限的杂质恐为基因毒性杂质的同仁,纯属自我恫吓,建议去看一下心理医生(切勿生气哦)。

看到全行业在过去
10
年,陷入
“
自我陶醉、甚至自鸣得意
”
的杂质研究泥潭,在下深感忧虑与焦急。撰写此文,绝非是想哗众取宠或特立独行,而是本人曾赴日本国家药检所进修学习,深谙发达国家在审评药物时的关注点与核心竞争力(绝非限于全世界都公开的指导原则),从而具备了独立观察与冷静思考。
诚挚寄望行业能早日驱散杂质研究“雾霾”,及时调整和停止在杂质研究上的无功而返与劳民伤财,尽快将有限资源用于药品有效性研究上,因现阶段我国仿制药的不足几乎都在有效性上,绝非是杂质引起的安全性上;即便是安全性,那也是因我国制剂拙劣、导致主成分副作用的显现!
【声明】
本文仅代表个人观点,不代表所在单位。文中如有不当之处,敬请相关人士海涵。同时,所述内容属于专业认知、见仁见智范畴,还请异议者切勿上纲上线,在此先作揖叩谢了!

本文来源蒲公英,内容仅代表作者观点,不代表本刊观点,如有版权问题请联系小编。
药事纵横网站已经开通,欢迎大家光临。我们的网站地址是:www.pharmaguider.cn 与我们公众号的微信号码相同。

药事纵横是一个开放,由自愿者组成的团体,现有成员14名,分别为Voyager88,雷诺岛,三分话,Herman,Mzwinsunny,文竹,duke,巉巉之石,蓝色枫叶,ISAL,海角边,冯姝婷,yhqqqqq,陈小牛,欢迎有志之士加入我们团队。投稿、加专业微信群【合成、制剂、分析、注册、BD、一致性评价】请加微信442015666,QQ群:22711855/22711679(限加一个)





