从理论上讲,BCS2类药是体内体外相关性最好的一类,然而事实却证明,BCS2类药物BE一次通过率是最低的,
为什么呢?原因在于,我们建立的溶出方法并不能真正地反映药物在体内的崩解、溶出过程,对于pH值依赖型药物,这一现象尤为突出。为此,药事纵横翻译组特翻译了
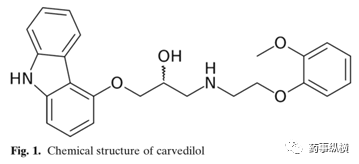
pH 值依赖性弱碱性 BCS II类药物卡维地洛的溶解度和体外溶出行为研究
一
文,抛砖引玉,望各位同仁取其精华,在一致性评价中少走弯路。
低溶解性、高渗透性药物,即生物药剂学分类系统(BCS)II类药物的溶出是口服吸收的限速步骤
(1-3)
。
弱酸性BCS II类药物卡维地洛(结构式见图1)在从胃液到肠液转运过程中,在不同pH值部位会表现出复杂的溶解度
,如在胃部(较低pH值)有利于其解离和完全溶解
(4)
,而到达肠液(较高pH)后,由于其较低的溶解度可能会产生沉淀
(4,5)
。
卡维地洛是非选择性β受体阻滞剂/α-1阻断剂,用于治疗轻度至严重充血性心力衰竭和高血压
,
其LogP 值为3.8,碱性 pKa为7.8
(6)
,酸性pKa为15.0(ChemAxon软件计算)。
卡维地洛的溶解度呈pH值依赖性
(7)
。卡维地洛在胃部酸性pH值条件下通过电离的形式溶解。然而,
在碱性pH值下,卡维地洛在远端小肠处可能发生沉淀的
(6,8,9)
。
例如,Stillhart等人研究表明,有78.2-91.8%的卡维地洛以结晶或无定型形式沉淀
(9)
。由于其水溶性差,卡维地洛的生物利用度很低
(10,11)
。
通过GastroPlus™ Simulation软件预测,卡维地洛的口服吸收约为45.9%
(6)
。
通常,
BCS II类药物的溶出度受很多生理因素的影响,如胃肠液的pH值、离子强度、缓冲容量是影响药物释放的三大因素
(2,12)
。
空腹状态下,胃液的pH值为1.4-2.1,进食后,pH值立即增加至pH3.0-7.0(取决于食物组成)。胃液的离子强度约在0.051-0.151mol/L范围内,均值为0.095mol/L
(13)
。胃液在禁食状态下的缓冲容量为0.013-0.019M /ΔpH
(14)
,进餐后约为0.028M /ΔpH
(15)
。
小肠内的pH值从十二指肠到回肠逐渐升高,范围为pH5.5-8.3,取决于具体部位及是否进食
(1,14,16)
。
pH值的增加是由于胃酸中和胰腺所产生的碳酸氢根离子所致
(1,12)
。肠液的离子强度在0.070-0.166mol/L范围内
(17)
。人体肠液的缓冲容量在餐前和餐后分别为0.003和0.013M /ΔpH
(18)
。Kalantzi等人研究发现十二指肠的缓冲容量餐前为0.006M/ΔpH,餐后为0.018-0.030M /ΔpH
(15)
。
由于胃肠液的生理特性,如pH、离子强度、缓冲容量,会随食物的摄入或者不同位置而发生变化,因此,研究这些因素对弱碱性BCS II类药物在胃肠液中的溶解度和溶出行为的影响是很有意义的。
本文的目的是以弱碱性BCS II类药物卡维地洛为例,研究其在模拟胃液和模拟肠液介质(pH为1.2-7.8)中的溶解度和溶出行为。此外,还研究了缓冲盐种类、离子强度、缓冲容量对Dilatrend速释片中卡维地洛的溶解度和溶出行为的影响。
这项研究有助于更好地理解弱碱性BCS II类药物卡维地洛在生理胃肠液pH范围内的溶解度和溶出行为,这将有助于我们了解这类药物在肠道内的溶出度和沉淀行为,并为建立体外-体内相关性的溶出方法提供指导。
卡维地洛(纯度为100.3%、总杂质为0.1%);
Dilatrend速释片(含25mg卡维地洛)(ROCHE Australia,lot#M2049B01);
磷酸二氢钠和磷酸氢二钠(Sigma-Aldrich,德国);
磷酸二氢钾、氢氧化钠和氯化钠购自Riedel-deHaën(德国);
醋酸购自ACROS(USA);
三水醋酸钠购自Fluka(美国);
盐酸(37%w/v)购自GFS Chemicals(美国)。
双蒸水使用GFL蒸馏装置制备(德国)。
所有化学试剂均为分析纯。
2、用于溶解度和溶出度研究的介质
本研究中使用的模拟胃液和模拟肠液如下:
模拟胃液的溶出介质:
(a)0.7%HCl(USP 38,pH 1.45)
(b)不含胃蛋白酶的模拟胃液(SGFsp,USP 38; pH1.2)
(c)空白餐前状态模拟胃液(空白FaSSGF,pH 1.6)
(19)
(d)空白餐后状态模拟胃液(空白FeSSGF,pH5.0)
(20)
模拟肠液的溶出介质
:
(a)不含胰酶的模拟肠液(SIFsp,USP26; pH6.8)
(b)0.05M磷酸盐缓冲液(pH 6.8)
(21)
(c)醋酸盐缓冲液(USP 28,pH 4.5)
模拟十二指肠液的溶出介质:
(d)空白餐前状态模拟肠液(空白FaSSIF,pH 6.5)
(e)空白餐后状态模拟肠液(空白FeSSIF,pH 5.0)
(22)
本文中的空白是指配制溶出介质时,不添加酶、表面活性剂或胆盐。
除了药典标准介质外,模拟肠液配制采用了pH 6.8磷酸盐缓冲液,并配制了不同的缓冲液浓度(6.25、12.5、25、50和100mM)以获得具有可变离子强度和缓冲容量的溶出介质。
磷酸盐缓冲液(100mM,pH 6.8)是根据Sigma-Aldrich Buffer Reference Center配制的
。无离子强度和缓冲容量的双蒸水作为空白对照。
pH7.2和pH7.8磷酸盐缓冲液也是根据Sigma-Aldrich Buffer Reference Center配制的,用于模拟回肠末端和模拟结肠的pH值。
本研究中用到的溶出介质的化学组成和理化性质(pH、离子强度和缓冲容量)见表I、II、III、IV。
3、溶出介质的理化性质
溶出介质的pH通过pH计测量,pH计在测量前需经校验。离子强度计算公式如方程(1)所示
(25)
。
介质的缓冲容量用Van Slyke方程(2)来计算。
4、溶解度研究
所有介质中卡维地洛的溶解度测定方法为:在已装有50ml介质的烧杯中加入过量的卡维地洛,将烧杯置于水浴振荡器上,速度为50rpm,温度为37℃±1℃。通过校正后的pH计监控介质的pH值,如有必要调节至初始值。经1、2、4、6、24h后,取溶液5ml,以3500rpm离心15min,取上清液并用介质稀释至适当浓度,采用UV法在285nm处采用标准曲线法测定供试品中卡维地洛的浓度。平行制备三份样品,SD应小于10%。
溶解度(Cs)与药物浓度(C
D
)的比值,Cs/C
D
用来表示漏槽条件(S值)。根据USP规定,S大于3即符合漏槽条件(26)。卡维地洛在各pH值下的离子性百分数通过Henderson-Hasselbalch方程(3)计算。
5. Dilatrend
片中卡维地洛的含量测定
Dilatrend片中卡维地洛的含量
采用UV测定
。
方法为:取10片,研细,精密称取约相当于卡维地洛25mg的细粉适量,置100ml量瓶中,加双蒸水10ml、甲醇-1M盐酸(9:1)混合溶液70ml,超声处理30min,放冷,用甲醇-1M盐酸(9:1)混合溶液稀释至刻度。样品溶液采用3500rpm离心15min,取上清液,用甲醇-1M盐酸(9:1)混合溶液稀释至合适的浓度,在285nm处测定吸光度,采用标准曲线法测定供试品中卡维地洛的浓度。平行制备三份样品。Dilatrend片已通过重量差异检查。
6. 溶出研究
采用
已校验的溶出仪(方法2桨法)进行溶出测定
。
转数为50rpm,介质体积为900ml,温度为37±0.5℃,在5、10、15、30、45、60、75、90、105、120、150、180、210、240min自动取样,用0.45µm滤膜滤过。为了考察聚乙烯膜对卡维地洛的吸附,考察了卡维地洛粉末在0.7%HCl(USP38,pH1.45)介质中的溶出情况,取样量与Dilatrend片相似,溶出该条件与Dilatrend片相似。
结果表明,过滤前后卡维地洛没有明显损失,回收率大于99.0%。
为了考察辅料是否干扰,配制了混合辅料,包括蔗糖、乳糖、聚维酮、交联聚维酮、二氧化硅和硬脂酸镁。在0.7%HCl(USP38,pH1.45)中进行了空白辅料考察,
结果表明,在285nm波长处辅料无吸收,说明辅料无干扰。
Dilatrend片中卡维地洛的溶出量通过标准曲线计算,溶出介质的pH值在整个试验过程中进行监控,
曲线的相似性通过相似因子f2进行评价,见公式(4)
(28)
。
如果f2小于50,说明溶出存在显著差异,如果f2在50-100之间,说明溶出相似。















