据悉,2001年我国医药出口额仅54亿美元,2015年竟已高达564.4亿美元。以上数据足以证实全球医药市场增长迅速。仿制药市场持续升温对我国自主创新能力较弱的制药企业无疑是一个契机。我国制药企业在保持原料药的基础上扩大制剂的出口,尤其是扩张对美国、欧洲、日本等世界主流医药市场的销售。然而,药品是一种特殊的产品,医药行业特殊。要想让中国药品“走出国门”,除制药企业具有国际注册和生产质量体系国际认证的经验外,更重要的是要求制药企业确保对他人知识产权不侵犯的前提下筛选出具有优势的产品。
鉴于各个国家有关知识产权的立法情况不一,因此有必要对一些主流国家的有关药品的立法情况进行梳理,为制药企业筛选品种时提供立题依据。与药品相关的知识产权主要有专利(Patent)和试验数据独占权(Data Exclusivity,也称试验数据保护)。专利对于大多数企业而言已经不再陌生。由于各国专利立法不一,因此专利保护期也不同。譬如,有些国家设有专利延长制度,有些国家则没有;大多数国家的专利保护期以申请日计算,而有些国家的专利保护期曾以授权日或颁证日开始计算。
药品试验数据保护则是指原研药公司为获得新药批准上市而向药品管理机构提交能证明该药品有效性和安全性的一系列“试验数据”。由于仿制药仅需验证其生物等效性与品牌药一致,无需进行大量的临床前试验和临床试验,因此其投资成本和风险大大降低。药品试验数据保护制度的设立就是为了杜绝仿制药公司“搭便车”,借用原研药公司的数据进行注册申报。因此,在数据保护期内不仅仿制药公司无权使用原研公司的试验数据,连药品管理机构也无权参考原研公司的试验数据对仿制药进行审批。
实际上,药品专利保护和药品试验数据保护是两种独立的保护系统,二者之间无直接联系。要判断一个产品对他人知识产权不侵犯,除需确认对他人专利不侵权外,还要确保对他人的药品试验数据也不侵权。
有鉴于此,现将各国专利保护期和药品试验数据保护期届满的计算方法归纳如下:
一、各国专利保护期届满的计算
1、澳大利亚(AU)
以专利扉页中的专利申请日(INID代码22)计,加20年即是专利届满日。
2、加拿大(CA)
①1989年10月1日(INID代码为22或86)之前申请的专利
以专利扉页中的专利证书颁发日(INID代码为45)计,加17年为第一个日期;再以专利扉页中的专利申请日(INID代码为22或86)计为第二个日期;对上述2个日期进行比较,后到期日即是专利届满日。
②1989年10月1日(INID代码为22或86)之后申请的专利
以专利扉页中的专利申请日(INID代码22)计,加20年即是专利届满日。
3、德国(DD/DE/EP)
①1990年7月1日(INID代码为22)之前申请的DD专利
以专利扉页中的专利申请日(INID代码22)计,加18年即是专利届满日。
②1990年7月1日(INID代码为22)之后申请的DD专利(包含1990年7月1日申请的DD专利)以及所有的DE/EP专利
以专利扉页中的专利申请日(INID代码22)计,加20年后所得到的时间再往后加1天即是专利届满日。
(DE专利和DD专利分别为之前的西德专利和东德专利)
4、西班牙(ES/EP)
①1986年6月26日(INID代码为22)之前申请的专利
以专利扉页中的专利授权日(INID代码45)计,加20年即是专利届满日。
②1986年6月26日(INID代码为22)之后申请的专利(包含1986年6月26日申请的专利)
以专利扉页中的专利申请日(INID代码22)计,加20年即是专利届满日。
5、法国(FR/EP)
以专利扉页中的专利申请日(INID代码22)计,加20年即是专利届满日。
6、英国(UK/EP)
以专利扉页中的专利申请日(INID代码22)计,加20年即是专利届满日。
英国设有药物专利延长制度(最长可达5年),因此具体到某个产品时应对其进行特别分析。
7、美国(US)
①1995年6月8日(INID代码为22)之前申请的专利
以专利扉页中的专利证书颁发日(INID代码为45)计,加17年为第一个日期;再以专利扉页中的专利申请日(INID代码为62或63)计为第二个日期;对上述2个日期进行比较,后到期日即是专利届满日。
②1995年6月8日(INID代码为22)之后申请的专利(包含1995年6月8日申请的专利)
以专利扉页中的专利申请日(INID代码62或63)计,加20年即是专利届满日。美国设有临时专利申请制度,对于临时专利(INID为60)则不考虑在内。
与英国相仿,美国也设有专利延长制度,因此具体到某个产品时应对其进行特别分析。
例如:诺华于1996年5月28日获美国专利商标局授权的格列卫产品专利US5521184(该专利申请日:1994年4月28日)原专利到期时间为2013年5月28日,经专利延长一系列程序后,诺华最终获得了该项专利586天的专利延长期。
8、中国(CN)
我国目前尚未设立专利延长制度。与大多数国家相仿,我国给予专利20年的保护期(以申请日开始计算)。
备注:INID代码是专利文献著录数据代码(Internationally agreed Numbers for the Identification of (bibliographic)data)的缩写。为易于识别和查找专利文献的著录项目内容,便于计算机存贮与检索,自1973年起各国专利局出版的专利文献开始标注由世界知识产权组织(WIPO)巴黎联盟专利局间情报检索国际合作委员会(ICIREPAT)规定使用的专利文献著录数据代码,即INID代码。这种代码由圆圈或括号所括的两位阿拉伯数字表示。
二、药品试验数据保护期的计算
1、澳大利亚
澳大利亚于1998年4月17日通过了《治疗用品法修正案》(Therapeutic Goods Amendment Act),该法案首次设置了药品试验数据保护制度,给予新的活性成分(不包括新的剂型,新的给药途径,新增适应症或新的复方制剂)5年的数据保护期,药品试验数据保护期以新药获得上市许可之日起计。保护期内,仿制药公司不能提交原研公司数据向澳大利亚药品管理当局提出注册申请。
2、加拿大
加拿大在1995年修订的《食品药品条例》(Food and Drug Regulations)中首次设立了药品试验数据保护制度,保护期为5年。在Bayer Inc.v.Canada案后的2006年,加拿大又对《食品药品条例》进行了修订,修订后的《食品药品条例》对特定药品进行了不同的保护期。根据加拿大不同阶段的立法情况,有关药品试验数据保护情况如下:
①2006年6月17日之前首次批准的含有活性成分的新药
该类药物主要涉及新的活性成分,对新剂型,新给药途径,新增适应症或新的复方制剂不给予数据保护。对于2006年6月17日之前批准的药物,加拿大药品管理当局给予数据保护期为5年,以上市许可日期起计。保护期内,仿制药公司不能提交原研公司数据向加拿大药品管理当局提出注册申请。
②2006年6月17日之后(包括2006年6月17日批准)首次批准的含有活性成分的新药
该阶段批准的药物,加拿大药品管理当局给予了8年的数据保护。其中,在6年的注册信息保护期内,仿制药公司不能提交原研公司的数据向加拿大药品管理当局提出注册申请。同时,对儿科用药活性成分给予额外6个月的保护,也即是8.5年的数据保护。
另外,加拿大现行的药品数据保护制度不适用于已批准活性成分的改盐、酯、对映异构体、溶剂化合物以及多晶型。
上述药物各保护期均以上市许可日起计。
3、欧盟
A、2004/27/EC指令生效之前,欧盟各国的数据保护
2001年,欧盟通过2001/83/EC号修正令。该修正令规定,对于在欧盟(包括列支敦斯登/瑞士)首次获批上市的新药给予6年或10年的数据保护,保护期以上市许可日起计。数据保护仅适用于新化学实体,不适合后来批准的新剂型、新给药途径或新增适应证。
①对于集中注册程序批准的药物,其保护期自首次获得欧盟批准之日起10年。
②对于在欧盟任一国家或相互认可注册程序批准的药物,其保护日自首次获得上市许可之日起计,保护期以药物首次上市国家的法律规定为准(欧盟各国有关数据保护的立法情况见表1)。
表1 欧盟各国有关数据保护的立法情况
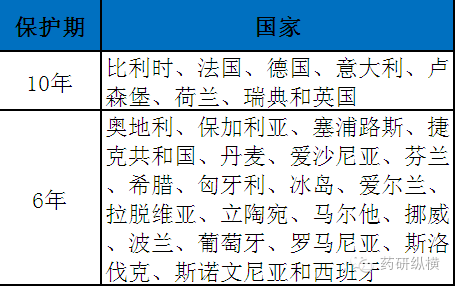
备注:2004年5月1日2004/27/EC指令生效之前,波兰给予3年的数据保护期;
自2004/27/EC指令生效之后,波兰才给予6年的数据保护期。
B、2004/27/EC指令生效之后,欧盟各国的数据保护
2004/27/EC指令规定欧盟任一成员国,按照集中注册程序批准的药品以及按照非集中注册程序批准的药品均同意遵循“8+2+1”模式进行保护。也即是新药在上市8年后,仿制药公司可以简略程序申请仿制药,但需要在10年的保护期届满后才能上市销售。对于获批新增适应证的药物,其保护期则可延长1年。
于2005年11月20日之后在欧洲上市的各药品,其保护期以首次获得许可上市之日起计,保护期为10年。对获批新增适应证的药物,其保护期将延长至11年。
4、美国
美国是首个设立药品数据保护制度的国家。美国的药品试验数据保护源于1984年9月24日通过的《药品价格竞争和专利期恢复法》(也称Hatch-Waxman 法案),该法案给予新化学实体5年的数据保护期。其中,5年的保护期有个例外,即是如果所提出申请的仿制药是Paragraph Ⅳ Certification,则相应的试验数据保护期降为4年。
FDA对新药补充申请(包括新型制剂、新增适应证以及处方药转换成非处方药)而需进行新的临床试验的药品给予3年的数据保护期。为促进罕见药和儿科用药的发展,美国给予罕用药7年的数据保护期,儿科用药则在5年或3年的保护期上再延长额外6个月。
为促进抗生素的发展,美国于2012年7月通过的《鼓励开发抗生素法案》(GAIN),根据规定,符合标准的抗生素药物将获得额外5年的市场独占权,这样抗生素类药物将获得10年的数据保护期。此外,于2010年3月23日通过的《患者保护以及可承受医费法案》为生物类药物设立了12年的数据保护期(详见表2)。
表2 美国不同类型药物的数据保护期限
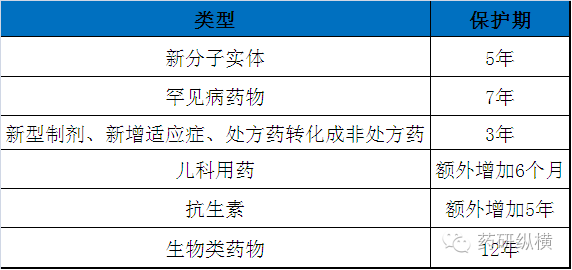 备注:上述不同药物各保护期均以首次获得FDA批准许可之日起计
备注:上述不同药物各保护期均以首次获得FDA批准许可之日起计
值得一提的是,除3年的数据保护期外,仿制药的申请仅在保护期届满后才能提出。FDA对仿制药的平均审评时间为18个月,因此美国的数据保护期实际上在原有基础上相应地延长了18个月,也即是1.5年。
例如:Deferiprone早在1984年就已应用于临床,并于1999年获EMA批准上市,但直到2011年10月14日才获FDA批准上市。Deferiprone在美国无化合物、制备方法等专利,但作为NCEs的Deferiprone可享有5年的数据保护期,其NCEs的数据保护届满日为2016年10月14日。Deferiprone在美国被界定为一种罕见病药物,其作为罕见病药物的数据保护届满日为2018年10月14日。
由此可见,原研公司对Deferiprone的独占权主要是通过数据保护而获得。
5、中国
我国于2002年颁布的《药品管理办法实施条例》第35条首次设立了药品数据保护制度,并以此为依据而制定的《药品注册管理办法》(2007年)第20条对药品数据提供6年的数据保护期。
















