今天是2017年7月28日
农历六月初六
医麦客:分享先进的T细胞工程技术
2017年7月28日/医麦客 eMedClub/--
BioCentury探询Eureka Therapeutics如何开发高亲和力的TCR mimicking抗体。
针对以往被认为是药物无法靶向攻击的细胞内抗原,业界的一场竞赛正在进行中。
作为开发TCR Mimicking(
TCRm
)抗体的先驱,Eureka Therapeutics(
优瑞科
)成功地利用了TCR识别胞内肿瘤抗原的能力来进行药物开发。
然而基于早期以TCR为基础对于相同类型抗原治疗所遭遇的问题,优瑞科还需要消除关于脱靶结合效应的担忧。

2017年6月,Eureka和合作伙伴MSKCC(MemorialSloan Kettering Cancer Center,纪念斯隆凯特琳癌症中心)共同在《Clinical Investigation》杂志上上发表了一项研究,
表明其TCR-mimicking(TCRm)抗体可以识别和杀死小鼠模型内表达肿瘤胞内抗原PRAME的癌细胞。
(注:Eureka研发的针对胞内抗原 peptide/MHC复合体靶点的治疗性抗体,在业界也被称为TCR-mimicking抗体,TCRm抗体或TCR样抗体)
虽然大多数以胞内抗原为靶点的方法都涉及到可穿透细胞的化合物,但是TCRm是从细胞外部起作用。
其技术原理概括如下:
Eureka专有抗体技术开发平台通过靶向MHC/免疫肽段复合物来发现识别肿瘤细胞内的特异性抗原。这些抗体因而能有效识别癌细胞内的特异蛋白质,然后调动免疫系统攻击相关肿瘤细胞。
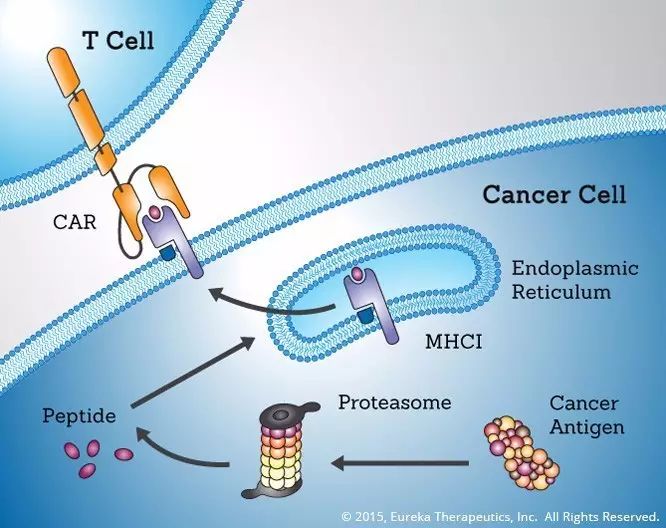
靶向胞内抗原(图片来源 Eureka官网)
优瑞科总裁刘诚博士告诉BioCentury,这种抗体之所以被称为TCR样(TCR mimicking),是因为抗体识别的抗原表位与T细胞(TCR)相同。其表位是细胞表面的9到10个氨基酸的肽段与MHCI形成的复合物。刘诚如此谈到: ”我们正是利用了免疫系统如何识别源自病原体入侵人体细胞而产生抗原的机理“
(注:Eukera的核心技术是开发针对细胞内靶点,实际上是胞内抗原处理后被MHC递呈到细胞表面的多肽复合物的抗体,即功能上类似于TCR的抗体)
事实上,这个领域的大多数研究工作都集中在传染性疾病上,递呈在细胞表面的病毒抗原可被TCRm抗体攻击。但是癌症方面的研究却很少。
MorphoSys AG和Pure MHC LLC的TCRm项目针对的是未披露的靶点。在学术界的科研方面,德州大学MD安德森癌症中心和德克萨斯理工大学健康科学中心报告了针对HER2或TMEM37的两种胞外靶点的TCRm研究。

Eureka CEO-刘诚博士(图片来源 Eureka官网)
对此刘诚博士表示,这个想法看似简单,但对于整个领域却是有着巨大挑战性的。首先是相较于巨大的MHC分子,抗原表位尺寸相当小。其次,
特异性抗原表位以非常低的密度表达在细胞表面。这就意味着抗体必须具有非常高的效能才能将其捕获,同时也需要具有高度的特异性而不识别MHC的其它部分。
“而最大的挑战在于MHC蛋白是身体中最丰富的蛋白质之一,除红细胞外的其他细胞中平均有50万到100万个拷贝,因而对于不呈现肽段的MHC分子交叉反应的耐受性几乎为零。“刘诚如是说。
MorphoSys的代理CSO Markus Enzelberger告诉BioCentury,
对该技术的怀疑是基于以前一些公司在修饰TCR提高其特异性方面遭遇的挫折。Enzelberger表示,针对这类靶位(MHC/肽段复合体)一直难以设计TCR,所以大多数人也会预期难以找到特异性的抗体(TCRm)。
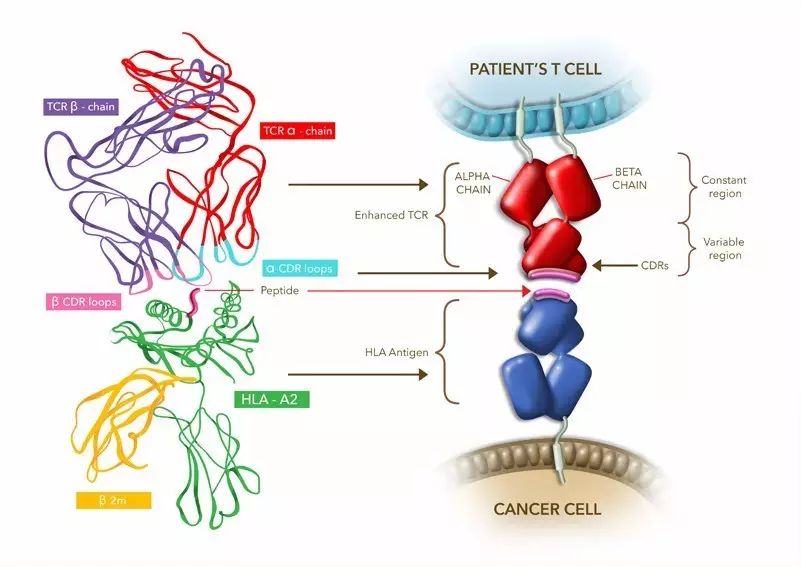
T细胞疗法(图片来源 Adaptimmune官网)
2013年,一名黑色素瘤患者和一名多发性骨髓瘤患者在接受Adaptimmune Therapeutics plc的T细胞治疗后不久,死于心血管方面的毒性。其T细胞疗工程化改造TCR是靶向胞内肿瘤抗原MAGEA3。
尸体解剖发现心脏组织并不表达MAGEA3,但是改造的T细胞被心肌中的无关联抗原表位激活
。
目前,Adaptimmune已经与葛兰素史克公司合作工程化的TCR T疗法,靶向细胞内抗原NY-ESO-1,目前在I / II期临床。其他项目还包括靶向MAGEA10和MAGEA4的I / II期临床。
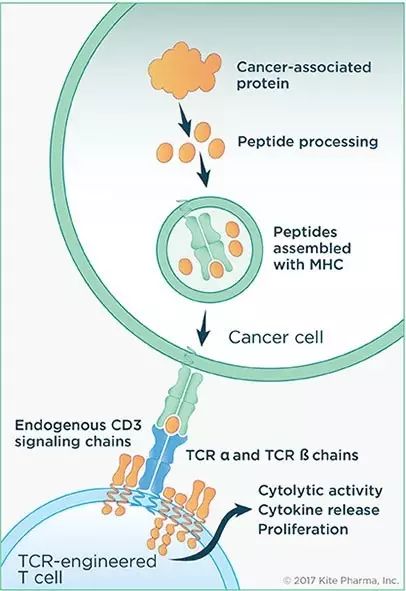
T Cell Receptor(图片来源 Kite官网)
2017年1月,Kite Pharma向FDA提交了KITE-718的研究新药申请(IND)。这是一种经过重编程后能识别MAGEA3和MAGEA6抗原的TCR T细胞疗法。
该公司表示,KITE-718是基于国家癌症研究所(NCI)的MAGE A3/A6 TCR program 的概念验证数据之上的。在NCI的I / II期试验中,没有观察到脱靶毒性。
(注:MAGE A3/A6是在一些常见肿瘤如膀胱癌、食管癌、头颈癌、肺癌和卵巢癌中广泛表达的抗原。KITE-718能够识别与Class II HLA结合的MAGE A3和MAGE A6片段,所以能够直接或间接地激活含有classII TCR的免疫系统,以此来杀灭肿瘤细胞)
据刘诚博士所说,TCRm抗体是可以与针对相同靶位的T细胞疗法竞争的。相比较而言,TCRm抗体更容易生产,并且无需定制(off the shelf)。
但他也同时指出,像HER2或CD20这样典型的细胞表面癌抗原的密度高达每个细胞50000至100000个分子。而相比之下,优瑞科靶向的T细胞抗原表位在每个细胞中少于100个分子。这显然是一个问题,刘诚如此说,
因为抗体介导细胞死亡的机制,比如 CDC和ADCC,需要更高的抗原细胞密度下限才能发挥作用。
刘诚博士表示,因着这些批评和挑战,大多数人认为即使我们可以找到具有特异性的TCRm抗体,也不会有治疗效果。但是对于我们以及MSKCC的合作伙伴而言,这个方法的成功希望却吸引着我们必须进行尝试。
PRAME TIME
2010年,优瑞科与MSKCC达成合作关系,发现并开发针对肿瘤抗原的TCRm抗体(TCR-mimicking)。优瑞科提供了其抗体研发能力及技术平台,而学术界的合作者则提供了其在肿瘤生物学方面的专长。

Eureka专有的E-ALPHA™噬菌体展示平台(图片来源 Eureka官网)
自成立以来,优瑞科已经建立了一个大型抗体库,这个技术平台通过与噬菌体展示技术和全新的筛选系统结合,旨在发现特异性结合肽段表位/MHC复合物的高效TCRm 抗体。其平台也包括对TCRm IgG结构的修饰以增强现有抗体药物的ADCC效应(TCRm抗体诱导的细胞死亡的主要机制)。
目前优瑞科和MSKCC已将公司的平台应用于PRAME。
PRAME是高度特异性的癌症抗原,但因其位于细胞内而在很大程度上研发不足。
根据BioCentury的BCIQ数据库,目前只有五家公司已经宣布了以PRAME为靶点的研究计划。其中包括:
Bellicum Pharmaceuticals





