事件
2018年12月14日,复宏汉霖披露赴港上市招股书。

【海通医药】赴港上市生物科技企业系列解读
1.
歌礼生物吹响赴港上市号角(附招股书摘要)
2.
赴港上市第二家花落华领(附招股书摘要)
3.
赴港上市新军又添盟科医药、信达生物(附招股书摘要)
4.
方达医药(泰格医药子公司)赴港上市招股书摘要
5.
Stealth、AOBiome两家美国企业加入赴港上市队伍
6.
康希诺生物赴港上市招股书摘要
7.
维亚生物赴港上市招股书解读
8.
过会!百济神州赴港第二上市几成定局(附招股书解读)
9.
君实生物赴港上市招股书解读
10.亚盛药业赴港上市招股书解读
11.迈博药业赴港上市招股书摘要
12.翰森制药赴港上市招股书摘要
13. 基石药业赴港上市招股书摘要
附:赴港上市公司招股书下载链接(持续更新中
http://t.cn/RrQc4Bl(注:相关网址需要复制至浏览器打开)
复宏汉霖赴港上市招股书摘要
一、公司简介
复宏汉霖由复星医药与海外科学家团队于2010年2月合资组建,公司主要致力于符合全球标准的生物类似药及创新型抗体药物的研发和生产,研发的产品主要覆盖肿瘤、自身免疫性疾病等领域。
二、股权结构
公司的前2大股东分别是复星新药、Cayman Henlius。全球发售完成后,股权结构如下图所示:
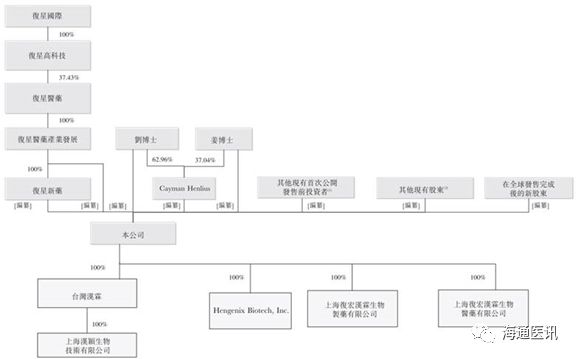
三、高管背景介绍
刘世高博士,复星国际全球合伙人,复宏汉霖联合创始人、总裁兼首席执行官。
1991年获得美国普渡大学生物系博士学位,而后于斯坦福大学进行博士后研究,并攻读雪城大学iMBA课程。曾先后担任美国UBI公司副总裁、美国百时美施贵宝(Bristol-MyersSquibb)公司及安进(Amgen)公司的质量控制总监,拥有超过25年的生技药品研发、生产制造、药政及质量管理经验。曾获得施贵宝公司的技术运营成就奖和瞩目焦点奖。
姜伟东博士,复宏汉霖联合创始人、高级副总裁兼首席科学官。
就读于浙江大学,于中国科学院上海细胞所获得硕士学位,后于德国吉森大学获得微生物与分子生物学博士学位,并在美国加州大学进行博士后研究工作。曾先后在ChemGenics (Millennium),Microcide ,AppliedMol. Evolution (Eli Lilly) 及 Catalyst Biosciences等公司担任高级科学家和总监职务,至今已有20多年的生技药品研发、生产经验,涉及抗体工程、高效重组基因表达系统工程、生产细胞株筛选及工艺优化等各个方面。
郭新军先生,公司副总裁兼董事会秘书。
毕业于上海复旦大学遗传学和遗传工程系,并拥有浙江大学管理学院MBA学位。曾先后就职于华东医疗股份有限公司、杭州九源基因工程有限公司、上海凯茂生物医药有限公司等,担任研究部经理、副总经理、总工程师等职务。曾参与研制中国第一家上市的国家二类新药重组人粒细胞集落刺激因子(rhG-CSF)注射液,获杭州市优秀技术开发人才、浙江省科技进步二等奖、杭州市科技进步一等奖等称号。郭新军先生现担任上海市生物医药行业协会单克隆抗体药物专业委员会副主任委员。
张均利博士,公司高级副总裁兼首席运营官。
张均利博士在加拿大卡尔加里大学获得生物技术博士学位,并在美国凤凰大学获得工商管理MBA。在美国蛋白质科学、人类基因科学、礼来、促基因等生物医药公司担任资深科学家、总监、资深总监等职务,从事研发、工艺放大、技术转移、cGMP厂房设计、欧美生物药品GMP生产管理等工作。熟练掌握生物医药研发、抗体药物产业化的核心技术,特别是大规模单克隆抗体生产技术。
陆英明博士,公司高级副总裁兼首席医学官。
于美国加州大学旧金山医学院分校获得神经科学博士学位并获得临床研究专业人员协会的临床研究认证,同时拥有美国哈佛商学院MBA学位。在科学与医学领域前沿期刊中累计发表文章50多篇,同时作为发明人申请8项专利。先后于Spark Therapeutics、Biogen、Bayer AG、Avigen(Sanofi)、Tularik (Amgen) 等公司担任临床开发、运营高级总监及副总裁等职务,并曾担任美国FDA临床设计委员会成员。最近获得了美国FDA第一个AAV基因治疗产品市场认可,现共有15种产品获市场认可。
四、公司发展历程
主要里程碑:

五、产品管线
通过高效的自主创新,公司已针对肿瘤及自身免疫疾病研发并建立了一个多元化、领先、高质量的产品管线。
在研管线
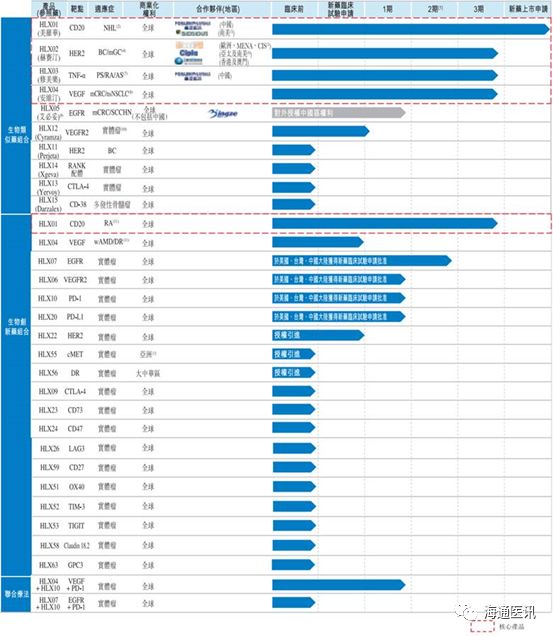
(1)预期可在近期实现商业化的单抗生物类似药
•
HLX01:利妥昔单抗注射液。
HLX01为美罗华生物类似药,就非霍奇金淋巴瘤适应症目前已获得国家药监局上市许可优先审评,预期于2018年底至2019年初取得新药上市申请批准,HLX01可望成为中国首个根据生物类似药指导原则批准上市的生物类似药。此外,国家药典委员会已批准HLX01在中国使用“利妥昔单抗注射液”作为通用名,且已被列入国家医保目录及国家基本药物目录。HLX01用于类风湿性关节炎适应症在国内正进行3期临床试验;
• HLX02:赫赛汀(曲妥珠单抗)生物类似药。
HLX02是首个在中国开发且在中国、波兰、乌克兰及菲律宾开展全球3期临床试验的生物类似药;公司于2018年6月完成3期临床受试者入组,计划于2019年就HER2阳性早期乳腺癌、转移性乳腺癌及转移性胃癌适应症提交新药上市申请。根据弗若斯特沙利文报吿,HLX02有潜力成为在欧盟推出的首个由中国公司开发的单克隆抗体生物类似药。曲妥珠单抗已被列入国家医保目录及国家基本药物目录;
• HLX03:修美乐(阿达木单抗)生物类似药。
已在国内进入3期临床试验,且已于2018年4月完成受试者入组。公司计划于2019年就斑块状银屑病、类风 3性关节炎及强直性脊柱炎适应症提交新药上市申请;















