
药明康德/报道
《自然》:肿瘤新抗原疫苗取得重大进展
来自美国Dana-Farber癌症中心和德国美因茨大学的两个团队同一天在《自然》杂志发表了两篇关于肿瘤新抗原疫苗的研究。这两个团队都对患者身上的肿瘤样本进行测序,并寻找其中只在癌细胞中出现的基因突变。并以此为基础,分别制造了基于多肽和RNA的疫苗。在晚期黑色素瘤患者身上进行的临床试验显示,这些疫苗能够引起免疫系统针对癌症的特异反应,超过60%的患者体内的肿瘤得到了至少一年的控制。此外,这些疫苗还展示出了与PD-1疗法的协同作用。由于每位患者体内的癌细胞产生的突变都不相同,针对每位患者都设计并制造了相应的疫苗,因此肿瘤新抗原疫苗意味着真正的癌症个性化治疗时代的到来。
《自然》:引起放疗副作用的关键蛋白被找到

清华大学的薛定教授团队通过对线虫模型的研究,找到了放疗后产生副作用的关键机制。在癌细胞接受高剂量辐射死亡后,会向全身释放大量信号,对健康细胞造成伤害。研究发现,细胞死亡后释放的CPR-4蛋白导致了对健康细胞的毒副作用,CPR-4及其上下游信号调控通路中的p53/CEP-1和DAF-2蛋白在这一过程中起了重要作用。CPR-4非常接近于人类的cathepsin B蛋白。这一发现有望带来多个可以减小放疗副作用的药物靶点。
《科学》子刊:CAR-T疗法有望治疗脑癌
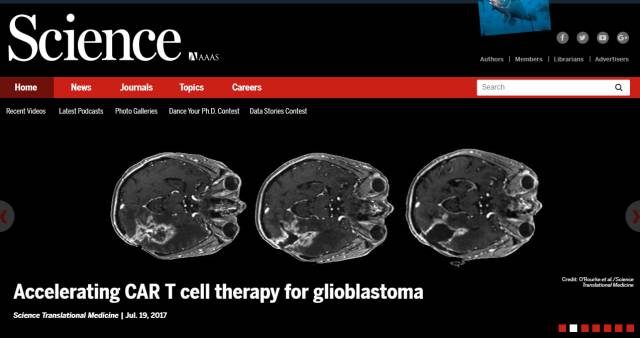
来自美国宾夕法尼亚大学的Carl June教授和他的团队提出了一种用T细胞疗法治疗常见脑癌——胶质母细胞瘤的策略。他们在体外改造T细胞,使其能识别一种在胶质母细胞瘤上常见的突变EGFR蛋白EGFRvIII。在患者身上进行的初步临床试验显示,这款疗法具有良好的安全性,T细胞能够特异识别肿瘤。在7位患者中,5位患者的EGFRvIII表达水平明显下降,显示了T细胞疗法的初步效果。不过这些患者的总体存活期仅有小幅延长。这项早期试验支持了使用T细胞治疗难治脑瘤的可能性。
《细胞》子刊:改造巨噬细胞攻击实体肿瘤
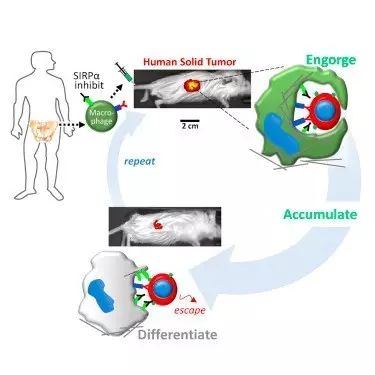
美国宾夕法尼亚大学的Dennis Discher教授团队发表了一种新的免疫疗法策略,通过体外改造巨噬细胞使其识别实体肿瘤,并吞噬癌细胞。癌细胞能够通过在表面表达CD47蛋白,结合巨噬细胞上的SIRPA受体,从而发出“不要吃我”的信号来躲过攻击。Discher教授团队在体外改造巨噬细胞上的SIRPA受体使其不能与CD47结合。他们将经过改造的巨噬细胞输回一个肿瘤的小鼠模型后,这些细胞能够聚集在肿瘤中并攻击癌细胞,使肿瘤体积减少了80%。这项研究有望带来一种可以与CAR-T疗法媲美的细胞免疫疗法。
《自然》:利用CRISPR技术寻找抗癌药物靶点

来自美国Dana-Farber癌症中心的Nicholas Haining教授团队发表了一项利用CRISPR技术在小鼠模型中寻找可以加强PD-1免疫抑制剂疗效的药物靶点的新研究。PD-1免疫抑制剂并不是在所有的患者体内都能取得很好的效果,因此科学们认为癌细胞还有其它可以抑制免疫系统的信号通路。CRISPR/Cas9系统对于基因的强大编辑能力使其能够高效率地筛选大量基因。在一个小鼠的黑色素瘤模型中,Haining教授的团队测试了2000多个基因对于PD-1免疫疗法的影响。除了已知的一些靶点如CD47之外,他们还发现了一些新的靶点,如PTPN2。PTPN2是一个酪氨酸去磷酸酶,敲除这个基因能够提高免疫疗法的效果。这项研究为大规模系统化寻找新的药物靶点提供了指导作用。
《自然》子刊:卵巢癌治疗的新靶点

美国费城Wistar研究的华人学者张如刚教授和他的团队找到了治疗卵巢癌的一个潜在新靶点。他们通过分析卵巢癌患者的样本发现,超过一半的患者带有ARID1A蛋白突变。在细胞和小鼠模型中的进一步研究发现,突变的ARID1A导致HDAC6表达量上升。HDAC6是一种去乙酰化酶,它的一个直接底物是抑癌蛋白p53。过多的HDAC6使p53上的关键位点去乙酰化,导致p53的抑癌功能受到影响。为了证实这一机制的作用,张教授团队使用了一种HDAC6抑制剂ACY1215,将其注入卵巢癌小鼠模型体内。实验发现,ACY1215抑制了肿瘤的生长,延长了小鼠生存期。这一研究发现了ARID1A和HDAC6具有合成致死的效果,为卵巢癌药物研发提供了一个新靶点。
《科学》子刊:早期检测胰腺癌的新方法
来自美国宾夕法尼亚大学的Kenneth Zaret教授及其团队发表了一项早期诊断胰腺癌的新方法。通过在一个由Zaret教授建立的胰腺癌体外细胞模型中的研究,这个团队首先发现了50多个在健康人群中表达量很小,在癌细胞中表达量上升的基因。然后通过实验将范围缩小到3个可能导致胰腺癌的基因。随后在胰腺癌患者和健康志愿者的血液中检测了这3个蛋白的水平,发现thrombospondin-2 (THBS2)是最佳选择。他们将THBS2和一个已知的胰腺癌标记物CA19-9联合使用,在500多名患者中进行的试验,结果发现这两种标记物联合使用检测胰腺癌的敏感度达到了87%,特异性更是超过98%。这一发现有望帮助医生们更早诊断出胰腺癌患者,尽早治疗获得最佳效果。
参考资料:
[1] An immunogenic personal neoantigen vaccine for patients with melanoma
[2] Personalized RNA mutanome vaccines mobilize poly-specific therapeutic immunity against cancer
[3] Cysteine protease cathepsin B mediates radiation-induced bystander effects
[4] A single dose of peripherally infused EGFRvIII-directed CAR T cells mediates antigen loss and induces adaptive resistance in patients with recurrent glioblastoma
[5] SIRPA-Inhibited, Marrow-Derived Macrophages Engorge, Accumulate, and Differentiate in Antibody-Targeted Regression of Solid Tumors
[6] In vivo CRISPR screening identifies Ptpn2 as a cancer immunotherapy target
[7] ARID1A-mutated ovarian cancers depend on HDAC6 activity
Detection of early pancreatic ductal adenocarcinoma with thrombospondin-2 and CA19-9 blood markers

















