作为一名医疗器械法规工作者,每天都有一堆似乎永远都忙不完的工作,不是默头编写各种文件、整理资料,就是奔走于各大检测所、食药监局,或者就是一些法规培训,有时候遇到一些棘手的问题,常常夜不能寐,工作职能,常常跨越质量、体系、文控、研发等等,哪里有需要,就去哪里,哪里有法规风险,就去哪里,义务加班成为常态,当别人问及你的职位时,说得最多的一句就是“打杂”,在各大群里,经常会看到群昵称都标注的是“打杂”、“跑腿”,而我们大家都习惯性地这样介绍自己,这就是法规工作者……
忙碌的我们没有更多的时间去思考我们的出路和未来,即使思考过,有时候却也有些迷茫……
今天,咱们就来聊一聊法规工作者们比较敏感的话题,“薪资”

医械资讯社区本次收集的城市主要为苏州和深圳,因为这两个地区的医疗器械公司占比最高(北京其实也多,但由于时间关系,所以未加入),相对来讲,更具有代表性一些,所以共收集了深圳72家企业和江苏44家企业相关的法规招聘岗位(注册、体系、质量等),以注册专员、注册工程师、体系工程师、法规经理、质量经理、国际注册等为主,虽然两地物价、消费水平和房价没有一定的可比性,但从事一线的法规工作的薪资水平,却有着一些共性。
本次整理的目的,仅仅只是为了帮助各位法规从业人员及人力资源快速了解薪资行情,也许能为你的职业规划和发展方向带来一些启示,你的出路在哪里、你的薪水现在处于什么阶段、你是否满足于当前的薪水、是否需要重产调整学习方向或发展方向……

以下数据来源于知名的招聘网,均为2017年6月最新发布,双击可方大查看:
我们先来看一下深圳地区的招聘情况,后面将分类进行对比:
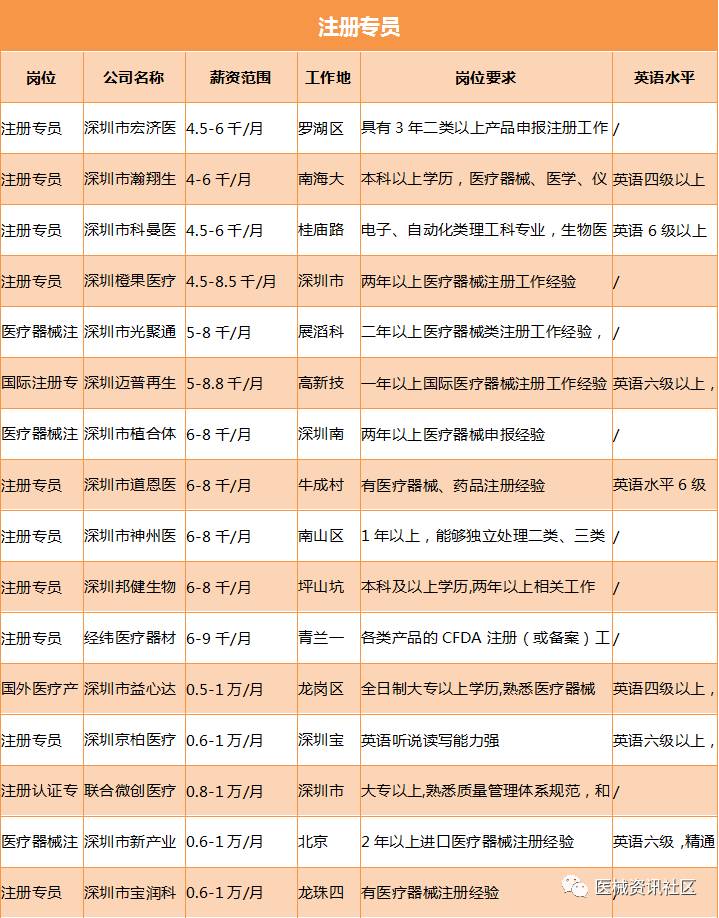
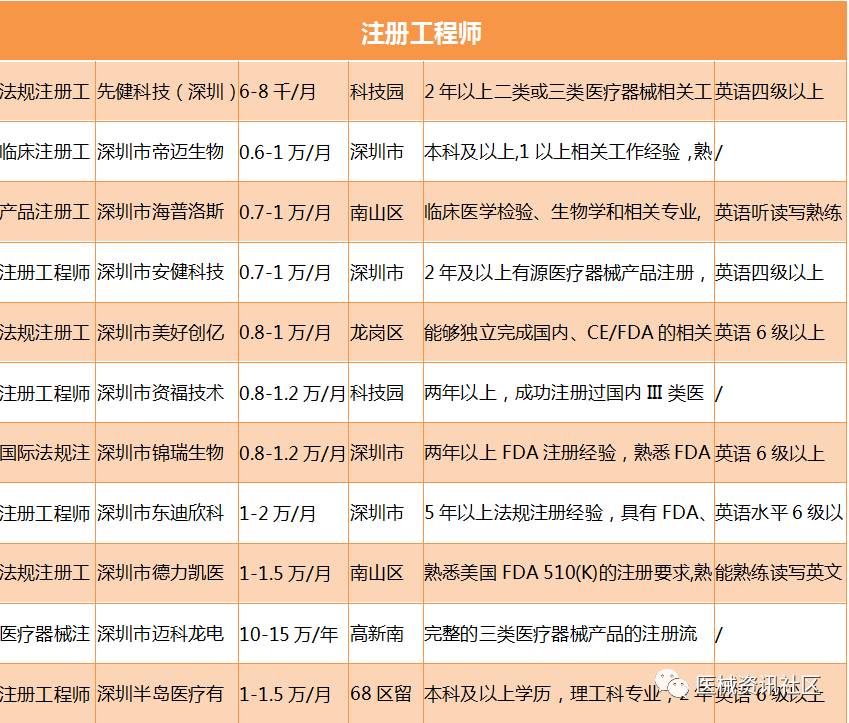
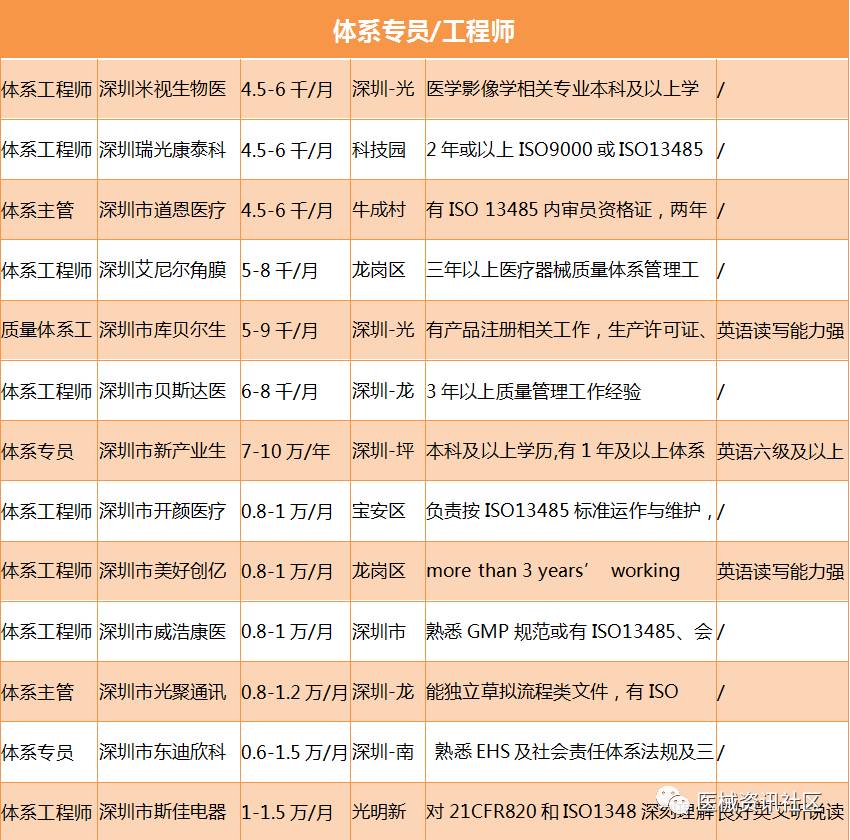
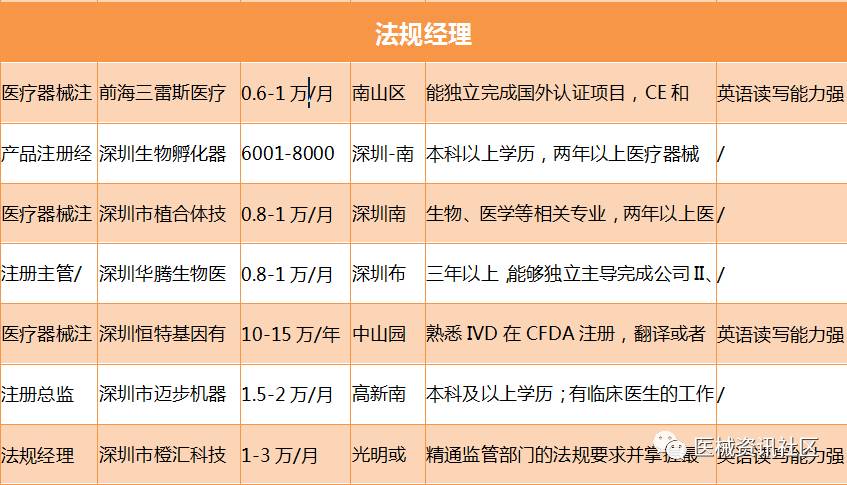

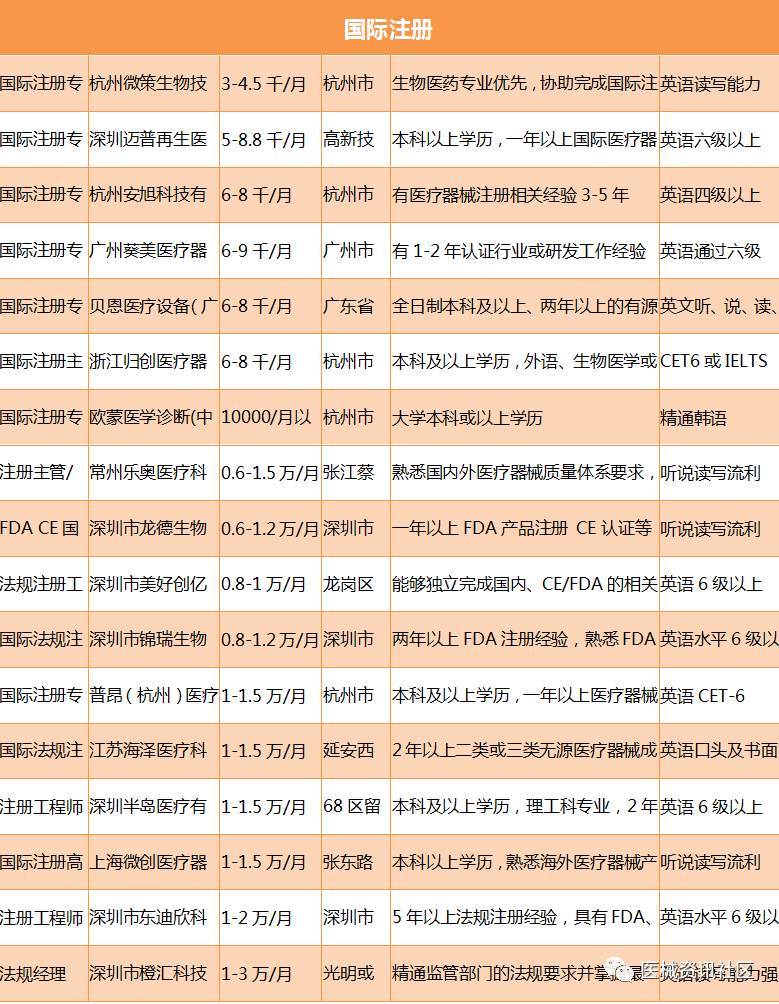
我们再来看一下苏州地区的招聘情况,后面将分类进行对比:
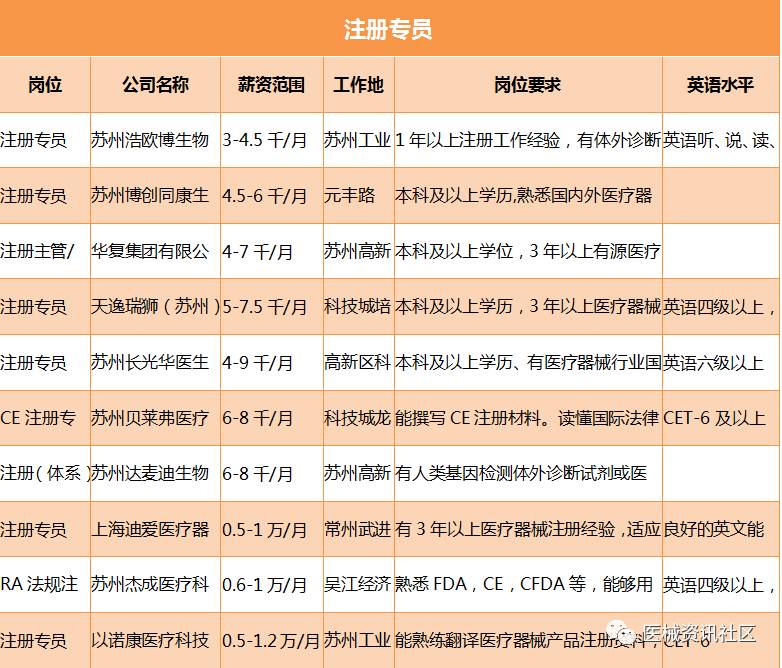
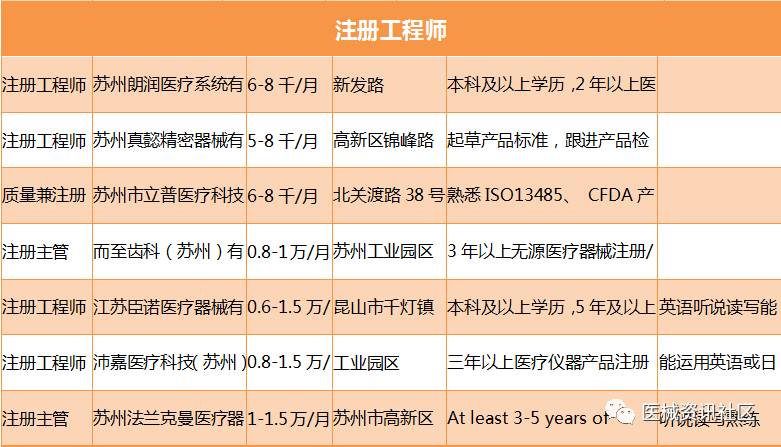
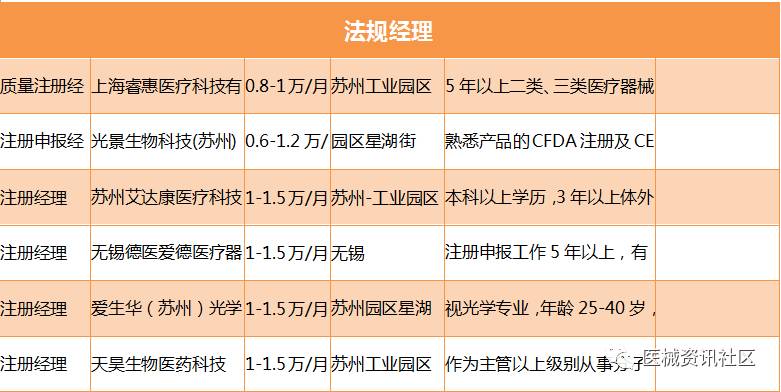
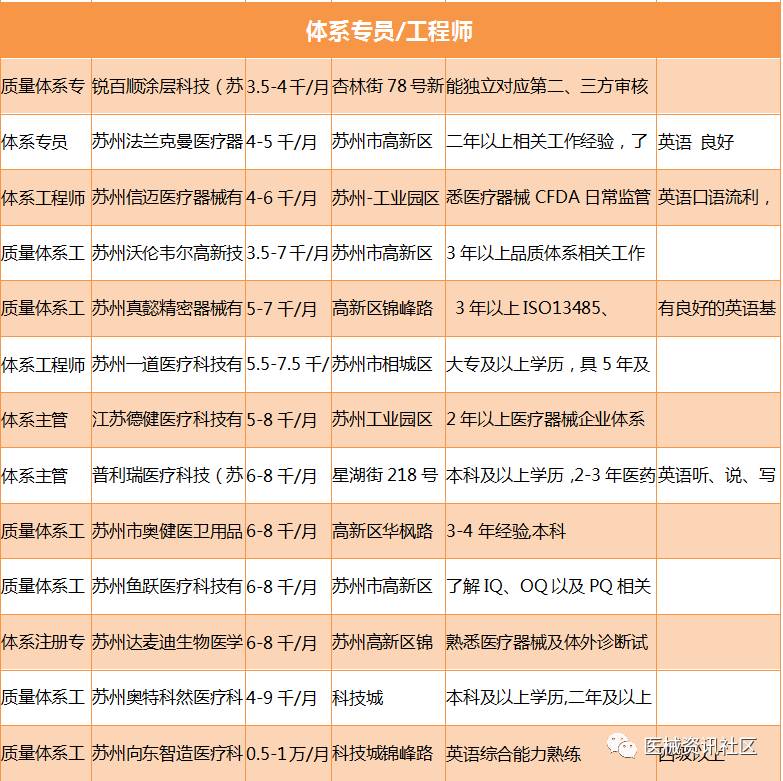

不知道各位看完以上的招聘信息后有何感想?
自从监管越来越严格,新法规不断,加上各大小企业的全球化产业布局,都在以CE、FDA、巴西等为主要战场。所以注册工作难度加大,专业知识水平更高,医械资讯社区从整理的招聘数据来看,法规工作者的门槛是越来越高,学历最低为大专,大部份为本科医疗相关专业,越来越多的任职条件都有英语4级以上的要求。

以下为医械资讯社区整理的对比,供大家参考:
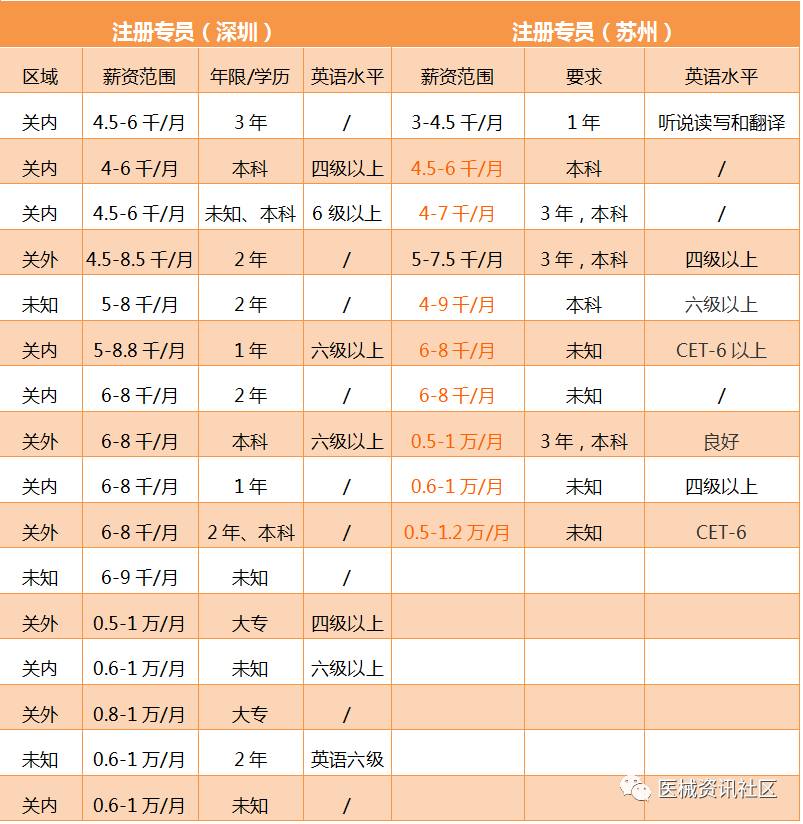
不管是深圳还是江苏,注册专员的薪资水平基本在4千至1万左右,范围值比较大,工作年限都在1年至3年左右,有英语硬性要求的,薪资水平比普通高2000左右,不论关内或者关外,都没有明显的差异。而注册专员是法规工作者的入门级。
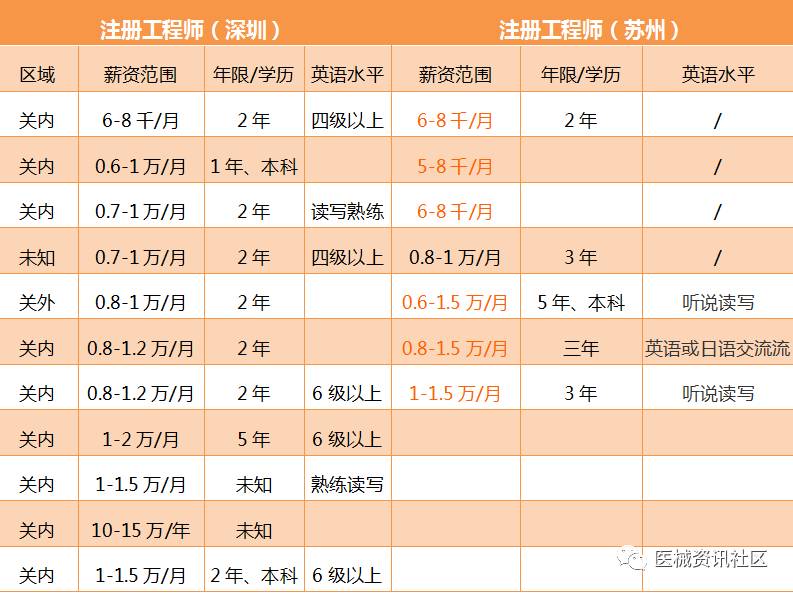
经过入门级“注册专员”的2年沉淀,具备了基本的法规知识,以及跑腿两年后学习到注册的基本流程,学习平台好的,基本上都撑握了独立注册的能力,这时候不论是在公司继续成长,还是跳槽出来,都会晋升为法规工程师等级,以薪资来看,苏州和深圳差异不大,起步价在6000以上,上限为1.5万。年限至少在2年以上,如果英语能力好的,则可能突破1万大关。而普通的注册工程师,此时突破1万大关似乎为些为时尚早。但如果刚从学校出来经过两三年的洗礼,就有可能突破1万元的大关,还是前途无量的

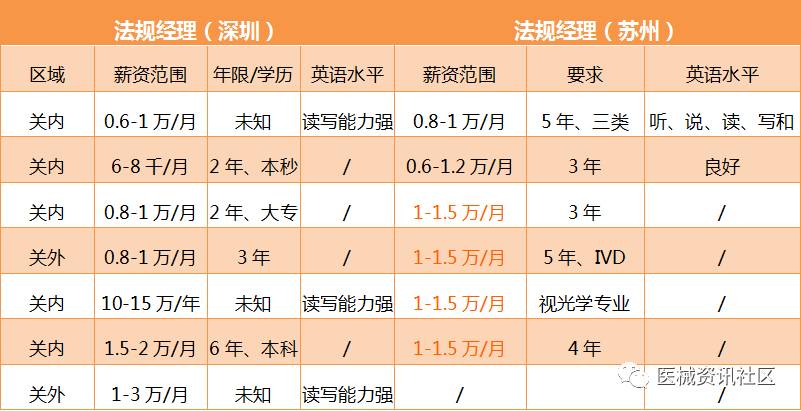
对于注册攻城狮来说,发展方向一定是越来越好,职位也会越来越高,注册专员经历两年,再经历几年攻城狮,不论如何,都会晋升,也许是资深法规攻城狮,也许是法规主管,也许是经理,对于个人职业规划来说,这是很好的发展方向和目标,但,事实并非如此。
从上面的招聘数据来看,苏州和深圳也没有太大的差异,深圳的上限比苏州要高,但同时对能力的要求也高不少。
其实公司更多的是以注册专员、法规攻城狮为主要招聘方向,就算招聘注册经理,薪资水平和攻城狮差不多,甚至有些名义上的注册经理,还不如攻城狮, 为什么会出现这样的一种怪像呢?

其实,单从注册角度来讲,真正做注册的,不是注册专员,就是法规攻城狮,头衔并不重要,就算是注册经理,下属也许就一两位实习生或助手,或者压根就没有,普遍来讲,法规经理的薪资水平很难突破1万5的大关(国际注册后面讨论),大公司则会不一样,但对于大众来讲,大公司未必是你想去就能去的,所以,这是多少注册工程师都将面临的一个瓶劲!
但有一个现象还是值得庆幸,注册经理的招聘要求里面,对英语的硬性要求没有那么高,毕竟作为管理方面的人才,更多的是需要带团队、人脉和统筹能力强等。
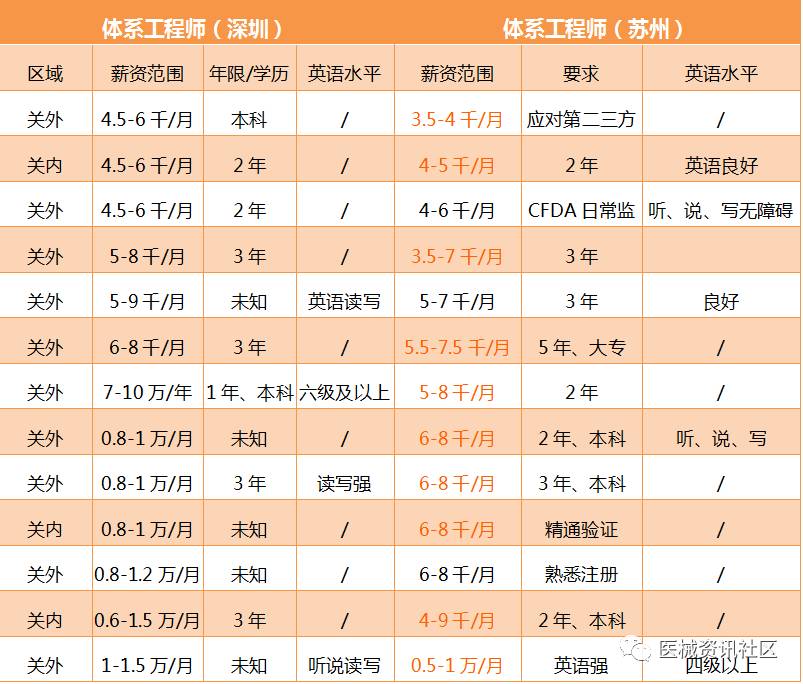
看完注册,我们再来看一看法规涉及的另一个岗位-体系工程师,体系不同注册,体系很少讲体系专员,都是以体系工程师定位为主,从上面的数据来看,体系的薪资水平和注册工程师的水平差异不大,也许刚入行还会更低,现在还有3500的工资。
深圳与苏州相比,起步工资与上限要高于苏州,要求却比深圳要高,从整理数据时发现,苏州企业对英语方面的要求更高,学历也高,年限要求也稍多一些,而且很多体系工程师的岗位职责里,都涉及注册方面的工程。
大家也许发现,医械资讯社区没有加入体系经理的数据,其实,体系工程师都被划到的质量部门下面,上司不是质量经理,就是法规经理或注册经理,只有大企业可能会单独将体系设为独立部门,由管理者代表为核心。

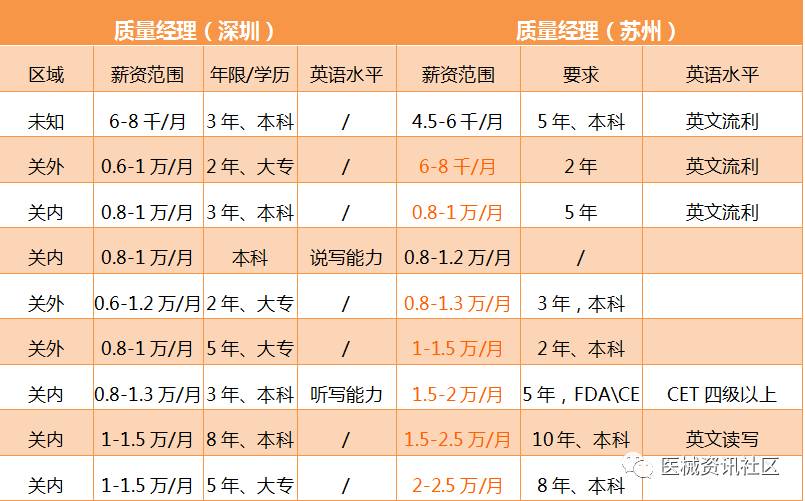
既然体系工程师普遍被划到质量部门,那质量部经理也是法规工程最重要的执行者和宣导者。从上面数据来看,苏州与深圳的薪资相差不算很大,苏州对质量经理的定位还有4.5起的,并且要求英文流利,而深圳起步为6000,要求大专以上,对英语没有要求,而上限来看,深圳为1.5万,苏州为2.5万,但年限与具体要求要高于深圳。这只是6月最新的数据,并不代表深圳的质量经理上限都为1.5万,想必大家都知道,工资更高的,人员基本稳定。
注册与质量相比,质量部门算是一个大部门,下属人员配置较多,涉及的内容也更广,更偏向于公司内部管理和法规的直接执行者,而质量体系又普遍划在质量部门,所承担的法规风险会更高,而招聘的工作职责也是如此。
但奇怪的现象来看,作为这么重要的一个岗位,一个部门经理,薪资水平普遍偏低,6000起招来的质量经理,要求把质量控制好,还要把体系贯彻到位,作为公司的BOSS,你能放得下心吗?
从CFDA官网发布的2016年飞检信息看,从2016年4月至11月,共对51家企业进行了飞行检查,其中11家停产整改,4家在飞行检查时已提交产品注册证或生产许可证的被注销申请,总占比约29%。涉及主要城市为北京、江苏、山东和广东等。不符合项涉及最多的是生产、质量部门
飞检力度在不断加大,涉及面也越来越广,越来越细,公司高层也引起重视,但从招聘的信息来看,似乎并没有从根本重视,招聘的要求高了,岗位职责也更多了,但薪资水平依然没有变化
而作为质量经理,如何蜕变和突破,则需要进一步思考……

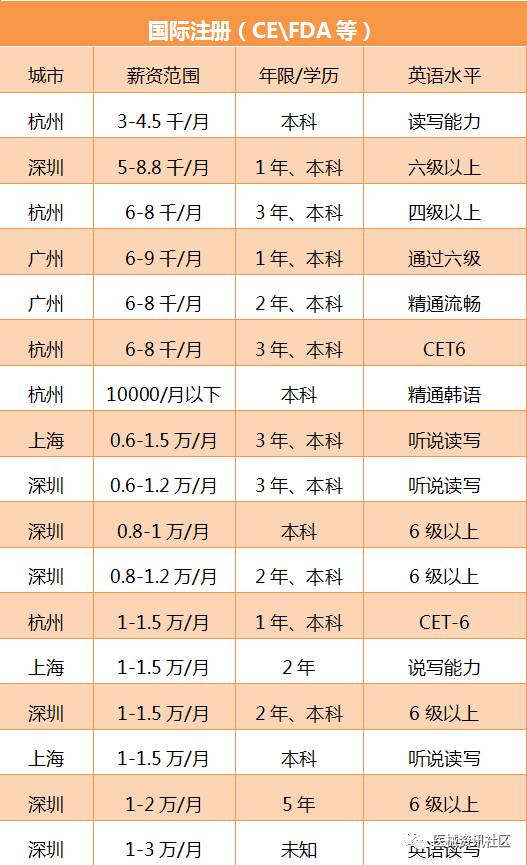
国际注册是很多注册攻城师都面临的问题,英语要求过硬,对于天生就害怕英语的伙伴们,无疑是望而生畏的领域,难怪做国际咨询的机构生意源源不断,异常火暴












