含吖啶片段的乙酰胆碱酯酶双位点抑制剂的合成及活性测试
Synthesis and Activity of Acridine-based Acetylcholinesterase Inhibitors
张 赢1,杨凤志1,2,姜发琴1,谢东升1,傅 磊1,2*
(1. 上海交通大学药学院,上海 200240;2. 上海交通大学-安捷伦科技药物分析联合实验室,上海 200240)
摘要:以吖啶和苄胺为关键片段,通过不同长度的碳链连接,合成了9 个乙酰胆碱酯酶(AChE) 抑制剂,并经核磁共振和高分辨质谱分析确证结构。测试了目标化合物对AChE 的体外抑制活性。结果显示,目标化合物对AChE 的抑制活性随着连接链长度的增加而提高;六碳链化合物的活性最佳( IC50=17.19 nmol/L)。本研究还通过计算机模拟对接分析,对活性测试结果进行了解析。
关键词:乙酰胆碱酯酶;双位点抑制剂;吖啶;计算机辅助药物设计
阿尔茨海默症(Alzheimer's disease,AD) 是一种神经退行性病变,主要表现为记忆和认知受损。AD 给患者及其家庭带来了沉重的负担,针对AD药物的研发迫在眉睫。在AD 的发病机制中,胆碱能系统的损伤会导致AD 患者的大脑功能异常[1]。乙酰胆碱酯酶(acetylcholinesterase,AChE) 是胆碱能系统中重要的组成部分,主要功能是水解乙酰胆碱,从而终止信号的传递。此外,AChE 可促进β-淀粉样蛋白(amyloid beta,Aβ) 的聚集,以致产生神经毒性。AChE 的结构较为复杂,主要包括:催化阴离子位点(catalytic anionic site,CAS)、外周阴离子位点(peripheral anionic site,PAS)、芳香峡谷以及后门区域等。其中,CAS 区域是AChE 的催化中心,而PAS 在AChE 促进Aβ 聚集的过程中发挥了重要作用[2]。抑制AChE 能提高突触间隙胆碱浓度,促进信号传递,还有望抑制淀粉样蛋白的聚集,是抗AD 的重要靶点之一。
目前,AChE 抑制剂按照作用位点主要分为三类:作用于CAS 位点的抑制剂,作用于PAS 位点的抑制剂,及同时作用于CAS 和PAS 的双位点抑制剂。目前已上市的AChE 抑制剂中,除了多奈哌齐与PAS 有微弱的相互作用外,其余均仅作用于CAS 位点( 如利凡斯的明、加兰他敏、石杉碱甲)。相比单位点抑制剂,AChE 双位点抑制剂有望提高化合物的活性,已成为AChE 领域的研究热点[3]。目前,AChE 双位点抑制剂呈现出结构多样性,代表类型有他克林类[3—4]、生物碱类[5]、苄胺类[6] 等。9- 氨基吖啶( 1a, 图1) 是他克林( tacrine,
1b,图1) 的类似物,具有与之相当的AChE 抑制活性[ 7—9];文献报道[7,10—11],9- 氨基吖啶衍生物1c、1d、1e( 图2) 对AChE 同样具有一定的抑制活性。然而,目前对含吖啶片段的AChE 双位点抑制剂研究极少,仅有一篇专利[12]。本研究以9- 氨基吖啶作为结合于CAS 区域的片段,寻求合适的片段结合PAS 区域,中间以合适的连接链连接,希望发现高效的AChE 双位点抑制剂。
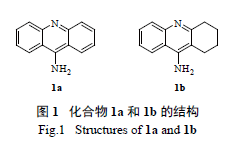
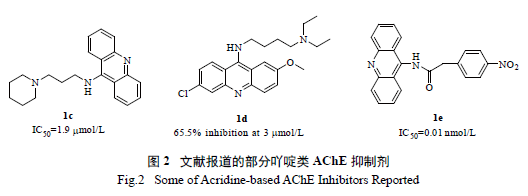
1 化合物的设计
AChE 双位点抑制剂一般由3 个结构区域构成 :作用于CAS 的A 片段,作用于PAS 的B 片段,以及连接A 和B 片段的连接链。其中,A 与B 片段均须带有电荷,或能产生疏水作用;连接链须具有合适的长度,以确保整个分子能同时与CAS 及PAS 发生作用。
本课题组对AChE 的活性口袋( 位点) 进行深入研究,发现PAS 口袋与CAS 口袋完全不同。AChE 的CAS 区域以TRP-86 残基为主要功能结构,空间有限[13],在较深处含有少量难以触及的位点,如酰基口袋、催化三联体等;因此,带有电荷的芳环体系( 如9- 氨基吖啶) 可作为CAS 片段的优先选择。PAS 区域也以TRP 残基为核心,但该区域口袋体积较大,对活性片段的体积要求并不严格[13];同时,该区域具有大量的TYR 残基,能提供氢键供体和受体;苄胺由于同时具备芳环、可电离部分及氢键供体/ 受体,是较为理想的结构。因此,本文以吖啶片段为CAS 结合片段,以苄胺片段为PAS 结合片段,2 个片段之间用不同长度的连接链连接,得到化合物2 系列。化合物2a ~ 2i 的结构式如图3 所示。
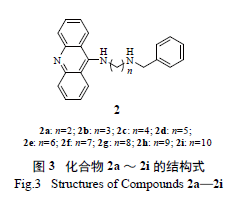
2 化合物的合成
目标化合物的合成路线如图4 所示。以2- 氯苯甲酸(3) 及苯胺(4) 为起始原料,经偶联得2- 苯胺基苯甲酸(5),5 通过分子内环合得9- 氯吖啶(6),6 与苯酚偶联得关键中间体9- 苯氧基吖啶(7);同时二胺11[ 其中,1,9- 壬二胺(11h) 由1,9- 壬二醇( 8h) 经氯代、邻苯二甲酰亚胺钾盐取代、肼解制得;其他二胺为市售试剂] 与苯甲醛(12) 经还原氨化得另一关键中间体13。最后,13 与7 共热得目标化合物2。为增加溶解性,将目标化合物2 制成相应的盐酸盐。本研究共合成了9 个目标化合物。除化合物2b 外,其余8 个化合物均为未见文献报道的新化合物。各中间体及目标化合物的结构均经1H NMR、13C NMR 及高分辨质谱确证。
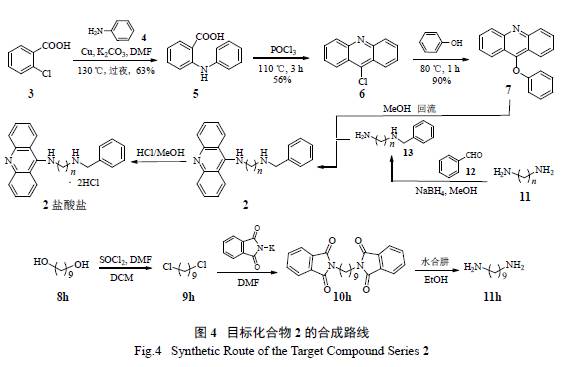
3 化合物对AChE 的抑制活性
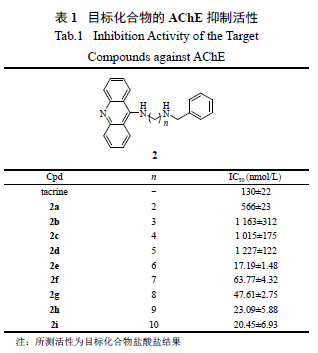
AChE 抑制活性测试:对Ellman 比色法进行改良[14],在96 孔板中进行测定。具体方法参见文献[15]。所用AChE 来源为大鼠的大脑皮质;AChE底物为碘化硫代乙酰胆碱。化合物以盐酸盐形式测定。测定时使用0.1 mol/L 磷酸盐缓冲液(pH 7.4)。每个浓度进行3 次平行试验,用GraphPad Prism 5计算IC50 值。目标化合物的IC50 值见表1。
4 化合物与AChE 的对接
为了进一步探究化合物对AChE 的抑制活性随链长变化的可能原因,将目标化合物与AChE 进行对接研究。
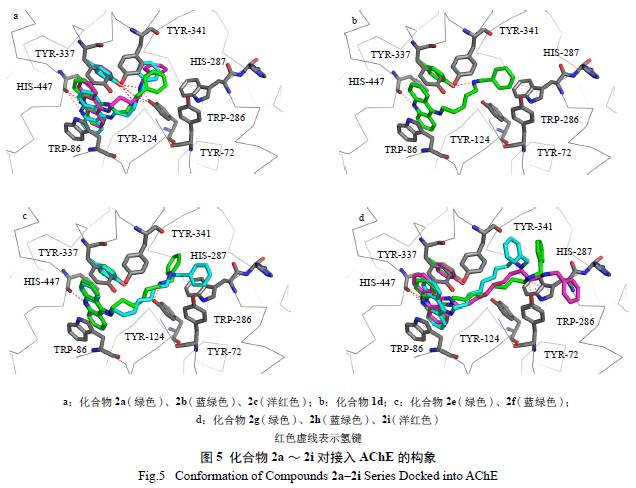
对接研究使用GOLD 软件进行,所用的AChE结构的PDB ID 为5DTI。AChE 的对接过程中,将TYR-337 残基设为柔性。对接条件已经过配体- 蛋白复合物重新对接验证,证明对于多个AChE- 抑制剂复合物而言,每次输出结果中能有至少2 个构象与原有结构相比均方根偏差(RMSD) 值小于3。对接研究结果见图5。从图中可以看出,在所有化合物中,吖啶环都在CAS 区域诱导TYR-337残基发生了相似的构象变化,质子化的吖啶环介于TRP-86 和TYR-337 残基之间,与上述残基发生了π-π 相互作用和阳离子-π 相互作用,芳环上质子化的N 上的H 与HIS-447 残基发生了氢键作用。当链长较短( n=2 ~ 4) 时,苄胺片段无法到达PAS区域的关键残基TRP-286,并与周围的残基产生了较多的过近接触,能很好解释为何这些短链化合物活性较差;当链长为5 时,苄胺的氨基与TYR-124产生氢键作用,苯环勉强到达TRP-286,但苄胺上的苯环受刚性和空间位阻的双重影响,不能与TRP-286 形成合适的角度,无法产生强烈的π-π 相互作用,在活性上体现为活性仍然较低;链长为6时,苄胺片段的苯环与TRP-286 发生π-π 相互作用,且苄胺的氨基与TYR-124 产生氢键作用,因此2e 抑制活性最佳;链长为7 时,苄胺片段的苯环与TRP-286 发生π-π 相互作用,苄胺片段中离子化的氨基与TRP-286 形成阳离子-π 相互作用,但与2e 相比,由于失去了强度更大的氢键作用,因此活性有所降低;链长大于等于8 时,苄胺片段中质子化的氨基能与TRP-286 产生阳离子-π 相互作用,而苯环与TRP-286 近乎垂直,暴露于活性口袋表面。化合物2g(n=8) 的氨基与TYR-72 残基形成了氢键,苯环与TRP-286 形成了较弱的π-π 相互作用。虽然该π-π 相互作用强度不如2h 那么强烈,但由于增加了一个氢键,因此作用力总体增加,2h的活性优于2g。化合物2h( n=9) 中,质子化的氨基与TRP-286 形成了阳离子-π 相互作用,且苯环与TYR-341 形成一定夹角,产生了π-π 相互作用。化合物2i( 链长为10) 与TRP-286 产生阳离子-π 相互作用和π-π 相互作用,质子化的氨基与TYR-72上的羟基发生了氢键作用;此外,化合物2i 的苯环还与His-287 产生了π-π 相互作用。在活性测试中,2i 表现为除2e 外的第二个活性极小值。
5 小结
本研究采用简便易行的方法合成了9 个AChE双位点抑制剂。该系列化合物中,有5 个化合物对AChE 的抑制活性(IC50) 达到了100 nmol/L,其中活性最强的化合物2e 对AChE 抑制活性的IC50为17.19 nmol/L。计算机辅助对接实验发现,化合物2e 能与AChE 形成理想的相互作用。本研究为AChE 抑制剂的进一步研究提供参考。
6 展望
本研究中所涉及的化合物,其组成结构类似于经典的AChE 双位点抑制剂,且对接实验显示该类分子能与AChE 的CAS 和PAS 位点同时发生相互作用;然而,为了进一步证明化合物是AChE 双位点抑制剂,我们还需进一步的验证,例如晶体学试验、酶动力学试验等。此外,在该系列化合物的2个片段或连接链上进行进一步的修饰,有望发现活性更强的化合物。
实验部分
2- 苯胺基苯甲酸(5)
9- 氯吖啶(6)
9- 苯氧基吖啶(7)
1,9- 二氯壬烷(9h)
1,9- 二邻苯二甲酰亚胺壬烷(10h)
1,9- 壬二胺(11h)
化合物13 的合成通法
目标化合物2 的合成通法
化合物2 盐酸盐的合成通法
致谢:感谢香港科技大学的Nancy Ip 教授课题组在活性测试方面的帮助;感谢上海交通大学的魏冬青教授和复旦大学的付伟教授在对接方面提供的帮助。
作者简介:张 赢(1992—),女,硕士研究生,专业方向:药物化学。
Tel:13917755513
E-mail:[email protected]
通信联系人:傅 磊(1962—),男,教授,从事药物化学及药物分析研究。
Tel:021-34204791
E-mail:[email protected]















