2017-09-02
西南医药团队(朱国广/何治力/陈铁林/陈进/周平/张肖星/施跃/张祝源)
中国医药行业正处于“师夷长技以自强”的多层次变革转型阶段 ,从政府到企业的新政策、新药、新技术将会在接下来一个很长的阶段不断向国际前沿看齐。在此背景下,西南证券海外医药一周资讯以投资的眼光整合分享最有价值的国际医药领域进展,帮助投资者更快、更好的了解全球医药的发展方向,把握国内行业发展历史机遇,助中国早日从制药大国向制药强国转变!
海外市场重磅新闻
• 阿斯利康将百亿收购第一三共?双方均否认
阿斯利康即将收购第一三共的消息一经曝出就引来行业热议,尽管双方很快对收购传言进行了回应,但在外界看来,收购或是阿斯利康在重要临床试验结果失败后的另寻他法,而对于第一三共而言,经历了对兰伯西收购案的失败,选择归于比自己体量更大的跨国巨头也不失为良策。(E药经理人)

• 辉瑞白血病新药Mylotarg终获美FDA认可
9月2日,辉瑞(Pfizer)公司宣布,其新药Mylotarg(gemtuzumab ozogamicin)得到了美国FDA的批准,用于治疗表达CD33抗原的新诊断急性骨髓性白血病(AML)的成人患者。FDA同时也批准该药物用于治疗2岁及以上的CD33阳性AML患者,这些患者经历复发或对初始治疗没有响应。值得一提的是,Mylotarg是首款包括儿童AML适应症的药物,也是唯一一款靶向CD33的AML治疗方法。(药明康德)

• 安进多发性骨髓瘤药物显著延长总生存期
安进9月1日宣布,应美国FDA要求的3期临床试验ENDEAVOR的事后分析取得了积极结果,确认了Kyprolis可以延长复发性多发性骨髓瘤患者的总生存期。(药明康德)

•
第一三共糖尿病周围神经性疼痛药Mirogabalin取得积极3期结果
8月31日,日本第一三共制药在研药物mirogabalin的一项用于糖尿病周围神经性疼痛亚洲人治疗的的多中心、随机、双盲、安慰剂对照的临床3期试验REDUCER以及随后52周开标的扩大研究取得了积极的顶线研究结果。(新浪医药新闻)

•艾尔健Truberzi获NICE批准 纳入英国医疗保障体系
近日,目前,艾尔健Truberzi药物获得英国NICE的批准,纳入了英格兰和威尔士地区的国民医疗保障体系,这标志其成为了英国肠易激综合征腹泻患者的首选治疗方案。(新浪医药新闻)

•美国FDA对印度Hetero Labs发出警告信
美国FDA周二公布了本月早些时候向印度合同制造商HeteroLabs在海得拉巴郊区的生产基地发出的警告信,指出其严重违反目前制成品制造规范。(美中药源)

•首款CAR-T疗法获批后 细胞疗法的未来会是什么模样?
8月31日,医药人的朋友圈被一条重磅新闻刷屏:诺华(Novartis)公司突破性CAR-T细胞疗法Kymriah(tisagenlecleucel,曾用名CTL019)获得FDA批准上市,适应症是急性淋巴性白血病(ALL)的25岁以下患者。该药物自研发以来就得到业界广泛关注,最终也如愿成为人类历史上的首款CAR-T细胞疗法。未来细胞疗法将会向三方面发展:靶向实体瘤;聚焦组合疗法和早期患者;个体化疗法到通用型产品。(生物制药小编)

•
诺华CAR-T定价47.5万美元合理么?
诺华声明仅对治疗后出现病情缓解的病人收取费用,而未出现病情好转的病人将不会收取治疗费用。这样的定价在华尔街投资者看来,低于预期36%,而对于患者来讲,远远超过他们的可支付能力,并且在这一标价公开之后引来社会上不少质疑的声音。诺华首席执行官Joseph Jimenez说这样的价格确实高,但是若没有相应的回报,企业无法实现技术上的突破,并且也只有在这样的定价下,诺华才能收回成本,毕竟生产的消耗,重新编辑这些细胞的消耗是非常巨大的。引入合理的竞争,同时在医保制度上保护患者的权益,似乎一条不错的解决途径。(药渡)

海外投融资新闻
•Gilead Sciences收购免疫疗法公司“Kite Pharma”
Kite Pharma成立于2009年,是 CAR-T领域的领先企业。Kite Pharma的拳头产品是嵌合抗原受体CAR-T细胞免疫疗法,通过增强人体自身的免疫细胞来识别并攻击癌细胞。近日,Gilead Sciences宣布公司将以119亿美元的价格收购免疫疗法公司Kite Pharma。(火石创造)

•罕见病诊断法开发商“MedGenome”获3000万C轮融资
MedGenome创立于2013年,这家公司的诊断方法分为两个方面。首先它会在印度提供一系列的基因诊断测试,包括出生前检测、小儿遗传病检测以及肿瘤检测等。之后,它位于硅谷的实验室能提供基因测序、生物信息、计算以及大数据分析等功能。本周,MedGenome获得了3000万美元的C轮融资,由红杉印度和Sofina联合领投,Zodius Capital和其它个人投资者参投。公司将利用这笔系融资去推动精准医疗的研究,并加快生物标志物工程的进度。(火石创造)

学术前沿
•人类多能干细胞改善帕金森猴症状 明年开启临床实验
科学家将由人类诱导多能干细胞(iPS)制成的神经元移植到帕金森病猴子中,使它们在两年内症状得到显著改善,并且没有产生任何危险的副作用。(生物探索)

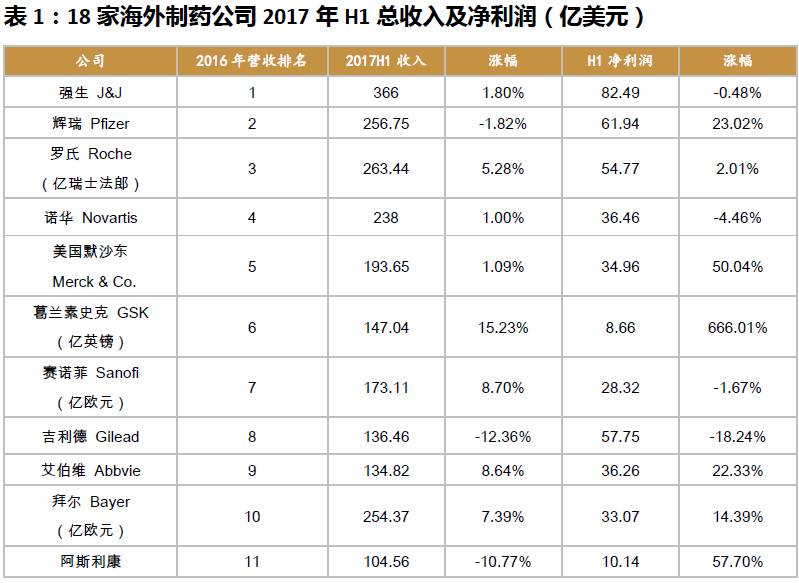
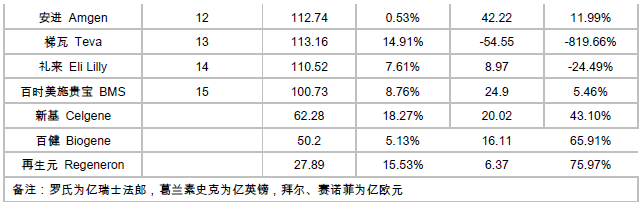
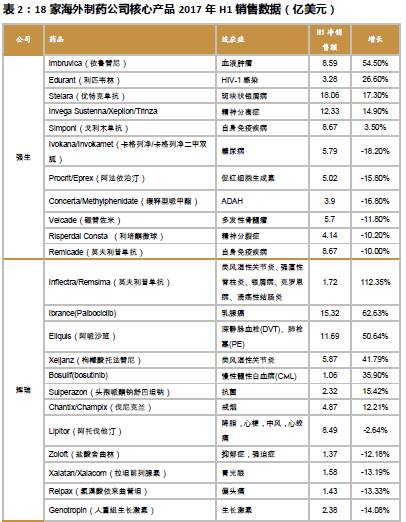
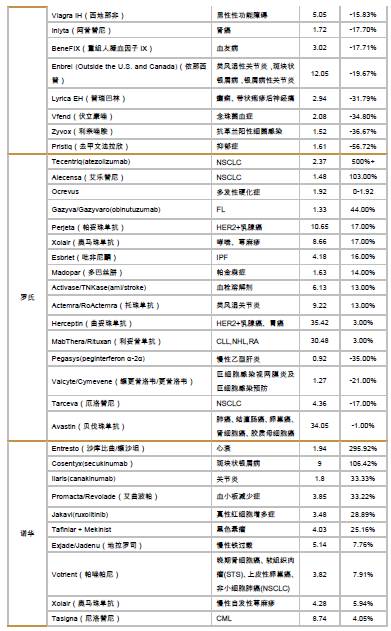
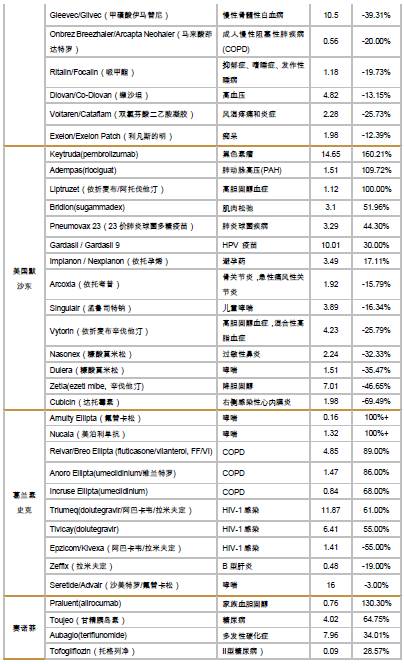
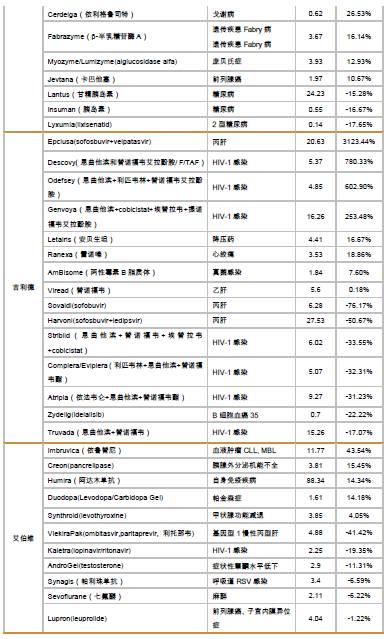
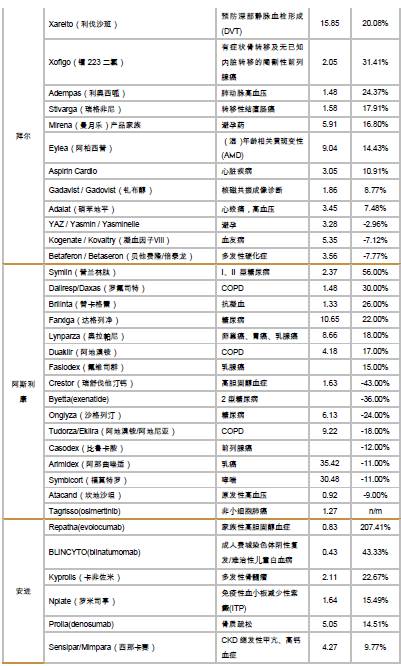
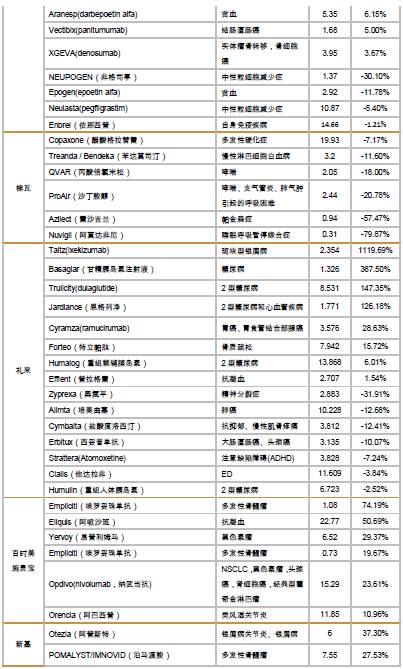
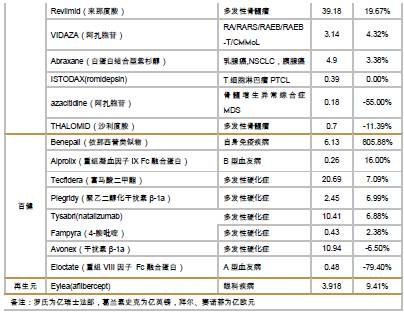
海外医药公司二季报/中报核心数据及点评