一种之前没有引起我们重视的细胞间的沟通渠道(cell-to-cell communication)可能就 是帮助肿瘤细胞和病原体在人体内播散的原因。
Yamashita 的课题组一直在研究果蝇是如 何维持精子供应(sperm supply)这个问题 的,她们也对能够表达某些特异性蛋白的细胞 进行了人工改造。不过奇怪的是,这些被改造 过的细胞并没有发生什么变化,反倒是这些细 胞表达的蛋白却对其它未被改造的细胞造成了 影响。
Yamashita 和她的博士后 Mayu Inaba 将这 种奇怪的现象称作“神奇的走私(mysterious t r a f f i c k i n g ) ” 。这个实验结果是确定无 误的, 但是其中的机制还不得而知。随后 Yamashita 暂停了这个实验,直到一年多之后 的某天,Inaba 给 Yamashita 看了几幅照片。这 些照片清楚地显示了细胞间某些细小的管道互 相联通的现象,这也许就是那些蛋白质的“走 私渠道”。
朊病毒( P r i o n s ) 就是通 过这些细小的纳米管通道 (nanotube),在小鼠细胞之间 传播的。
对于这个结果,Yamashita 还是持怀疑态 度的,于是她决定看看她自己在 12 年前做博 士后期间的实验记录。结果发现,在她以前的 实验记录里也看到了细胞之间这些细小的突 起。Yamashita 当时大吃了一惊。2015 年,她 们发表了这项研究成果,指出这种纳米管可能 就是帮助睾丸细胞与邻近细胞进行精准交流的 通道。Yamashita 表示,她们过去也认为蛋白 质是可以在细胞间转移的,只是当时并没有想 到,细胞之间存在这样的联通管道。
Yamashita 等人发现的这种纳米管又给细 胞间的“神秘通道(cryptic conduits)”家 族增添了一名新的成员。在哺乳动物细胞之间 的、更长的通道似乎不仅可以传递分子信号, 也可以传递病毒颗粒、朊病毒、线粒体等更 大的“货物”。德国海德堡大学(University of Heidelberg in Germany)的神经生物学家 Amin Rustom 认为,这些研究成果表明,细胞 间存在着我们还不能充分认识和了解的沟通机 制。大约 20 年前,Rustom 当时还只是一名研 究生,当时他就发现了这些管道,这也让他成 为了发现细胞间管道的第一人。如果这些研究 成果得到证实,那么将彻底改变医学和生物学 的现状,因为这将彻底改变我们看待组织的方 式。
不过美国北卡罗来纳大学教堂山分校 (University of North Carolina in Chapel Hill)的细胞生物学家 Richard Cheney 则比较 谨慎。他一直关注这个研究方向,也曾经与 Rustom 的博士指导老师合作过。Cheney 指出,毫无疑问,这些细长的管道无处不在。可 问题是它们的作用是什么?是在细胞需要的时 候给其它细胞传递信息,还是开启一个传递物 质的通道?Cheney 认为,它们的作用应该还 是以传递信息为主。
需要指出的是,对这些管道开展科学研究 是非常困难的。要证明这些管道的存在就已经 非常不容易了,更别说确定它们的功能了。 Yamashita 等人采用遗传工程学的方法,并使 用已经被明确证明了功能的果蝇基因进行了实 验,结果发现这些管道可以在细胞间传递信 息。但是从事哺乳动物细胞间相关研究的科研 人员可就没有这么好的实验基础和条件了。目 前已经有许多科研人员错误地将细胞培养皿上 的划痕当作了细胞间的纳米管通道。迄今为 止,能够证明在哺乳动物细胞间也存在这些通 道的实验证据还非常少。
不过无论如何,这个研究领域最近已经成 为了一个热门的研究方向。英国葛兰素史克 制药公司(GlaxoSmithKline in Stevenage, UK)新兴研究平台部门的负责人 George Okafo 就是其中之一。Okafo 认为,细胞之间 的这些通道可以解释阿尔茨海默病、帕金森氏 症、疟疾、HIV 和朊病毒感染等难治性疾病的 相关机制。还有很多机制是我们传统药物没有 涉及到的,比如疾病在细胞之间传播的机制。
2016 年 9 月,Okafo 召集 GSK 的部分工作 人员和大约 40 名相关领域的科研人员一起召 开了一场小型会议。2017 年 3 月,NIH 也要求 那些研究细胞间通道对于应激细胞、或者肿瘤 细胞间的沟通有何作用的科研人员提交基金申 请,这些都说明细胞间的联通这个研究领域正 在逐渐兴起。今年 12 月,美国细胞生物学学(American Society for Cell Biology)还将在 他们今年的年会上设立一个专场讨论环节,以 讨论这方面的问题。
细长的通道
科研人员们早已发现,很多细胞表面都 会长出天线一样的突起,这些暂时出现的伪 足可以帮助细胞迁移。直到 1999 年,美国加 州大学旧金山分校(University of California, San Francisco)的细胞生物学家 Thomas Kornberg 的一个发现才让我们意识到,这些 “天线”可能还具有其它非常重要的作用。 Kornberg 当时正在研究蝇蛆(fly larvae)翅 膀的发育过程。他观察到翅芽(wing bud) 处长出了很多细丝状突起, 而且这些突起 全都朝向对于生长至关重要的信号中心 (signalling centre)。Kornberg 用“细胞 线(cytoneme)”这个词来形容这种结构。 他认为,我们过去发现的一些细胞间的沟通 (cellular chatter)可能就是这些细胞线的作 用,而过去我们认为那可能就是信号在细胞间 的弥散(diffusion)作用。Kornberg 提出的这 个观点在当时还是比较新颖的,接受这个观点 的人并不多,但是到了今天,这已经是被写进 教科书的理论了。
2004 年,两个科研团队都发现了在哺乳动 物细胞间存在纳米管的实验证据,而且这些管 道还可以在细胞间双向运送细胞器或囊泡等大 型“货物”。Rustom 研究的是体外培养的大 鼠细胞。有一次他在做实验时忘记了洗涤步 骤,结果在细胞间发现了细细的、笔直的管道 样结构。
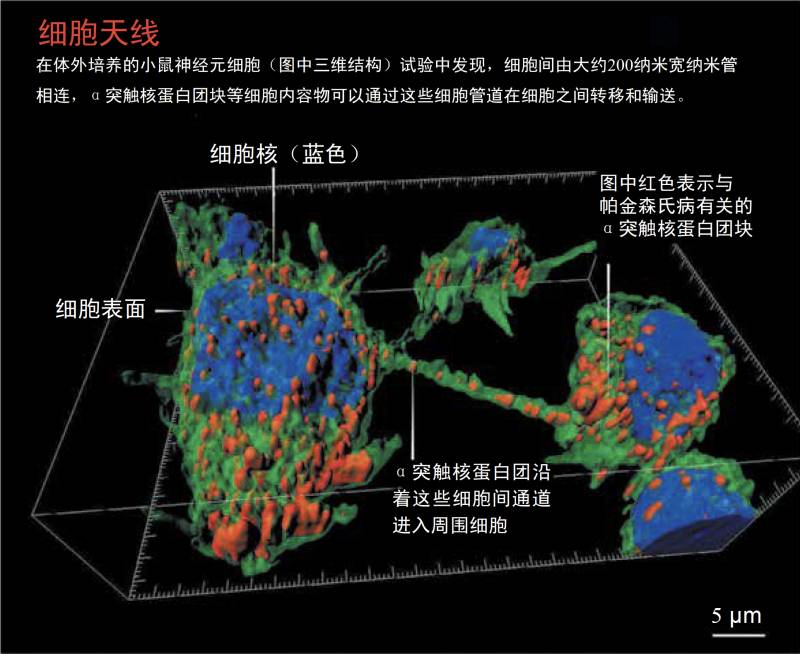
于是他和他当时在德国海德堡大学的导师 Hans-Hermann Gerdes 对细胞进行了遗传学 改造,使细胞可以表达荧光蛋白,结果真的看 到了这些荧光蛋白在细胞之间的“流动”。 他们将这个偶然的发现发表在了《科学》 (Science )杂志上,并且在文章中将这种细 胞间的通道称作“纳米管高速公路”。有些人 认为,他们之所以选择“纳米管”这个词,就 是为了蹭热点,因为当时“纳米”是非常流行 的一个概念。
英国帝国理工学院(Imperial College London) 的 Daniel Davis 也在 2004 年发 现了“细胞膜纳米管系统(memb r a n e nanotubes)”,即从细胞膜上向外伸展出的 细长的、长度可以达到细胞直径好几倍的管 道,而且这些管道在不同免疫细胞之间起到了 联通作用——一个细胞产生的脂质成分可以通 过这些管道到达其它细胞。Davis 认为,他们 之所以能够取得这一研究成果,是因为他们整 个团队都有不放过眼前任何一点蛛丝马迹,一 定要追查到底的科研精神。也就是说,他们不 仅发现了这些管道,而且会不断深挖下去。 Davis 团队又陆续发现了好几种不同的纳米管 道,其中一些能够转运线粒体和细胞内的囊泡等物质,还有一些管道甚至可以转运细菌这些 庞然大物。
还有一些实验室也在神经细胞、上皮细 胞、间充质干细胞、免疫细胞和肿瘤细胞等 不同的细胞之间发现了这种连接管道,也发 现了不同种类的管道。2010 年,Gerdes 等 人又发现,有一些管道在细胞间的缝隙连接 (gap junction)处中断了。我们知道,这些 缝隙连接可以让神经元细胞更快地传递神经电 信号,也可以传递肽段和 RNA 等生物分子。 Yamashita 怀疑,这些连接可能就是神经突触 (synapses)。她指出,神经元细胞可能首先 就是让它们的细胞膜突起,然后升级成更高级 的器官,比如形成突触等。通过这种方式,神 经元细胞获得了特定的功能。
大多数研究这些细胞通道的科研人员并不 太关注这些通道的起源和发育过程,他们更关 注的是这些通道对于人体健康和人类疾病的作 用和意义。到了 2015 年,德国海德堡大学的肿 瘤研究人员 Frank Winkler 终于得到了足够的证 据证明,这些细胞间的通道与人体疾病的确有 关系。与其他科研人员一样,Winkler 等人也 并不局限于这些细胞膜上的突起结构,他们对 神经胶质瘤(gliomas)细胞的生长也进行了 系统的研究。首先,将人体神经胶质瘤细胞注 入试验小鼠脑内,同时在小鼠头部也开一个骨 窗(用透明的玻璃取代了一部分头骨),然后 对小鼠颅内的肿瘤细胞直接进行活体观察。
结果发现,在这些肿瘤细胞不断向周围侵 蚀的过程中,第一步就是细胞膜往侵蚀方向形 成突起结构。更进一步的观察发现,这些突 起就是将细胞间的缝隙连接联系起来的细小管 道。彼此联系起来之后,这些细胞对放射线 照射的耐受能力获得大幅提高,这很有可能 就是因为这些通道的作用,让某种“抗性因 子”能够在不同的细胞之间交流和沟通。当放 射线照射杀死了这些肿瘤细胞之后,其中的 细胞核也会通过这些管道转移到其它地方, 形成新的肿瘤灶。研究人员在肿瘤病人的活 检标本中也发现了这些“肿瘤微管(tumour microtube)”,而且如果这些微管越长、越 密,那么患者的治疗效果就越差,预后也更 差。Winkler 认为,如果能够开发出这种微管 的抑制剂,那么这将会是一种疗效非常不错的 抗癌新药。紫杉醇(paclitaxel)的抗癌药理作 用可能就是抑制了这种微管。Winkler 等人为 一种药物申请了专利,该药物通过干扰神经胶 质瘤细胞形成微管,从而达到治疗神经胶质瘤 的效果。
这项工作需要很多想象力。Okafo 认为, 这是一篇非常伟大的论文。在此之前,对于 是否真的存在细胞间通道还存在不少的质疑。 但是科研人员们还不太清楚,Winkler 的研究 结论是否同样适用于其它细胞。我们知道, 多种脑细胞在生长和增殖时都可以伸出这种 细胞膜突起。Winkler 等人观察到的这些通 道要比 Gerdes 发现的常规意义上的细胞间纳 米管大许多。而与之前报道过的纳米管不同 的是,Winkler 发现的这些通道里含有微管 (microtubule),它可以利用纤丝让物质在细胞中移动。可是,Winkler 认为他们发现的这 些通道也属于纳米管样通道。他指出,在体外 培养环境下,这些通道不太可能长得和在体内 环境中一样大,而且他自己在实验中观察到的 通道就是大小不一的。Winkler 还回忆起 2013 年时与 Gerdes 进行的一场讨论,据 Winkler 介 绍,当时 Gerdes 觉得这才是我们这个领域一 直期待的研究成果。这也证实了 Winkler 之前 的想法。
在其他研究领域,这些纳米管也同样备 受关注。比如在美国罗格斯新泽西医学院 (Rutgers New Jersey Medical School in Newark)研究 HIV 病毒的 Eliseo Eugenin 就认 为,被 HIV 病毒感染的细胞也可以通过这些细 胞间的管道将病毒传播给其它健康细胞。但是 这种传播方式的效率不太高,所以并不会导致 病毒在短时间内大量扩增,以致这与感染初 发时的情况不太吻合。Eugenin 指出,这个时 候,数学公式是不起作用的。他认为,其他科 研人员不太认可纳米管是因为他们不相信细胞 之间一直在不停地进行物质,包括遗传物质的 交换。因为这样一来,整个关于细胞的概念就 被彻底颠覆了。所以大家都不接受细胞间纳米 管这个事实,除非我们先修改细胞的定义。
对立的观点
如果细胞的定义被颠覆了,那么对纳米 管的质疑声就会小很多。美国明尼苏达大学 (University of Minnesota in Minneapolis) 的肿瘤研究者 Emil Lou 就介绍了他们申请的课题。他们计划在人体肿瘤细胞上寻找这种纳米 管,并对其进行鉴定,可是却受到了评审专家 的嘲笑,因为他们根本就不相信存在这种纳米 管。
还有一部分研究人员认为只有在体外培养 的条件下才会出现这种纳米管。比如英国牛津 大学的免疫学家 Michael Dustin 就表示,他们 在培养皿里的确观察到了这种纳米管,但是他 们还是认为,如果是在紧实的器官里,是不会 存在这种结构的。比如,白细胞产生抗体时会 在培养皿里形成非常漂亮的、牛眼样的对称图 案,但是在体内时却是另外一副杂乱无章的、 混乱的样子。
除此之外,还有一些“机械方面的”问 题。有一些科研人员就认为,这些纳米管的两 端都是开口的,因为只有这样,物质才可以在 细胞间流通。比如美国霍华德休斯医院研究院 (Howard Hughes Medical Institute Janelia Research Campus in Ashburn, Virginia)的 细胞生物学家 Jennifer Lippincott-Schwartz 就 担心,这样一来,细胞彼此之间就会混为一 体,最终导致细胞融合。她认为,那些相信存 在纳米管的人首先需要向生物物理学家们咨询 一下。按照 Lippincott-Schwartz 的观点,细胞 间的膜突起只会有非常少的接触,使其刚刚碰 到细胞,并且其中的内容物被胞吞进去就够 了。
法国巴斯德研究所(Pasteur Institute in Paris)的细胞生物学家 Chiara Zurzolo 认为, 目前存在的这些不同的意见使这个研究领域变得更加的不严谨了。Zurzolo 就发现,朊病毒 和神经退行性变蛋白都可以通过这些纳米管来 传输。据 Zurzolo 介绍,很多论文都没有探讨 纳米管的末端是开放的,还是关闭的这个问 题,也没有涉及这些纳米管是否与物质在其中 的运输有关的问题。随着新报道的纳米管种类 的不断增多,命名的增多,我们更加难以探讨 这个问题了。所以 Zurzolo 认为,首先就必须 在命名上规范起来,因为现在的命名实在是太 乱了。
但是美国加州大学尔湾分校(University of California, Irvine)的细胞生物学家 Ian Smith 指出,我们现在最需要的就是对整个过 程有一个清晰的认识。然而,要获得一幅活细 胞的清晰图片非常困难。大部分显微镜技术都 不能获得清晰的、正在运输物质的纳米管的图 像,哪怕是对体外培养的细胞进行拍摄也是非 常困难的。Smith 正在开发一种可以观察细胞 纳米管的显微镜,他主要使用的是点阵光片显 微镜技术(lattice light-sheet microscopy)。 该技术可以将多层图像重建成为三维立体图 像。Smith 希望能够利用这种技术捕捉到物质 在细胞间转移的图像证据。同时他也承认,尽 管这个研究方向比较冒险,但是他还是愿意试 一试。
让 Lou 感到比较振奋的是,对于纳米管的 质疑声正在慢慢减少。最开始,人们都认为这 些“管道”只不过是显微镜下的假象。后来, 大家的说法慢慢开始变成——就算在培养皿里 有这些管道,也不代表它们就一定具备生物学 意义。再后来大家的态度又变成:“你很可能 弄错了吧。”不过 Lou 对这个研究方向还是非 常感兴趣的,他认为,我们应该非常认真地将 其当作一个治疗靶点来研究这个问题。不过五 年前他也没有这种想法。
原文检索:
Monya Baker. (2017) LINES OF COMMUNICATION. Nature , 549: 322-324.
(来源:生命奥秘 Oct 31, 2017)