过去12年肾癌药物治疗可谓波澜壮阔,从无到有,从少到多,经历细胞因子、靶向治疗和免疫治疗3个时代,免疫治疗方兴未艾,靶向治疗从1.0版要更迭到2.0版。本综述来自肿瘤神刊CA Cancer J Clin.展示肾癌当前治疗并展望未来方向。
肾癌是十大恶性肿瘤之一,占新发肿瘤3.7%,肾细胞癌(RCC)为最常见的类型占85%,中位诊断年龄64岁,男性多于女性。5年生存率有所提高,但整体预后仍较差,特别是分期较晚患者。过去12年,RCC经历细胞因子时代、靶向治疗时代和当下免疫治疗时代。本文总结RCC治疗现状,探讨未来的治疗趋势。
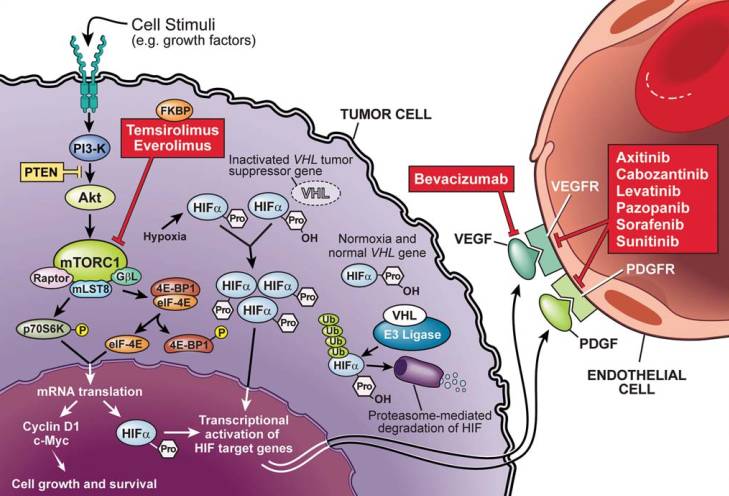
RCC为不同组织、分子和基因改变的一组疾病,主要包括透明细胞、乳头Ⅰ和Ⅱ型、嫌色细胞。透明细胞RCC(ccRCC)是最常见的类型,与VHL基因改变相关。VHL失活乏氧诱导因子(HIF)活性增加,VEGF和PDGF表达上调, mTOR通路可增强HIF活性。对VHL通路理解的深入促进了RCC靶向治疗发展。抑制VEGFR、PDGF、mTOR、MET和AXL等靶点药物陆续批准于RCC的治疗。RCC靶向治疗生物学通路见下图。
TNM分期是RCC最强预测因素之一,已更新至第8版。Ⅰ期5年无复发生存率超过92%,但Ⅱ和Ⅲ期患者术后仍有40%会复发转移。有多种模型用来预测术后结局。Mayo 诊所SSIGN评分系统包括肿瘤分期、大小、核分级和坏死,将ccRCC分低危、中危和高危三组,预后准确指数为0.78~0.86。UISS评分系统包括肾癌分期、Furhman分级和ECOG评分,预后准确指数0.79~0.86。因缺乏相应的治疗措施,预后评分系统对个体价值不高,主要用于临床研究。基因改变可提供额外的预后信息,但目前整合基因改变预后模型还不成熟。
靶向治疗时代前,细胞因子(IFN-α和IL-2)、激素(三苯氧胺、甲羟孕酮)、化疗(5-FU、阿霉素联合吉西他滨)或放疗的辅助治疗研究基本失败。
当前RCC领域中,大型、随机、安慰剂对照3期辅助研究有7项(见图1)。ARRURE研究纳入中高危RCC1943例(≥pT1b),任何病理类型(透明细胞占80%),分为舒尼替尼、索拉菲尼和安慰剂三组,治疗持续1年,中位DFS5.8年、6.1年和6.6年(无差异)。后续分析pT3、pT4或淋巴结阳性患者1069例,三组5年生存率亦无差异。S-TRAC是第2项研究,高风险ccRCC615例,1年舒尼替尼治疗较安慰剂提高DFS1.2年(6.8年和5.6年,HR0.76,P=0.03),目前两组中位
图1:肾癌辅助治疗3期研究一览表
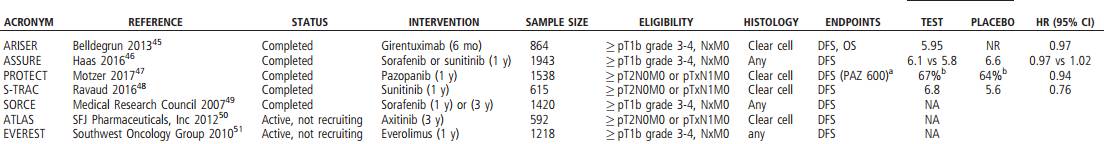
辅助治疗研究有那些启示呢?第一S-TRAC研究首先验证了辅助治疗是可延长DFS,与ARRURE研究比较,高复发风险和ccRCC可能是获益人群。第二重视剂量强度,PROTECT研究中,培唑帕尼800mg组DFS风险下降而600mg组DFS无差别,二次分析培唑帕尼剂量与DFS相关(HR0.58,P = .002),S-TRAC和 ASSURE中位治疗持续时间差不多,但是舒尼替尼相对剂量强度高88.4%对比71.4%。第三平衡安全性,S-TRAC获益时间比治疗时间略长。第四DFS延长能否转化为OS获益还不清楚。
CheckMate-025研究显示出PD1/L1抑制剂较标准治疗在耐受性和疗效上更好,纳武单抗、派姆单抗和atezolizumab正在进行辅助、新辅助、围手术期治疗的研究。
预后模型
初诊时晚期患者占30%,治愈性治疗三分一会出现复发或转移。在mRCC中,预后风险模型有助于患者咨询、危险分层和治疗选择。MSKCC评分建立在细胞因子时代,包括体力状态、乳酸脱氢酶、血红蛋白、血钙和自诊断到药物治疗时间,分为低危(0个)、中危(1~2个)、高危(3~5个),相对应OS为30个月、14个月和5个月。靶向治疗时代,IMDC评分包括MSKCC预后因素中4个(除外LDH),又纳入血小板和中性粒细胞计数,低危、中危和高危组中位OS分别为35.3个月、16.6个月和5.4个月。
手术
细胞因子时代,2项随机研究支持转移性疾病可行肾切除术,246例接受IFN-a治疗mRCC,肾切除将OS从8个月延长至11个月。靶向治疗时代肾切除术应用在下降,纳入12项研究近4000例患者的meta分析,肾切除可带来OS获益。目前肾切术适用于PS评分好、无或轻微疾病相关症状,转移负荷低、手术能显著降低肿瘤负荷的患者。
TKI前时代,手术切除转移灶是合理和有效的,回顾性分析278例mRCC,治愈性转移灶切除5年生存率明显增加(44%对比14%)。转移灶切除术5年DFS延长因素有肾切除至转移灶发现≥1年、单发转移、年龄≤60岁。
一线治疗
舒尼替尼、培唑帕尼、贝伐珠单抗及用于高危患者替西莫罗斯推荐用于透明细胞为主型的RCC一线治疗。除培唑帕尼后,其他药物均与IFN-α比较。非劣效性COMPARZ研究显示培唑帕尼与舒尼替尼疗效相近,但QOL上支持培唑帕尼。PRISCES研究患者较舒尼替尼更倾向于选择帕唑帕尼。上述药物PFS 5.5~11个月,OS23~26个月。新的两个TKI阿昔替尼和tivozanib,较索拉菲尼显著延长PFS。阿昔替尼对比索拉菲尼的3期研究(n=288),PFS10.1个月对6.5个月(HR0.77,P=.038),ORR32%对比15%,但OS无差异。Tivozanib对比索拉菲尼一线治疗ccRCC(n=517),中位PFS11.9个月对比9.1个月(HR0.80,P=.04)。目前两个药物均未获得FDA批准用于一线治疗。
二线及后线治疗
至2015年,二线推荐药物为依维莫司(RECORD-1,2008)和阿昔替尼(AXIS,2011)。RECORD-1研究抗血管生成治疗透明细胞为主型RCC失败的患者(n=410),依维莫司和安慰剂中位PFS4.0个月对比1.9个月(HR0.30),ORR1%对比0%,更新OS数据(14.8个月和14.4个月)无差别。阿昔替尼与VEGFR结合力是既往药物的50~450倍。AXIS研究中,阿昔替尼对比索拉菲尼二线治疗723例转移性ccRCC,既往舒尼替尼治疗占54%、细胞因子治疗占三分之一,中位PFS 6.7个月和4.7个月(HR,0.67),ORR19.4%对比9.4%(p<0.01),预设亚组分析中,既往接受舒尼替尼或细胞因子治疗患者,阿昔替尼疗效均优于索拉菲尼。
2016年伴随纳武单抗、卡博替尼的获批和乐伐替尼/依维莫司研究公布,mRCC二线治疗发生巨大变化。这些研究主要是ccRCC,对照组均为依维莫司。卡博替尼同时抑制VEGFRs、MET和AXL,克服血管靶向药物的耐药,3期的METEOR研究(n=658),一线VEFR TKI治疗进展的ccRCC,卡博替尼和依维莫司中位PFS7.4个月对比3.8个月(HR0.58),ORR21%对比5%,OS21.4个月对比16.5个月(HR0.66)。另外卡博替尼对比舒尼替尼一线治疗的2期CABOSUN研究(n=157),入组未经治疗中高危ccRCC,卡博替尼的PFS更长(8.2个月对比5.6个月,HR0.66),提示联合抑制AXL和MET在治疗RCC上有优势。
纳武单抗对比依维莫司二线或三线mRCC的CheckMate-025研究(n=821例),OS延长6个月(HR0.73,25.0个月对比19.6个月),疗效与PD-L1表达无关,ORR25%对比5%,但两组PFS无差异(4.6个月对比4.4个月),安全性和QOL数据支持纳武单抗。多靶点TKI乐伐替尼,联合mTOR抑制剂二线治疗的PFS12.8个月,OS25.5个月均为史上最好数据,但因联合治疗毒性大治疗中断率高,FDA要求进行14/5mg对比18mg/5mg的研究。
非透明细胞RCC(nccRCC)异质性强,具有不同分子、组织学特征和预后,包括乳头状RCC、嫌色细胞RCC、集合管癌、肾髓质癌等。对ccRCC有效药物可能对nccRCC无效,但是总体治疗选择与ccRCC相同的药物。
舒尼替尼对比依维莫司有两项2期随机研究ASPEN和ESPN,共176例(乳头状RCC占55%),另一个2期研究INTORSECT包含10% nccRCC,总体上舒尼替尼优于依维莫司。因nccRCC无标准治疗,可选择抗VEGF抑制剂,因预后较差建议加入临床试验。
化疗对于集合管RCC和肾髓质癌有效,遗传性1型和部分散发乳头状RCC伴有MET基因的改变,MET抑制剂治疗有效。免疫治疗研究多将nccRCC排除在外,101例nccRCC患者PD-L1阳性率为10.9%,回顾纳武单抗后线治疗23例mccRCC,ORR29% ,PFS4.2个月。
二代抗VEGF靶向治疗、免疫药物和联合用药将改变RCC未来的治疗。临床前研究,VEGF TKI可增强肿瘤微环境的抗肿瘤免疫效应,VEGF TKIs联合免疫检查点抑制剂策有广阔的应用前景,阿昔替尼+pembrolizumab、阿昔替尼+avelumab、乐伐替尼+pembrolizumab的Ⅰ或Ⅱ期研究,ORR32%~67%, AEs可管理,目前3期研究正在进行。除了免疫检查点抑制剂,其他新型免疫药物如T细胞激动剂、肿瘤疫苗、调节T细胞抑制剂正在研发。合理选择患者增强疗效需要更好的生物标志物和预测模型,随着NGS对RCC分子亚型认识深入,RCC治疗会朝着精准医学方向发展。
Treatment of renal cell carcinoma: Current status and future directions.CA Cancer J Clin.2017 Sep 29.
28个肿瘤相关临床试验招募患者
点击下方图片即可查看详情
















