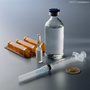
全球核素新药陆续上市,国内影像设备及核素药物市场提升空间大。全球核素药物市场规模约为100亿美元,保持10%左右的增长。随着国外重磅核素新药上市,全球市场有望迎来新一轮快速增长。前列腺癌治疗核素氯化镭[223](Xofigo)上市第3年就实现3.5亿美元销售额,有望成为全球第一个销售额突破10亿美元的重磅核素药物。核素抗体偶联药物的问世能够实现肿瘤的可视化诊断和治疗,而且更换搭配药物就有望获得新适应症,或将推动全球核素药物高速扩容。2016药物市场规模约为40亿,2020年有望达到100亿。我国核素药物市场规模偏小,一方面是缺少新产品,另一方面是核素所需的影像设备偏少。如我国每百万人的PET/CT保有量仅为0.17台,远低于全球平均水平0.7和发达国家平均水平2.0以上,随着成本降低、适应症扩张、使用频率增加,保守估计还有4-10倍的增长空间,也必将推动全国核素药物市场发展。持续整合核素产业链,产品梯队齐全+核药房网络布局打造核素药物龙头企业。东诚药业通过并购形成了初步的核素诊断+治疗产品线。从产品来看,东诚药业的核素药物产品线齐全,现有产品(云克注射液、氟[18]-FDG)稳定增长+在研重磅品种获批(铼[188]-HEDP注射液、氟[18]-AV45)+外延并购预期,能够保证核素药物的产品梯队;从渠道来看,东诚药业的安迪科+GMS整合提升核药房盈利能力,逐步建成覆盖全国的核药房网络掌控终端。丰富的产品梯队+广泛的营销渠道将推动公司的核素药物业务保持快速增长,具备发展成全国核素药物龙头的潜力。
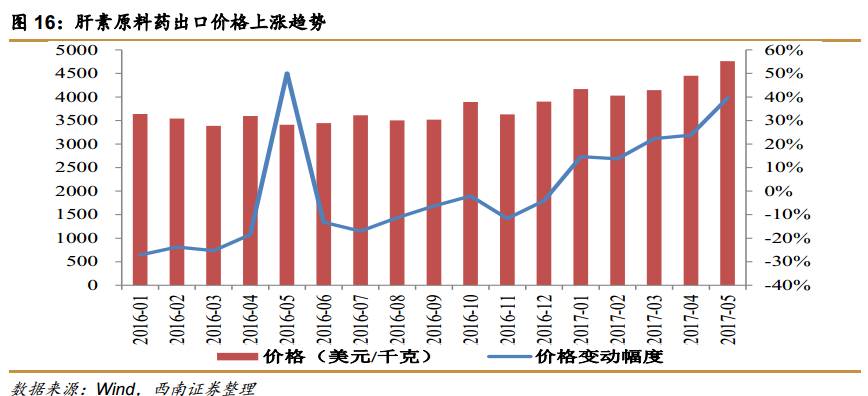
肝素原料药触底反弹,价格有望持续提升。本轮肝素原料药行情的主要推动因素是下游制剂企业的补库存需求和上游原材料涨价,最终导致肝素原料药价格提升。肝素原料药价格在2016年中开始缓慢回升,4月份开始提价速度加快。2017年5月份价格同比提升40%,年初至今的平均价格与2016年同期相比提升23%。肝素原料药价格仍然存在持续上涨的预期,有望显著增厚公司业绩。
盈利预测与投资建议。考虑增发摊薄(拟发行6075万股,占公司总股本的8.6%,作价8.2亿),预计公司2017-2019年归母净利润分别为2.2亿、3.8亿、4.7亿,对应PE分别为50倍、29倍、23倍。如考虑安迪科在2017年全年并表,预计2017-2019年备考净利润分别为2.8亿、3.8亿、4.7亿,对应PE分别为39倍、29倍、23倍。预计2018年东诚药业的归母净利润将达到3.8亿,同比增长35%,考虑核素药物的稀缺性和持续外延并购预期,我们认为公司应该享受一定的估值溢价,给予公司2018年40倍PE,对应目标价19.60元。
风险提示:并购标的收购进度及业绩或不及预期;原料药出口或低于预期。
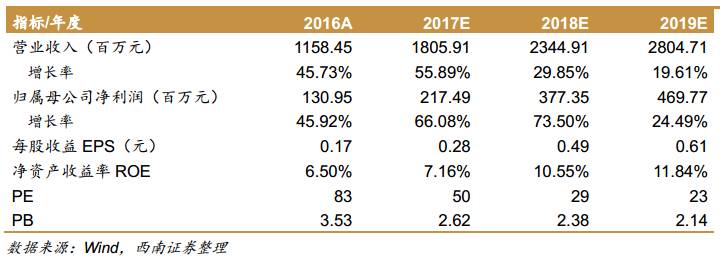
1全球核素重磅新药陆续上市,市场高速成长
全球核素药物市场规模接近100亿美元,市场增速超过10%,其中核素诊断药物和核素治疗药物之比约为8:2。核素诊断药物是前期市场增长的主要原因,近年来随着核素治疗药物上市和更多在研产品陆续获批,将成为市场扩容的主要驱动力。
从全球核素药物发展历史来看,2004年之前比较平缓,但随着肿瘤诊断药物氟[18]脱氧葡萄糖注射液(以下简称为氟[18]-FDG)的兴起,全球市场进入了一轮快速发展期。2013年前列腺癌治疗核素氯化镭[223](商品名Xofigo)上市快速放量,随着其他核素治疗药物尤其是核素抗体偶联药物的兴起,全球核素药物市场将进入高速成长期。
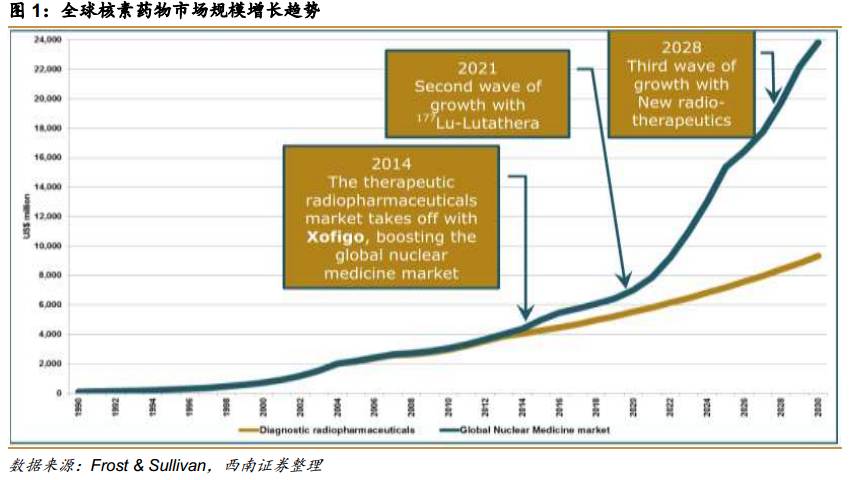
Xofigo有望成为全球第一个销售额超过10亿美元的核素药物,吸引更多药企进入核素药物市场。Xofigo主要用于治疗晚期骨转移前列腺癌,可以使患者总生存期提高3个月,而且安全性很好。Xofigo于2013年陆续获得美国和欧盟批准上市,目前正在我国做临床试验。Xofigo于2014年正式上市,当年即实现接近1亿美元销售额,2016年销售额约为3.5亿美元,预计2020年有望突破10亿美元销售。Xofigo还在开展临床试验探索其治疗乳腺癌的疗效,未来有望扩大到其他适应症。Xofigo需要使用放射性同位素镭[223],使用价格昂贵,是全球治疗费用最高的5种抗癌药物之一。高单价和潜力市场大使得Xofigo有望成为全球首款10亿美元级别的重磅核素药物,吸引更多制药企业进入核素药物市场。

近年来核素单抗偶联药物的研究突飞猛进,产品有望陆续获批,为核素药物市场带来新增量。单抗能够特异性结合肿瘤标志物,使得偶联药物在肿瘤所在部位进行聚集,如偶联放射性核素,则可通过影像设备进行可视化分析,从而确定肿瘤位置、了解肿瘤进程、评估治疗效果和预后;如偶联治疗性核素,则可通过核素的放射性作用在局部杀伤肿瘤细胞。核素单抗偶联药物不仅能够实现肿瘤诊断、治疗、预后全程的可视化监测,而且还能够充分发挥核素的放射性杀伤作用,治疗作用显著。
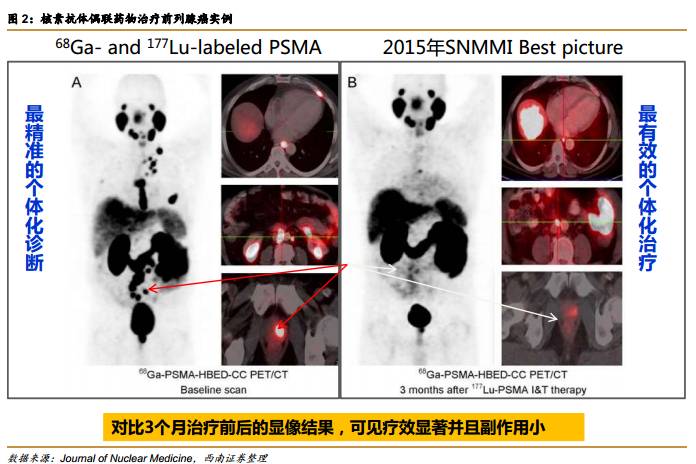
Ga[68]标记的PSMA于2012年首次被应用于前列腺患者诊断,能够弥补氟[18]-FDG诊断前列腺癌的假阴性等缺陷,能够更准确地发现和诊断前列腺癌。2017年3月欧洲核医学协会(EANM)联合核医学和分子影像学学会(SNMMI)共同发布了前列腺癌Ga[68]-PSMA的PET/CT检查指南,为前列腺癌的PET/CT检查提出诊疗建议。
Lu[177]标记的PSMA对前列腺癌患者的疗效良好。临床数据显示了145名前列腺癌患者接受治疗后,共99例患者生化缓解,仅有18例患者发生了3-4级的血液毒性反应,45%的患者是在全部疗程结束后达到生化缓解,显示Lu[177]-PSMA治疗对前列腺癌患者具有较高的疗效。
核素药物在肿瘤诊疗中发挥的作用越来越大,如Ga[68]-PSMA可用于前列腺癌的精确诊断,Lu[177]-PSMA可用于前列腺癌的放射性治疗,另外还有In[111]-PSMA提供手术引导,从而实现了诊疗一体化,为前列腺癌的临床诊疗决策提供了新选择,代表着核素药物发展的未来趋势。
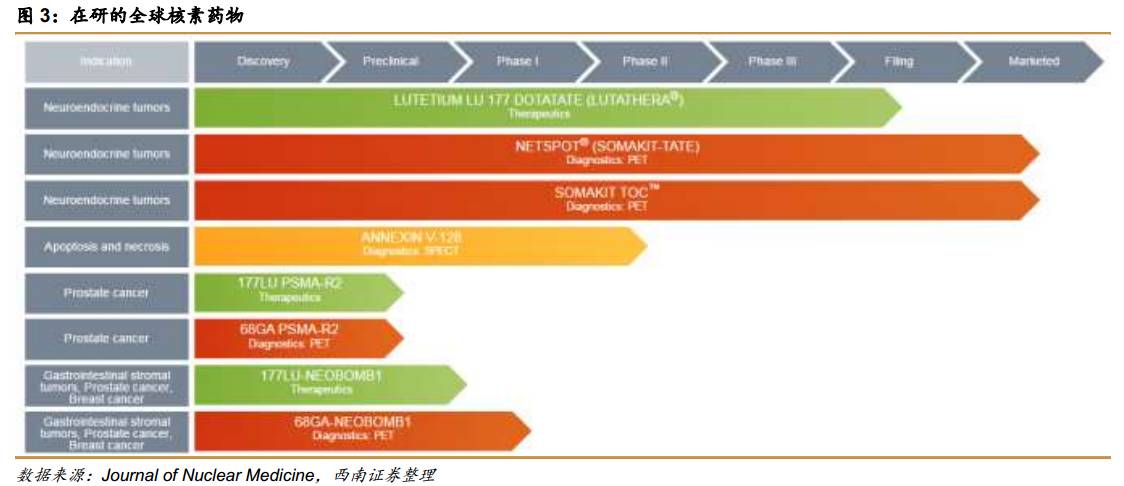
Ga[68]-PSMA(已上市)和Lu[177]-PSMA(生产申报阶段)证明了核素药物在肿瘤诊断和治疗中的作用机制,只要更换标记的单抗分子就可以开发其他适应症,如AAA就将PSMA换成NeoBOMB1,正在对Ga[68]-NeoBOMB1和Lu[177]-NeoBOMB1进行研发,目标适应症包括胃肠道间质肿瘤、前列腺癌和乳腺癌。
因此核素抗体偶联药物的问世为核素药物的发展打开了新的空间,相关诊疗机制得到证实,未来如更换放射性核素或单抗分子就有可能开发出新的适应症,新药有望陆续上市,推动整个核素药物市场扩容。
2国内影像设备数量增加推动核素药物市场扩容
2013年中国的核素药物市场规模20亿,2016年市场规模约为40亿,预计2020年市场规模将突破100亿,保持25%的复合增速。PDB样本医院的数据显示2016年核素药物的销售额达到2.2亿,同比增长18%。
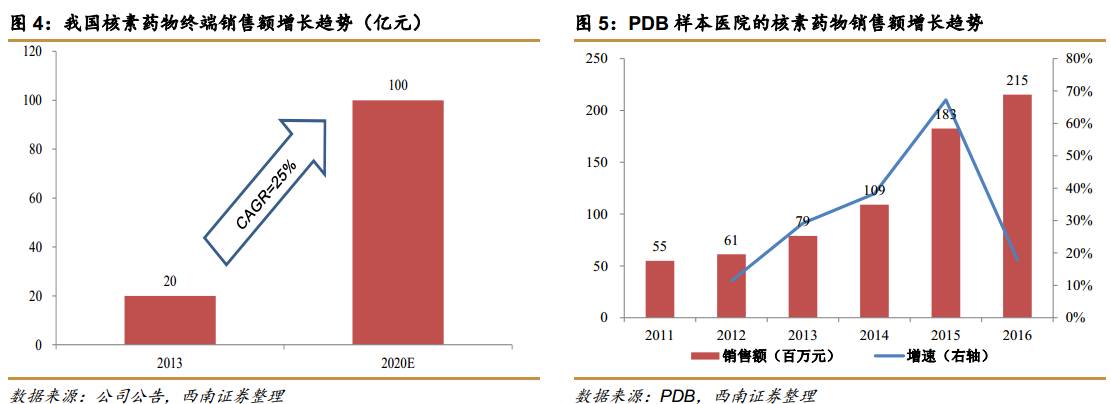
我国的核素药物市场远低于发达国家,无论是总体市场规模还是人均支出都远低于美国。我国的人均核素药物支出从2012年的1.8亿增加到2016年的2.8亿,增幅达到56%,但仅为美国的1/19,还有巨大的增长空间。
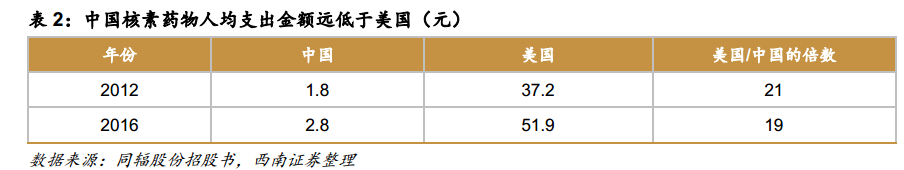
中国的核素药物发展落后于发达国家的原因主要是因为核素药物配合使用的影像设备配置数量少。以PET/CT为例,全球每百万人平均的设备保有量为0.7台,丹麦达到5.32台为全球最高水平,中国大陆仅为0.17台,与全球平均水平相比还有巨大的差距。
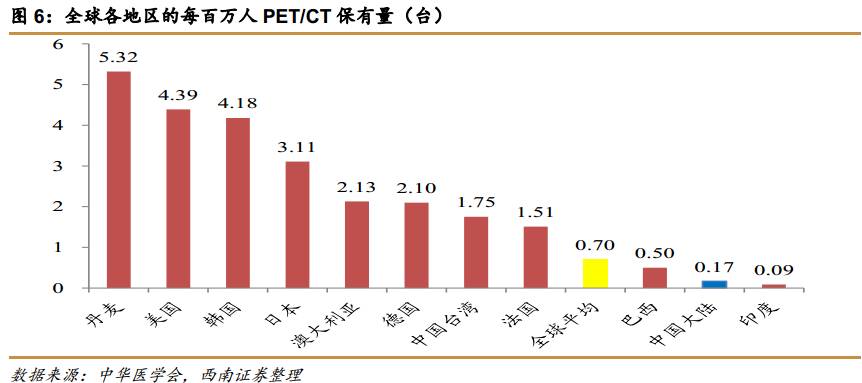
近年来,中国的PET/CT数量稳步增长,从2009年的98台增长到2015年的240台,保持16%的复合增速,检查例数从2009年的增长至2015年的47万例,保持20%的复合增速。PET/CT检查需要使用氟[18]-FDG药物,早期医院以自制为主,但一般仅供一家医院使用规模小而成本高。随着市场化发展,越来越多的医院选择从企业采购,2015年对外采购的比例提升至65%。
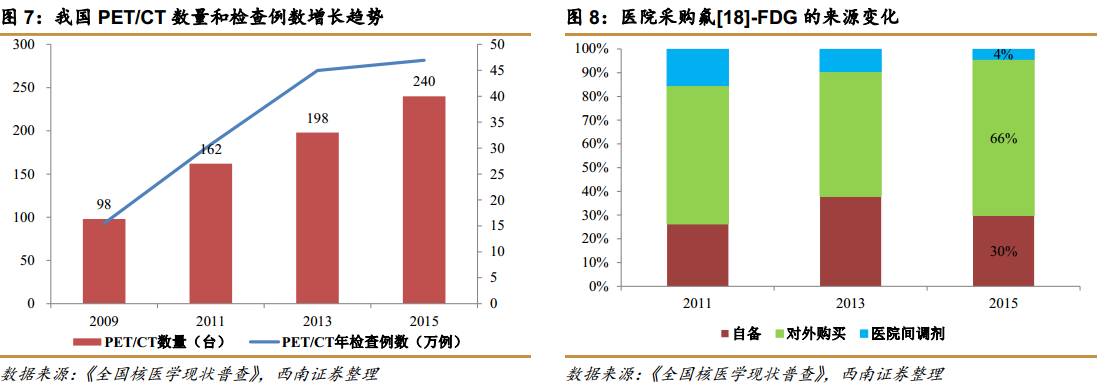
PET/CT与早期的MRI和CT类似,由于价格昂贵和使用范围少还未获得大范围推广。但是随着技术进步和国产化带来成本降低,PET/CT的价格也将会逐步下降,且新的核素药物陆续上市和检查项目增多,也将推动终端需求增长,最终使得PET/CT的配备数量和药品市场规模扩大。
以MRI为例,2010年我国的MRI数量约500台,2012年已经超过1000台,2014年超过6000台,预计2020年将达到16000台。CT的保有量在2015年已经接近20000台。随着CT和MRI的保有量增加、适应症拓展、使用频率提升,造影剂市场也保持高速增长,PDB样本医院的销售额从2005年的4亿增长到2016年的23.8亿,保持18%的复合增速。
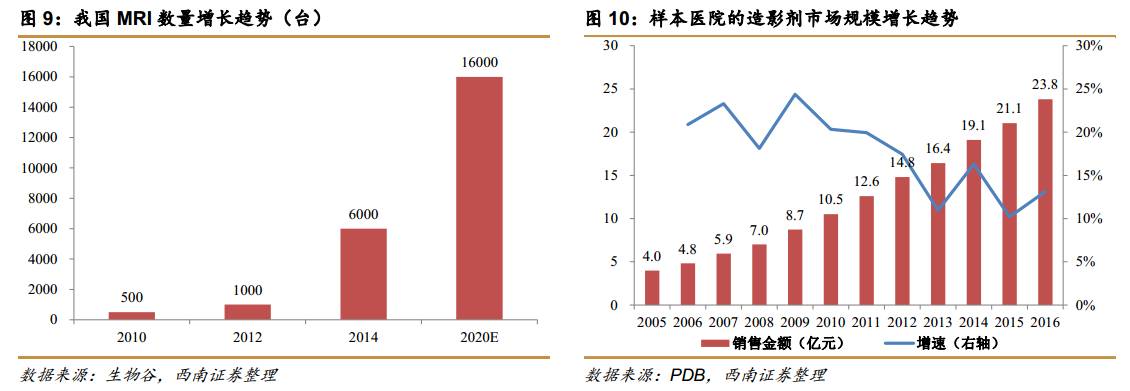
我国的核素药物市场潜力巨大,目前主要是受限于PET/CT等相关影像设备的数量偏少,但参照MRI和CT的路径,随着成本降低和检查项目增多,市场保有量将会大幅度提升。以PET/CT为例,我国的每百万人保有量仅为0.17台,低于全球0.7台的平均水平,更低于发达国家2.0台的水平,保守估计未来还有4-10倍的增长空间,必将带动核素药物持续扩容。
3产品梯队+营销网络打造全国核素药物龙头
2015年公司制定了大力发展核素药物的战略,2015-2017每年启动一项核素药物并购,目前已经形成了初步的核素药物产品线:核素诊断药物包括锝[99]、碘[125]密封籽源、氟[18]-FDG、C[14]等产品,治疗性药物包括云克注射液、铼[188]-HEDP注射液。
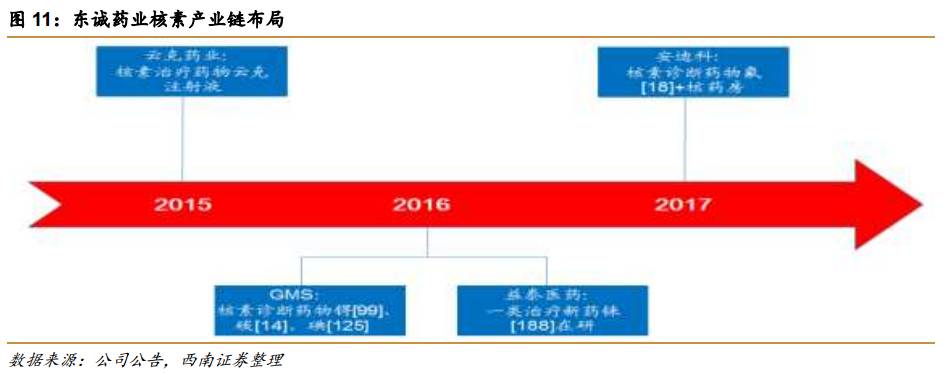
3.1内生+外延拓展产品线,重磅品种陆续上市
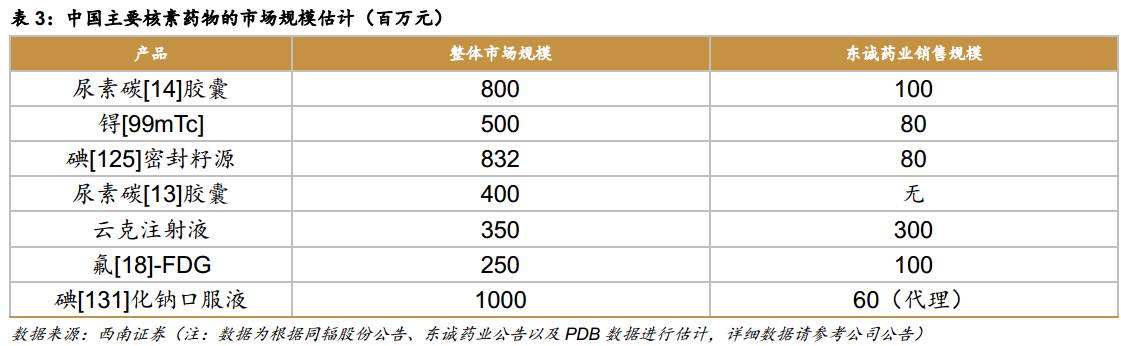
从全国来看,核素诊断药物销售规模较大的品种包括尿素碳[14]胶囊、尿素碳[13]胶囊、碘[125]密封籽源、碘[131]化钠口服液、氟[18]-FDG、锝[99mTc]、云克注射液等产品。东诚药业的核素药物主要是已形成销售规模的氟[18]-FDG和云克注射液,其他产品销售额较小。未来公司将通过内生和外延持续扩大核素药物的销售额。
云克注射液:逐步走向普药,下沉基层终端
云克注射液全名为锝[99Tc]亚甲基二膦酸盐注射液,是云克药业(东诚药业持股52.11%)的独家品种,也是国内首个用于类风湿性关节炎(RA)临床治疗的核素药物。
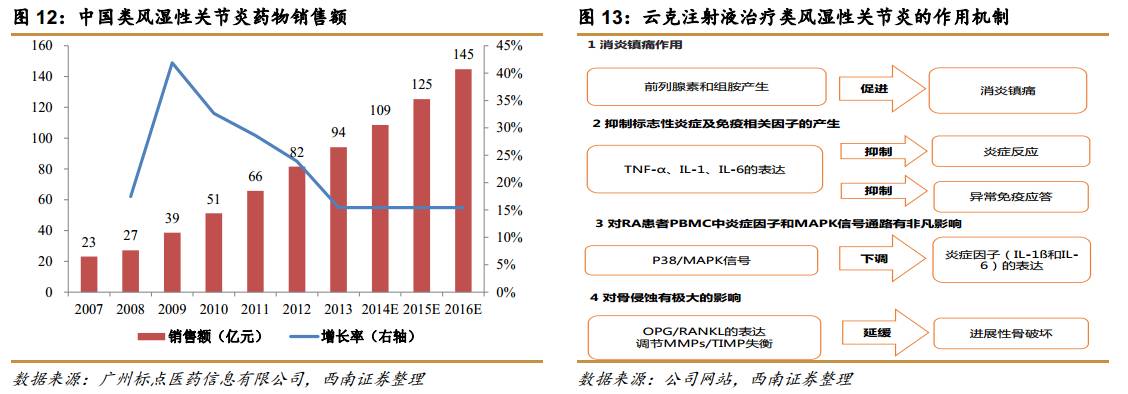
2013 年我国类风湿性关节炎药物销售额为94亿元,同比增长15%,预计2016年销售额超过120亿。我国类风湿性关节炎的患病率为0.32%-0.36%,按 13.7亿人口测算,预计我国类风湿性关节炎患者约 450万人。如治疗渗透率达到50%,按照人均2万元测算,则未来市场空间超过450亿。
云克注射液的有效成分是人工微量元素锝[99Tc]与亚甲基二膦酸盐形成的络合物,能通过独特的免疫调节机制,降低IL-1、IL-6、TNF-α、MMP3等多种标志性细胞因子水平,抑制破骨细胞活性,同时促进成骨细胞分裂增殖,从而修复骨侵蚀,恢复关节功能。与其他类风湿性关节炎治疗药物相比,云克注射液具有明显优势。云克注射液不仅具有非甾体消炎药的消炎镇痛作用,还具有激素和抗风湿药的免疫抑制作用,且毒副作用少而轻微,也无致癌倾向。10多年来的临床应用表明云克注射液治疗类风湿性关节炎的总有效率超过85%。
云克注射液目前主要有两种销售途径:1)以核医学技术的形式在医院的核医学科报销。我国的核医学科室从2011年的767家提高了2015年的891家,云克注射液已经覆盖了绝大多数核医学科,主要增量来自于提高在单个核医学科的销售量。2)以普通药物的形式销售。云克注射液含有的锝[99Tc]是锝元素最稳定的同位素之一,半衰期长达二十一万多年,药品的放射性剂量水平低于天然本底辐射,因此环保部和CFDA都批准云克注射液可以按照普通处方药进行使用和管理。目前云克注射液已经进入了北京、广东等少数省份的地方医保目录,在上海是以自费药物的形式销售(价格为106元,远高于其他省市的50-75元)。随着云克注射液以普通处方药的形式在更多省市争取到自费药或是医保药的身份,将逐步从现在的三甲医院为主向基层延伸,推动销量快速增长。
氟[18]-FDG:PET/CT数量和使用频率增加,核药房快速扩张
氟[18]-FDG广泛用于PET/CT显像诊断,可早期发现全身肿瘤病灶,为临床治疗提供参考依据。氟[18]-FDG的半衰期约为109.77分钟,完成配置后必须尽快运送到医院才能使用,核药房的数量成为氟[18]-FDG快速放量的瓶颈。
短期来看,氟[18]-FDG的增长主要来自于核药房的快速扩张。安迪科拥有7家核药房,GMS拥有7家核药房,双方资源共享能够使得氟[18]-FDG覆盖的医院终端大幅度增加,且安迪科还有十多家核药房处于在建和拟建阶段,预计5年后将建成覆盖全国的核药房网络,从而推动氟[18]-FDG销售。
长期来看,氟[18]-FDG的销售取决于我国PET/CT的保有量。我国PET/CT的年诊疗人次总数约47万例,渗透率仅0.2%左右,远低于发达国家2%的渗透率,主要是因为我国PET/CT数量少仅355台,每百万人口保有量为0.25台,而发达国家平均每百万人保有量超过2台。如我国的每百万人保有量达到2台,市场规模将扩大7倍。
碘[125]密封籽源和尿素碳[14]胶囊:销售模式改革提升盈利能力
GMS的子公司上海欣科拥有碘[125]密封籽源和尿素碳[14]胶囊的生产批文。碘[125]密封籽源适用于浅表、胸腹腔内的肿瘤(如头颈部肿瘤、肺癌、胰腺癌、早期前列腺癌)、以及经放射线外照射治疗残留的肿瘤以及复发的肿瘤。云克药业的碘[125]密封籽源产能不足而GMS的碘[125]密封籽源交由同辐代理销售,盈利能力未能充分体现。随着公司将云克药业和GMS的销售渠道整合,有望实现收入和利润同步高增长。
尿素碳[14]胶囊可用于幽门螺杆菌检测,需要配合试剂盒使用。GMS只有尿素碳[14]胶囊的批文,配套检测试剂盒还在研发中,预计2018-2019年有望上市。目前GMS的尿素碳[14]胶囊是为同辐代工生产,价格偏低且盈利能力差,转为代理后有望提升盈利能力,如检测试剂盒获批或将迎来爆发式增长。
在研产品:核素新药研发领先,或将诞生10亿级别重磅药品
东诚药业旗下的益泰医药、GMS等核素药物企业拥有众多核素药物研发项目,包括铼[188]-HEDP注射液、氟[18]-AV45等重磅产品。
铼[188]-HEDP注射液是益泰医药研发的1类新药,目前处于临床IIb阶段。铼[188]是性质优良的治疗性核素,发射的β射线的能量和平均穿透深度适合骨转移灶的缓解治疗,同时伴生的γ射线适于显像,便于临床及治疗时观察药物代谢情况和疗效评价。铼[188]能与HEDP形成稳定的螯合物浓集于骨组织,特别浓集于肿瘤的骨转移灶,从而达到治疗的作用。
铼[188Re]-HEDP注射液可用在多种肿瘤骨转移的治疗,以前列腺癌骨转移治疗为例。据全国肿瘤登记中心发布的数据显示,2015年全国前列腺癌的新发病人数为6万,前列腺癌的骨转移率约为70%,前列腺癌骨转移患者的中位生存期约为40个月,据此推算前列腺癌骨转移患者数量超过12万人。此外,前列腺癌的发病率年均增长12%。保守估计铼[188Re]-HEDP注射液上市后的目标患者将超过10万人。按照15%的临床使用率、8000元/支(国产同类产品氯化锶为1.5万元/支,国外同类产品氯化镭为8万元/支)的单价和人均使用4支计算,上市5年后销售额有望突破4亿元。如考虑其他肿瘤骨转移治疗,未来市场空间突破10亿是大概率事件。
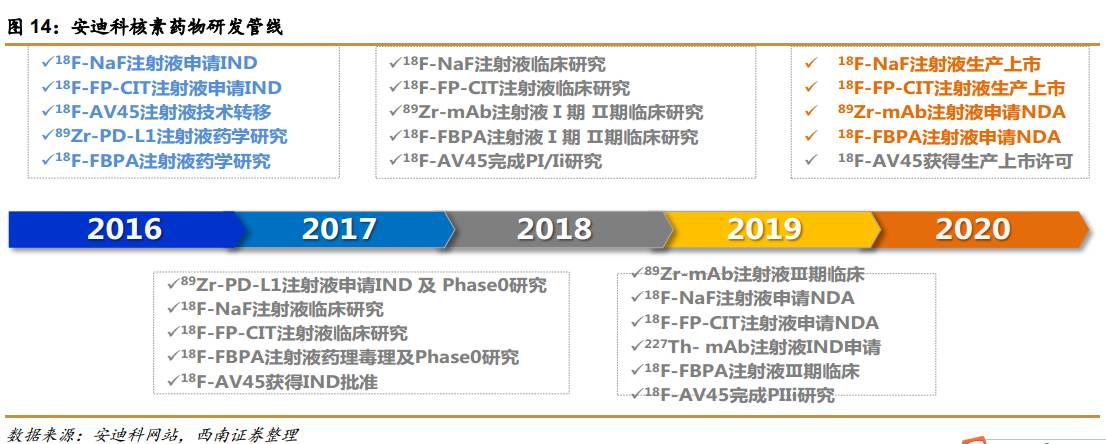
安迪科已有多个项目处于立项阶段,重点开发氟[18]的相关产品,能与现有的氟[18]-FDG形成协同效应。安迪科还与国际制药巨头礼来进行合作,获得了礼来的氟[18]-AV45(老年痴呆检测)在国内的技术转移,未来将负责其在国内的注册申请、生产和销售。安迪科与礼来的合作仅仅是个开始,未来或将承接更多核素药物转移至国内。由于核素药物半衰期短,一般都需要在医院周边生产,且需要大量的核药房布局才能实现放量。目前国内只有同辐和东诚具备条件,考虑到东诚作为民营企业的机制更灵活且效率更高,预计陆续会有更多国外企业与东诚合作将核素药物新药引入国内。
总体来看,东诚药业目前已经形成了初步的核素诊断+治疗药物布局,短期看云克注射液和氟[18]-FDG的持续放量,中期看碘[125]密封籽源和尿素碳[14]胶囊的销售变革带来收入和利润高速增长,长期看在研的重磅产品铼[188Re]-HEDP注射液等陆续获批及国外新药引进。而且东诚还存在持续并购预期,或通过并购对核素药物行业进行持续整合,将更多大品种纳入其核素产业链布局。
3.2打造全国核药房网络,掌控市场终端
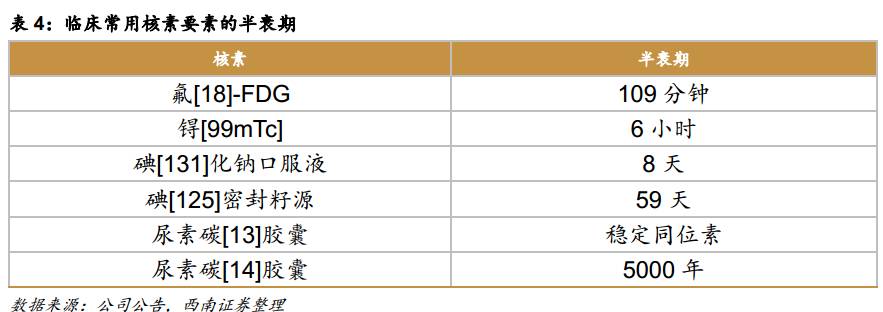
由于临床上应用的大部分核素药物的半衰期较短,与普通药品相比保存时间有限,尤其是氟[18]-FDG和锝[99mTc]的半衰期分别为109分钟和6小时。因此必须即用即制,不能在传统企业生产,必须在核药房生产后立刻安排车辆运送到医院使用。在核素药物市场领域,拥有核药房就相当于掌控了市场终端,能够获得明显的竞争优势。
GMS和安迪科都有各自的核药房,GMS和安迪科目前各有7个,另外安迪科还有约20个核药房在建和拟建。未来安迪科将在黑河-腾冲线的东侧建立覆盖全国的短半衰期和长半衰期核药房布局,抢占市场危机。
短期来看,GMS核药房的锝[99mTc]与安迪科核药房的氟[18]-FDG能够形成互补,双方通过资源共享未来都能满足这两种核素药物的生产,从而快速扩大规模和提升盈利能力。长期来看,全国性的核药房网络完成布局完成后,东诚药业降掌控市场终端,能够推动公司的多个核素药物快速放量。
我们认为:从产品来看,东诚药业的核素药物产品线齐全,现有产品稳定增长+在研重磅品种获批+外延并购预期,能够保证核素药物的产品梯队;从渠道来看,东诚药业的安迪科+GMS整合提升核药房盈利能力,逐步建成覆盖全国的核药房网络掌控终端。丰富的产品梯队+广泛的营销渠道将推动公司的核素药物业务保持快速增长,具备发展成全国核素药物龙头的潜力。
4肝素原料药持续提价增厚业绩
我国肝素钠原料药主要是出口到欧美发达国家,供应量占全球需求量的50%以上。2010年我国肝素钠原料药销量为19.2万亿单位,占全球需求量的62%,其中出口18.4万亿单位,出口占比高达96%。
最近几年肝素原料药产业整体下滑,主要原因在于我国主要原料药生产企业自2010年起进行了大规模扩产,在2014年左右达到产能高峰期,供应量持续增长,供给端增速超过需求端,导致肝素出口价格持续下行。2010年最高价达到11154美元/千克,最新单价仅为3596美元/千克。
由于生猪出栏量降低导致猪价上涨,猪小肠-肝素粗品-肝素原料药整个产业链的价格都出现上行,且环保压力加大导致部分产能退出进一步加剧了肝素原料药的涨价趋势。2017年以来肝素原料药的价格持续上涨,2017年1-5月的平均价格上涨23%,且涨幅逐月提升,5月份同比上涨40%,预计涨价趋势仍将持续,有望推动肝素原料药业务盈利能力提升。
5盈利预测与投资建议
假设1:预计2017年肝素原料药销量不变但价格提升30%,毛利率提升至35%;
假设2:假设安迪科现金收购部分预计在2017年8月完成,股权收购部分在2017年底完成,预计2017-2018年分别并表25%和100%,2017-2019年销量增速分别为16%、18%、20%;
假设3:2017-2019年云克药业保持20%的销量增速。
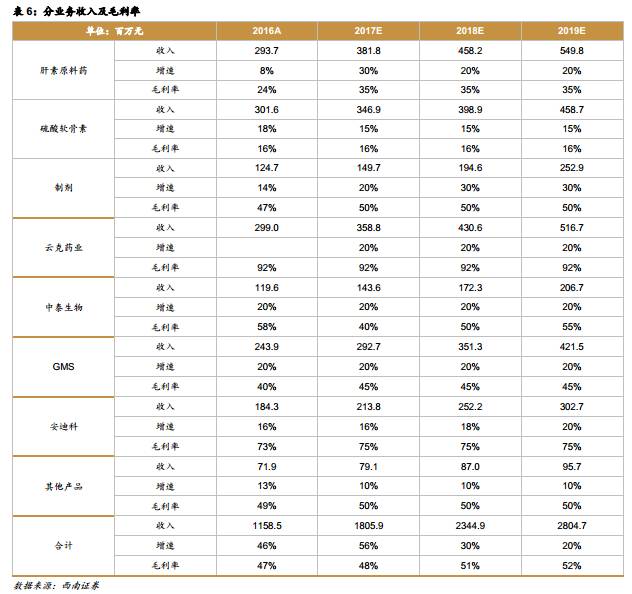
考虑增发摊薄(拟发行6075万股,占公司总股本的8.6%,作价8.2亿),预计公司2017-2019年归母净利润分别为2.2亿、3.8亿、4.7亿,对应PE分别为50倍、29倍、23倍。如考虑安迪科在2017年全年并表,预计2017-2019年备考净利润分别为2.8亿、3.8亿、4.7亿,对应PE分别为39倍、29倍、23倍。
按照备考业绩测算,预计2018年东诚药业的归母净利润将达到3.8亿,同比增长35%,考虑核素药物的稀缺性和持续外延并购预期,我们认为公司应该享受一定的估值溢价,给予公司2018年40倍PE,对应目标价19.60元。
6风险提示
1、安迪科收购进度或业绩不及预期的风险;
2、肝素原料药提价幅度或不及预期的风险。

分析师承诺:本报告署名分析师具有中国证券业协会授予的证券投资咨询执业资格并注册为证券分析师,报告所采用的数据均来自合法合规渠道,分析逻辑基于分析师的职业理解,通过合理判断得出结论,独立、客观地出具本报告。分析师承诺不曾因,不因,也将不会因本报告中的具体推荐意见或观点而直接或间接获取任何形式的补偿。

重要声明
西南证券股份有限公司(以下简称“本公司”)具有中国证券监督管理委员会核准的证券投资咨询业务资格。
本公司与作者在自身所知情范围内,与本报告中所评价或推荐的证券不存在法律法规要求披露或采取限制、静默措施的利益冲突。
本报告仅供本公司客户使用,本公司不会因接收人收到本报告而视其为客户。本公司或关联机构可能会持有报告中提到的公司所发行的证券并进行交易,还可能为这些公司提供或争取提供投资银行或财务顾问服务。
本报告中的信息均来源于公开资料,本公司对这些信息的准确性、完整性或可靠性不作任何保证。本报告所载的资料、意见及推测仅反映本公司于发布本报告当日的判断,本报告所指的证券或投资标的的价格、价值及投资收入可升可跌,过往表现不应作为日后的表现依据。在不同时期,本公司可发出与本报告所载资料、意见及推测不一致的报告,本公司不保证本报告所含信息保持在最新状态。同时,本公司对本报告所含信息可在不发出通知的情形下做出修改,投资者应当自行关注相应的更新或修改。
本报告仅供参考之用,不构成出售或购买证券或其他投资标的要约或邀请。在任何情况下,本报告中的信息和意见均不构成对任何个人的投资建议。投资者应结合自己的投资目标和财务状况自行判断是否采用本报告所载内容和信息并自行承担风险,本公司及雇员对投资者使用本报告及其内容而造成的一切后果不承担任何法律责任。
本报告版权为西南证券所有,未经书面许可,任何机构和个人不得以任何形式翻版、复制和发布。如引用须注明出处为“西南证券”,且不得对本报告进行有悖原意的引用、删节和修改。未经授权刊载或者转发本报告的,本公司将保留向其追究法律责任的权利。