专栏名称: 生信人
| 共同学习生物信息学知识,共同探究生物奥秘。 |
目录
相关文章推荐

|
华大集团BGI · 重塑“秘密花园”:华大等揭秘人工阴道菌群演化之谜 · 12 小时前 |

|
生物探索 · Immunity | ... · 2 天前 |
|
|
华大集团BGI · 华大集团祝您中秋快乐,阖家团圆! · 2 天前 |
|
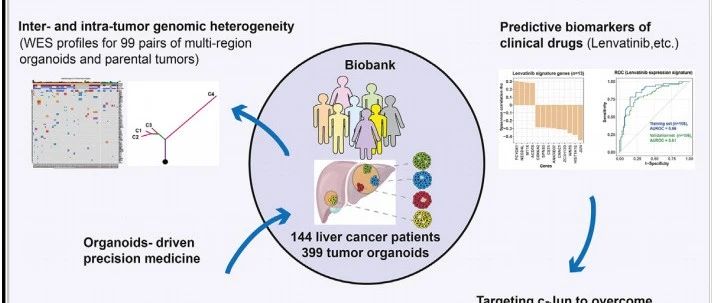
生信人 · 顶刊聚焦类器官,生信也能尝尝鲜 · 4 天前 |

|
BioArt · Cell重磅,胶质母细胞瘤如何实现“免疫逃逸 ... · 4 天前 |
推荐文章

|
华大集团BGI · 重塑“秘密花园”:华大等揭秘人工阴道菌群演化之谜 12 小时前 |

|
生物探索 · Immunity | 肠道Tuft细胞分泌乙酰胆碱促进宿主排虫 2 天前 |
|
|
华大集团BGI · 华大集团祝您中秋快乐,阖家团圆! 2 天前 |

|
生信人 · 顶刊聚焦类器官,生信也能尝尝鲜 4 天前 |

|
BioArt · Cell重磅,胶质母细胞瘤如何实现“免疫逃逸”,100%单细胞分选技术助力细胞系构建! 4 天前 |

|
创事记 · 重回主流,微博做对了什么,还需做什么 7 年前 |

|
陈安之 · 从欠款还款看人品 7 年前 |

|
新华网 · 习近平最牵挂的人是谁? 7 年前 |

|
无极太极 · 缘起无极太极:让更多人学到真功夫! 7 年前 |

|
色影无忌 · 为什么摄影人无法理解当代艺术? 7 年前 |
