这就是人类和癌症做斗争中所面临的最残酷的现实和挑战:抗药性和变异性。以免疫检查点抑制剂为例,其耐药机制与免疫识别缺陷,对免疫效应分析的敏感性,肿瘤微环境和新生血管,肿瘤多能性和可塑性,肠道微生物以及染色质重塑复合物等相关。
今天为大家阐述免疫识别缺陷中影响抗原呈递的两个重要因素:HLA杂合性缺失与B2M缺陷。
人类白细胞抗原(human leucocyte antigen,HLA) 是人类组织相容性复合体(MHC)的表达产物,肿瘤细胞表面上也存在HLA,参与抗原的处理和呈递。HLA对CD8+ T Cell识别肿瘤细胞必不可少。人体大部分细胞含有两套HLA分子编码基因:一套基因遗传自母亲,另一套基因遗传自父亲。有时,基因变化能够导致一套基因全部或部分丢失,称为杂合子缺失(LOH)。
当HLA位点发生LOH,有可能促进免疫逃避,从而导致免疫治疗耐药(图1)。
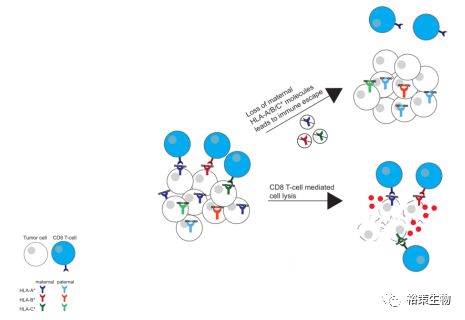
图1 癌细胞表面杂合性缺失导致免疫逃逸
2017年11月,《Cell》杂志发表的一篇文章:Allele-Specific HLA Loss and Immune Escape in Lung
Cancer Evolution1。文章中作者及其团队开发了一款从测序数据中确定HLA等位基因特定拷贝数的软件,叫做LOHHLA,并对90位非小细胞肺癌患者进行了HLA LOH鉴定,发现40%的患者具有HLA杂合性缺失。
杂合性缺失在非小细胞肺癌里面呈现正向选择(图2),这些数据显示了HLA LOH在肺癌进化过程中是一种常见的免疫逃避机制。
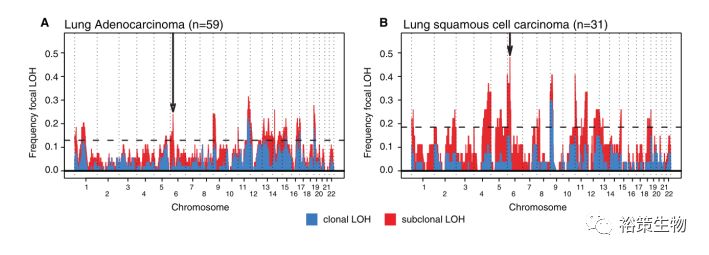 图2 LOH在非小细胞肺癌里面呈现正向选择
图2 LOH在非小细胞肺癌里面呈现正向选择
紧接着,2017年12月,《Science》杂志发表的一篇文章:Patient HLA class I genotype influences cancer response to checkpoint blockade immunotherapy2。 CD8+ T细胞杀死癌细胞,需要通过HLA-I型分子有效地呈递肿瘤抗原。然而,针对特定患者的HLA-I基因型对抗PD-1/CTLA-4响应的程度目前还不清楚。
为了阐明HLA-I基因型与免疫检查点抑制剂疗效之间的关系,作者分析了1535名接受免疫检查点抑制剂的晚期癌症患者的HLA-I基因型。
将所有的患者分成了两组,Cohort1:有269位晚期黑色素瘤患者和100位晚期非小细胞肺癌患者接受anti-CTLA-4或者anti-PD -1治疗;Cohort2:有1166位不同晚期肿瘤类型的患者,接受anti-CTLA-4,或anti-PD-1/PD-L1,或者是两者联合治疗。杂合型HLA-I可以提高患者的OS(图3)。
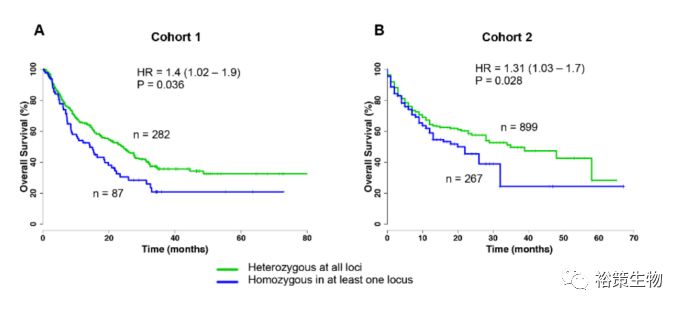
图3 杂合型HLA-I可以提高患者的OS
作者在研究过程中思考,既然如此,是否有更大的多样性(杂合性)可以在免疫检查点抑制剂治疗过程中获得更好的生存期呢?作者将黑色素瘤的27个HLA-A等位基因划分为6个超亚型,50个HLA-B等位基因划分为6个超亚型。其中,使用anti-PD-1或anti-CTLA-4治疗的黑色素瘤患者有HLA-B44超亚型的整体存活
率显著提高(图4)。
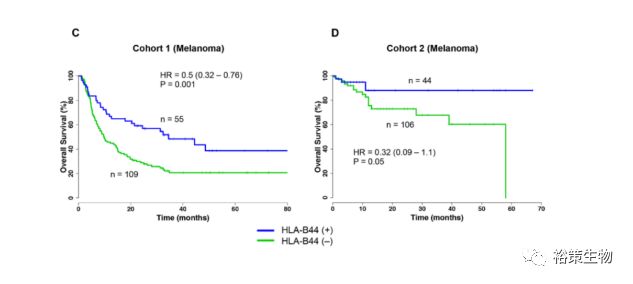 图4 有HLA-B44超级型的黑色素瘤患者整体存活率显著提高
图4 有HLA-B44超级型的黑色素瘤患者整体存活率显著提高
相反,具有HLA-B62(HLA-B*15:01)超级型的患者与更差的预后相关(图5)。
这项研究结果显示,HLA-I基因型会影响使用免疫检查点抑制剂患者的生存期。表明可以在未来临床试验的设计中考虑这个因素。
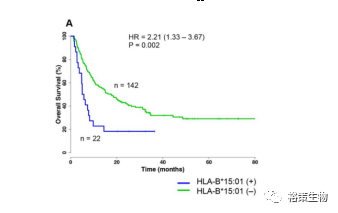
图5 HLA-B62超级型患者OS较差
大量的证据已经表明B2M基因缺陷会影响MHC I的正常折叠和运输到细胞表面(图6),从而产生对免疫检查点抑制剂的耐药。
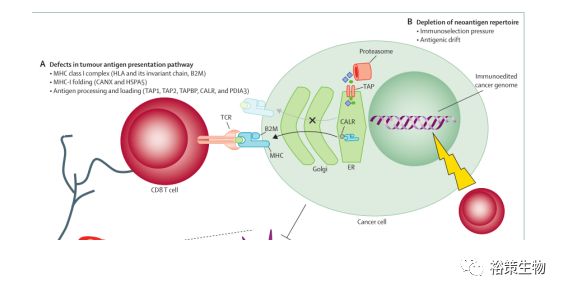
图6 B2M是MHC折叠和运送到细胞表面的关键基因
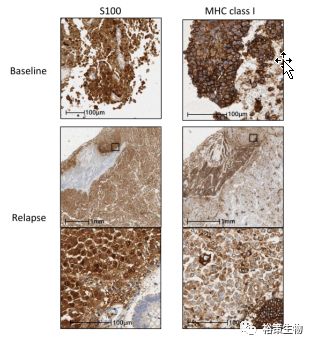
2016年9月,《NEJM》发表的:Mutations Associated with Acquired Resistance to PD-1 Blockade in Melanoma3,文中提到B2M的截断突变导致了MHC I的细胞表面表达的丢失。其中一名B2M突变的患者的肿瘤细胞进行MHC I型免疫组织化学染色,显示出B2M突变的患者肿瘤细胞的外细胞膜缺乏MHC I型(图7)。