
抗药物抗体(ADA)是蛋白药物成功临床应用的一个主要障碍,降低患者的治疗效果和安全性。预测抗体药物的免疫原性,对于临床试验顺利进展以及药物临床使用极其关键。
影响蛋白类药物免疫原性的因素,包括治疗性蛋白的内在和外在特性,患者相关因素(HLA单倍型、免疫状态)、治疗环境、药物递送方式和作用模式(MoA)等。
生物信息学评估
生物信息学主要用于预测药物氨基酸序列中潜在的
T细胞表位
。
系统扫描蛋白质的一级结构,计算可以与HLA结合的9-15mer表位并评分。在药物开发阶段,减少从苗头化合物(Hits)到候选药物(leads)数量,同时减少将来进入临床的候选药物的潜在T细胞表位,降低临床试验中ADA的发生。
单纯靠HLA亲和力进行预测,会大大高估T细胞表位数量,需要考虑更多的因素,如
影响9-15ʹmer氨基酸序列成为功能T细胞表位的因素:
-
HLA分子形成复合物的稳定性
-
APC对于表位的自然处理
-
序列-MHC-II槽特定的CD4+T细胞的存在
HLA结合序列不能成为T细胞表位的其他因素:
-
亲和力太低,无法引起免疫反应,
-
阴性选择已经清除了特定的T细胞,
-
Treg介导的外周耐受。
MHC洗脱肽结合质谱分析获得基础数据,再对算法系统进行教育,使其获得判断T细胞功能表位的能力。
有一些相关技术被开发:
-
MixMHC2pred
:集成了等位基因特异性基序,肽长度和结合核心偏移偏好,使用超过99000个独特的洗脱肽,进行
MoDec
分析(一个新的肽深度基序反褶积概率框架)。
-
MARIA
:基于多模态递归神经网络算法,包括肽序列、基于侧翼残基预测信息的切割分数和HLA结合分数,两者都来自新的预训练神经网络。Maria还包括基因表达水平,这是其特有的。
-
MAPTAC
:基于HLA-II等位基因纯化结合肽,通过LC/MS分析肽序列,预测肿瘤HLA-II结合肽。
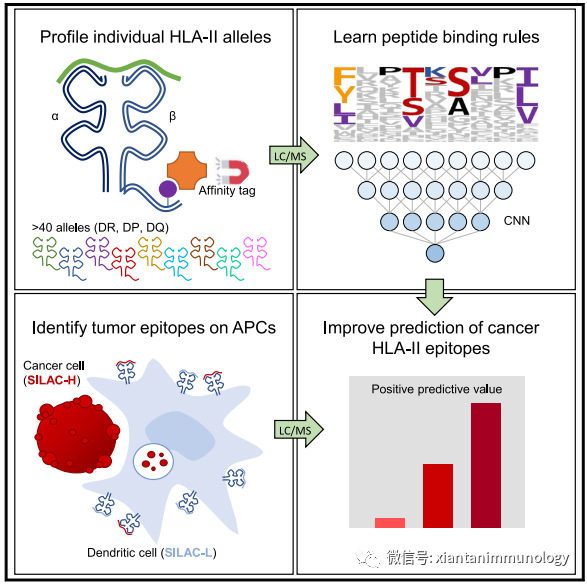
Immunity
2019,
51
,
766–779
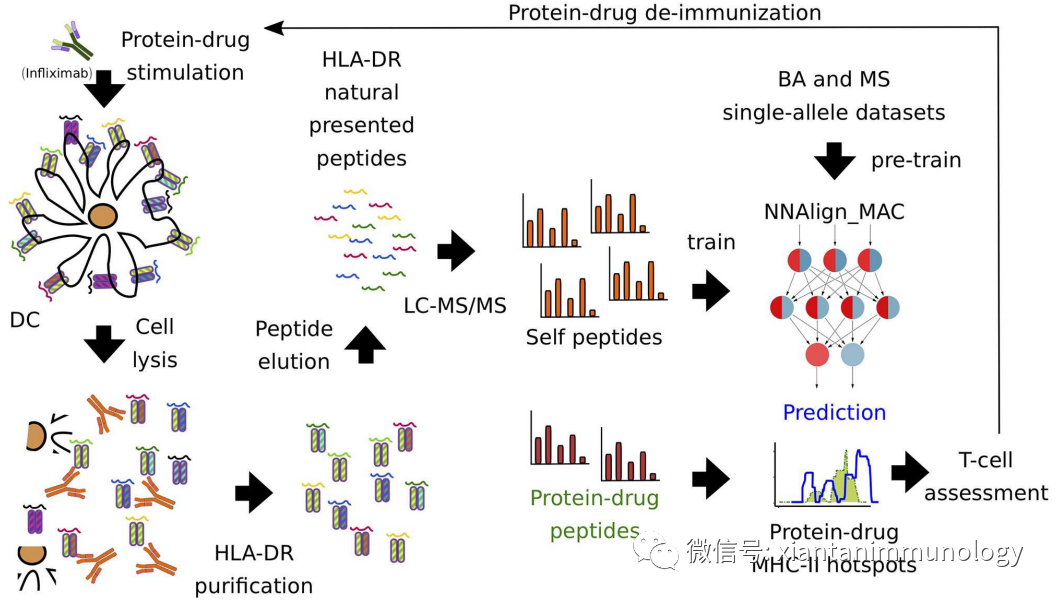
NNAlign_MAC 蛋白质药物(英夫利昔单抗)免疫肽谱分析
Front
Immunol. 2020;11:1304.
上述方法有特定的应用场景,且没有整合ADA的临床检测数据,因而不可以盲目使用。
免疫细胞功能实验
1. DC细胞成熟试验
可以激活DC等APC细胞,是预测生物药产生ADAs的指标之一。监测DC细胞成熟可以作为监测药物免疫原性的工具。
moDC可以通过几种方式生成。从人血液中分离PBMCs后,用磁珠分选单核细胞。加入
GM-CSF
和
IL-4
,诱导纯化单核细胞分化为不成熟moDCs。
使用生物药攻击moDCs,监测攻击后15分钟到48小时的
细胞参数
:
-
4-48小时,检测
细胞表面标记物
表达(至少包括CD83、CD80、CD86和CD40)
-
24-48小时,检测细胞培养上清
细胞因子分泌
(IL-1β、IL-6、IL-8、IL-10、IL-12和TNF)
-
15-30分钟,参与DC成熟的
信号通路蛋白
的磷酸化,如Akt,ERK1/2和Syk,
-
早期(6-24小时)mRNA定量细胞因子和/趋化因子
对照组设定
对结果的评估取决于所使用的方法,通常涉及对至少10个捐赠者的统计分析。DC激活细胞表面标记物增加50%或100%。
2. T细胞功能试验
体外T细胞活化试验,试图通过测量CD4+T细胞对药物T细胞结合结构域的活化情况,评估治疗性蛋白和多肽的免疫原性风险。
T细胞功能检测通常由四个不同的成分和顺序步骤组成:1)抗原攻击、2)细胞培养成分和刺激、3)检测结果读出、4)数据分析
试验的关键点
1)抗原攻击
抗原剂量/浓度
对于记忆/回忆反应
单次攻击就足够了;攻击后24-72小时细胞因子读数,第7天的增殖读数。
对于初始反应
产生抗原特异性T细胞需多个连续抗原攻击;孵育时间可能在7到28天之间变化。
抗原作用模式
基于抗原性和靶点作用,细胞和检测形式将发生改变。
2) 细胞培养成分
-
培养基:RPMI, DMEM, Earle’s modified
-
血清:AB血清、自体血清、无血清
-
刺激抗原
-
细胞因子:IL-2, IL-6, IL-7, IL-12,IL-15, IL-17, IL-21(考虑:剂量、时间点、持续时间)
-
用于DC成熟的细胞因子:IL-4、GM-CSF和LPS,减少旁观者T细胞反应,并使用IFN-α减少背景
-
外源性刺激:LPS、TNF-α、IFN-α、CD40L、成熟鸡尾酒刺激未成熟树突状细胞
3)结果读取
ELISPOT 和 Fluorospot
:多重检测,根据细胞因子谱分析Th亚型。是短期记忆T细胞分析的理想选择,可以识别记忆T细胞的低频T细胞前体。
T细胞增殖
:
T细胞活化的标记物
;荧光标记物(如
CFSE
);DNA增殖标记物和
Ki67
的细胞内染色;最适合延长刺激时间以产生初始T细胞反应。
使用
基于
流式细胞术
分析
:细胞
表面标记物如CD154(表明抗原特异性CD4T细胞活化)或细胞内细胞因子染色(作为T细胞活化
的标记物)
利用
Luminex®和MSD
等平台分泌细胞因子panel
3. B细胞功能分析
评估特定生物药品激活CD4+T细胞的潜力,它们激活B细胞,并诱导其分化为产生ADA的浆细胞。
B细胞表位
和产生生物药品特异性IgG的
B细胞数量
,是免疫原性风险的重要标准。然而,免疫原性风险评估中的B细胞成分目前被大大忽视了,主要受限于体外评估B细胞的技术。
B细胞表位
生物信息学预测方法已经被开发,如SEPIa,一种结合了13种不同序列衍生特征的算法,包括氨基酸组成、亲水性、溶剂可及性和主链灵活性。研究发现,SEPIa的性能优于基于序列和基于结构的现有方法,但与T细胞表位预测相比,仍然有局限。
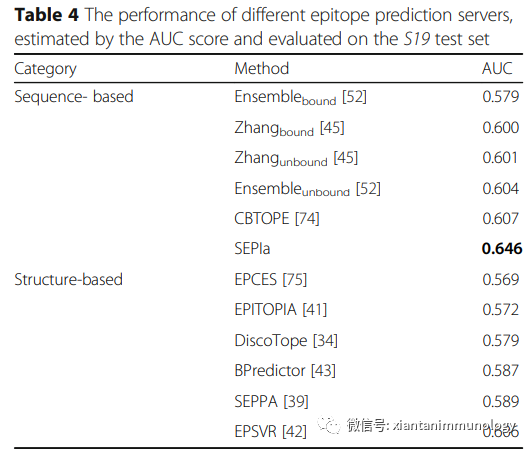
产生特定IgG的B细胞数量
迄今为止,只有基于
ELISpot/FluoroSpot
的检测方法,被报道用于体外评估生物药品特异性IgG-B细胞。
它用PBMCs进行实验,报告分泌靶抗原特异性抗体的B细胞的数量。
该实验通过用激活鸡尾酒(通常至少包含一种TLRs激动剂和IL-2)启动B细胞,将记忆B细胞分化为浆细胞。




















