高血压与慢性肾脏病(CKD)密切相关,二者本身都具有非常严重的疾病负担,二者共病是临床上较为常见的情况。据研究显示,约 1/3 的高血压患者合并 CKD
[1]
。需注意的是,
高血压与 CKD 在病理生理机制上相互作用,形成恶性循环,进一步加重疾病负担
[2]
。在临床工作中,面对高血压合并 CKD 患者,如何改善患者心肾获益,是临床医生面临的重要问题。
在刚刚结束的第二十七届中国医师协会介入心脏病学大会暨第十三届中国胸痛中心大会上,多位专家学者围绕高血压合并 CKD 疾病主题展开精彩讨论,强调临床心肾共管的重要性。基于此,我们邀请到
广东省人民医院心内科陈鲁原教授,
分享高血压合并 CKD 的最新诊疗理念,以期为临床诊疗带来新启发。
SGLT-2i 的作用机制是什么,有哪些研究支持?
Q1:
高血压合并 CKD 患者的临床处理较为棘手,其治疗需要综合考虑降压治疗、肾脏保护以及心血管疾病预防等方面。那么,目前最新高血压领域的指南对于高血压合并 CKD 患者有哪些诊疗建议?
陈鲁原教授:对于高血压合并 CKD 患者,控制血压与优化 CKD 管理,二者应双管齐下,同步进行
[3]
。
►
首先,关于降压治疗。陈鲁原教授强调,一旦肾脏出现损伤,高血压合并肾脏疾病的血压控制尤为困难,通常需要联合治疗。《欧洲高血压学会(ESH)高血压管理指南 2023》(以下简称「ESH 高血压指南」)推荐优先选择 RAS 抑制剂(包括血管紧张素转换酶抑制剂/血管紧张素 Ⅱ 受体拮抗剂)
[3]
,若血压未控制,可联合应用钙离子
拮抗剂(CCB)
或利尿剂。其中,利尿剂的选择需根据估算的肾小球滤过率(eGFR),通常 eGFR < 30 mL/min/1.73m
2
时应用袢利尿剂,eGFR ≥ 45 mL/min/1.73m
2
时应用噻嗪类利尿剂
[3]
。
若患者实施三联疗法后,血压仍无法得到充分控制,此时需考虑引入第四种药物。其中 ESH 高血压指南指出,对于 CKD 处于 1-3 期的患者,第四种降压药物推荐盐皮质激素受体拮抗剂(如螺内酯);然而在 CKD 第 4、5 期,因存在高钾血症的风险而不推荐使用螺内酯,可选择 β 受体阻滞剂或 α1 受体阻滞剂(图 1)
[3]
。值得注意的是,目前已有数种新型抗高血压药物进入临床应用或将要进入临床,如内皮素受体拮抗剂等
[2]
,有望开启高血压合并 CKD 共病管理新航程。
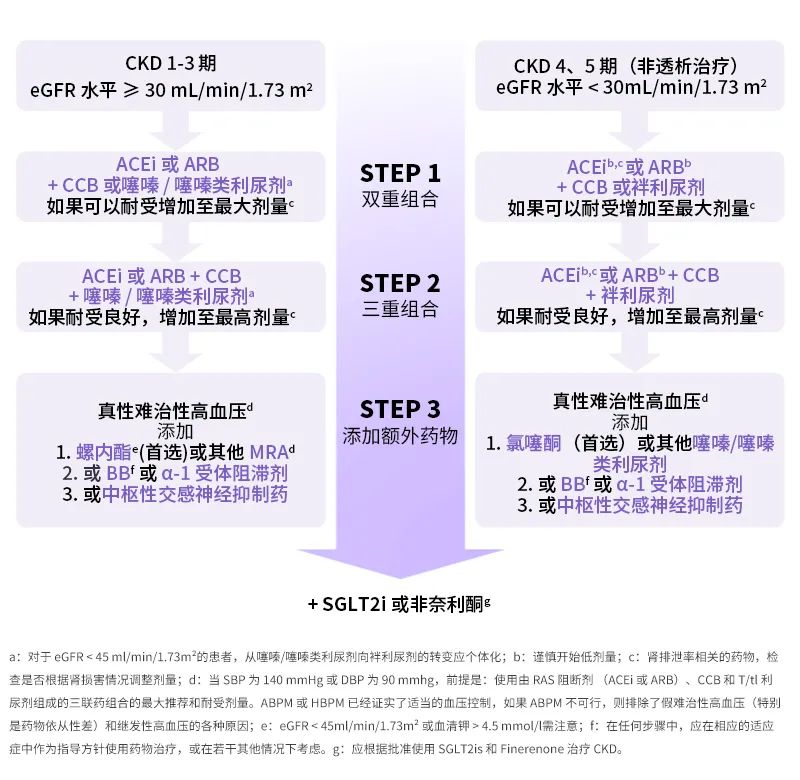
(点击查看清晰大图)
图 1 高血压合并 CKD 患者的降压治疗方案
[3]
►
其次,陈鲁原教授认为,针对肾脏保护措施,尽管
血压控制本身即肾脏保护的一部分,但并不能完全替代其他肾脏保护策略
。
除了生活方式的改善,如合理饮食和适当运动外,特定药物的应用也至关重要
[3]
。
SGLT-2i 即钠-葡萄糖协同转运蛋白 2 抑制剂,已明确被纳入 ESH 高血压指南
[3]
、《KDIGO 慢性肾脏病评估与管理临床实践指南 2024 版》
[4]
及《钠-葡萄糖转运体 2 抑制剂在慢性肾脏病患者临床应用的中国专家共识(2023 年版)》
[5]
(以下简称「SGLT-2i 中国专家共识」)中,推荐用于高血压合并 CKD 患者治疗。其原因是
SGLT-2i 能改善肾脏血流动力学,降低肾脏血管阻力,同时具备抗炎、抗纤维化作用,此外还能改善肾脏缺氧、改善代谢相关危险因素等,从而发挥肾脏保护作用
[6]
。
审批编号:CN-134733;过期日期:2024-10-25
Q2
:
目前研究显示 SGLT-2i 可以带来心肾获益。可否请您谈一谈,SGLT-2i 的作用机制以及相关重要研究。
陈鲁原教授:SGLT-2i 作为一种新型降糖药,在降糖的同时,还具有明显的肾脏保护作用,兼具改善心脏结局事件
[6]
。
●
在心血管保护方面,SGLT2i 已经是全射血分数心力衰竭患者治疗的基石。研究显示 SGLT-2i 介导的尿钠和尿糖的排出可降低心脏负荷;SGLT-2i 还可以通过改善心肌能量代谢增加心肌供氧,改善心肌纤维化延缓心脏重构进程
[7]
。
●
在肾脏保护方面,SGLT2i 同样具有抗炎症、抗肾脏纤维化的作用。此外研究显示, SGLT-2i 可通过收缩入球小动脉调整肾血流量和肾血管阻力,减少近曲小管重吸收减少 Na+/K+ 泵 ATP 耗氧量,改善高滤过和缺氧状态,发挥肾脏保护功能,改善肾脏结局
[6]
。
●
2 型糖尿病患者使用 SGLT-2i 治疗,不增加低血糖风险
[5]
,安全性良好。
SGLT-2i 对伴或不伴糖尿病 CKD 患者的心肾保护作用是近十年来 CKD 管理的重要发现之一。这一发现源自一系列大规模、随机、双盲、安慰剂对照研究。其中,达格列净(DAPA-CKD
[8]
)、恩格列净(EMPA-KIDNEY
[9]
)及卡格列净(CREDENCE
[10]
)三项主要肾脏结局研究,
建议对 eGFR ≥ 25 mL/min/1.73m
2
的成人 CKD 患者(伴或不伴 2 型糖尿病)使用 SGLT-2i
。
DAPA-CKD 研究
[8]
是针对 CKD 患者(合并或不合并 2 型糖尿病)的肾脏终点研究,入组患者中超 90% 合并高血压。主要结局是 eGFR 持续下降至少 50%、终末期肾病或因肾脏或心血管原因死亡的综合结局。结果显示,在中位 2.4 年的随访时间内,达格列净显著降低主要终点事件风险 39%(95% CI,0.51 to 0.72;P<0.001),肾脏特异性复合终点风险 44%(95% CI,0.45 to 0.68;P<0.001),心血管复合终点风险 29%(95% CI,0.55 to 0.92;P=0.009) 和全因死亡风险 31%(95% CI,0.53 to 0.88;P=0.004)。
EMPA-KIDNEY 研究
[9]
,旨在评估 SGLT-2i 对 CKD 患者(合并或不合并 2 型糖尿病)的心肾保护作用,主要结局是肾脏疾病进展的综合结果。结果显示,在中位 2.0 年的随访期间,与安慰剂组相比,恩格列净组显著降低出现肾脏疾病进展或心血管原因死亡的风险 28%(风险比 0.72;95% CI 0.64~0.82;P
CREDENCE 研究
[10]
,旨在评估 SGLT-2i 对 2 型糖尿病合并 CKD 患者肾脏和心血管结局的影响,并评价药物的安全性终点事件(如骨折、胰腺炎、酮症酸中毒和肾细胞癌)。结果显示,卡格列净组发生终末期肾病、血清肌酐倍增、肾脏或心血管死亡组成的主要复合终点的相对风险下降 30%(95% CI,0.59 to 0.82;P=0.00001),由终末期肾病、血清肌酐倍增或者肾性死亡组成的肾脏特异性复合终点相对风险下降 34%(95% CI,0.53 to 0.81;P
SGLT-2i 一旦开启应用,建议在起始治疗的 2~4 周内检测肾功能,并监测血压和血容量,及时评估药物的耐受性和不良反应,以确保疗效和安全性
[5]
。SGLT-2i 中国专家共识提示,SGLT-2i 开始治疗 2~4 周内,可能出现 eGFR 的一过性下降,只要 eGFR 下降小于基线值的 30%,不需要停用 SGLT-2i,只需监测 eGFR 水平变化,经过一段时间治疗后,eGFR 往往会趋于稳定且长期有所改善;更多证据也表明,早期 eGFR 较大幅度的急性下降,反而可以延缓 CKD 进展,是初始治疗获益的标志。仅当 eGFR 下降等于或超过基线值的 30% 时,才建议停药,并寻找可能原因
[5]
。
未来,SGLT-2i 不仅可降糖,也可用于高血压合并 CKD 患者。此外,随着针对 CKD 不同分期和伴随疾病的个性化治疗策略进一步细化和完善,有望通过多靶点、多路径的整合治疗策略,更有效地降低患者心血管事件和肾脏功能恶化的风险。
陈鲁原教授
广东省人民医院心内科、广东省心血管病研究所主任医师、教授
中国高血压联盟副主席、中华医学会心血管病分会第二、第三届高血压学组副组长、中国老年医学会高血压分会副主任委员、广东省医师协会高血压专业医师分会名誉主任委员、中国医师协会高血压专业委员会常务委员(第一、二、三届)、中国医疗保健国际交流促进会高血压分会常委
(第一、二届)















