精彩内容
即将过去的2017年,对诺华来说绝对算得上是硕果丰收的一年。全球首款获批的CAR-T疗法、25年来急性骨髓性白血病首款新药便是最好的例证,这些响亮的标签也同样展现着诺华强劲的新药研发能力。恰逢米内网全球新药研发监测数据库重磅推出之际,我们便从数据库的角度分析下诺华的后期研发管线。
表1:2016全球企业研发投入排行榜(医药企业)
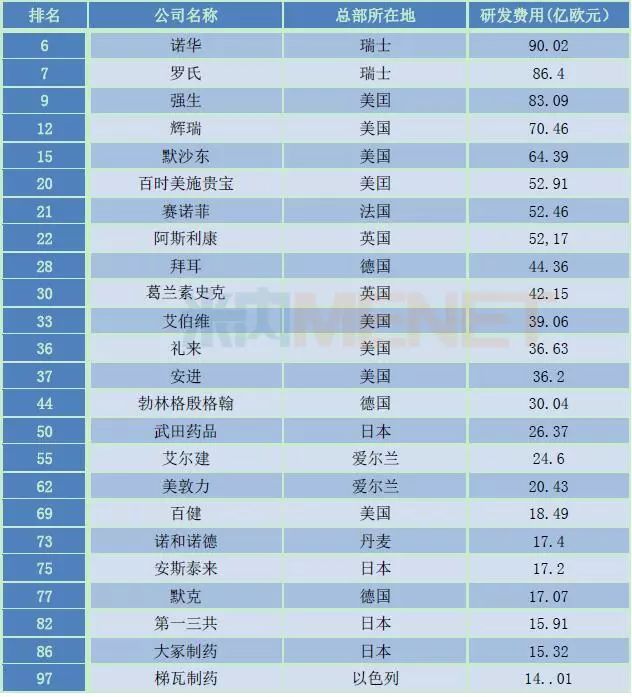
(数据来源:欧盟委员会官方网站)
新药研发有三高一长的特征,高风险、高投入、高回报、研发时间长。欧盟委员会2016年12月27日发布“2016全球企业研发投入排行榜”,此项调查统计了2015/16财政年度全球2500家企业投入的研发(R&D)费用,共有24家医药企业跻身其中前100强企业,占比近四分之一。其中,诺华以90.02亿欧元的研发费用在医药企业中排名第一,在所有企业中排名第6;罗氏和强生紧随其后,研发费用均在80亿欧元以上,并且在所有企业的排名中位居前10。
图1:米内网全球药物研发库搜索结果
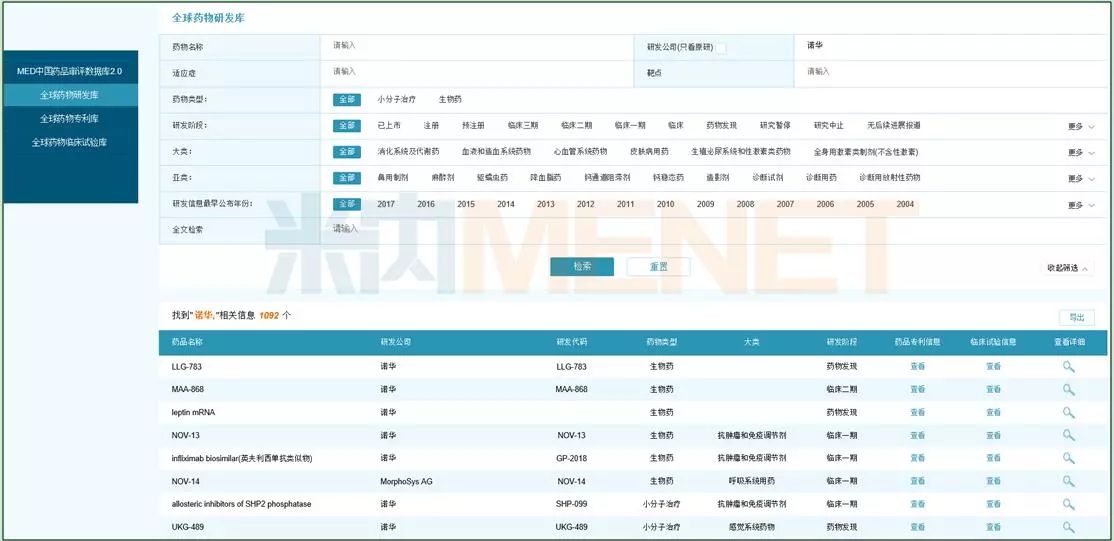
(点击图片可放大)
在米内网全球药物研发库查询诺华的产品管线,发现诺华公司目前在记录的有1092个药物研发项目。
图2:诺华2017年各研发阶段的项目数量统计
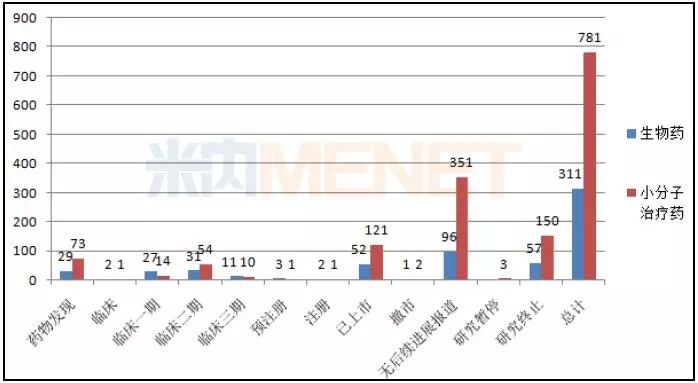
(数据来源:米内网全球药物研发库)
诺华拥有业内最受尊重的药物开发管道,拥有超过250个药物在研项目,是少有的拥有强大创新药物开发和药物仿制能力的公司。目前诺华处于临床三期的药物有21款,处于提交上市申请阶段的药物有7款(预注册 + 注册)。7款提交上市申请的药物中,共有5款仿制药,2款新药。
图3:有望成为重磅炸弹药物的5款新药

(数据来源:米内网全球药物研发库)
根据对米内网全球药物研发库查询出的1092个诺华药物研发项目的分析,我们可以看出诺华的研发管线非常丰富,涉及多个治疗领域。在诸多研发管线中,有5款潜在的重磅新药赢得了大家的持续关注。
诺华的雷珠单抗在国际市场受到再生元阿柏西普的挤压,市场份额持续被侵蚀。在眼科用药市场扩容的情况下,销售额从2015年的35.80亿美元下降至32.41亿美元,衰退之势已经不可避免。眼看诺华抗AMD(老年性黄斑变性)领域霸主地位不保,Brolucizumab及时站了出来稳住了场子。Brolucizumab是诺华开发的新一代抗AMD产品,目前处于临床三期。诺华在近期公布的最新数据显示,Brolucizumab在治疗湿性黄斑变性中能与Regeneron的上市药物Eylea效果媲美。在给药频率方面,Brolucizumab每12周给药一次,时间要久于Eylea的8周一次,这也有望让患者更轻松地接受治疗。基于Brolucizumab药效长、疗效好、给药频率较低等优势,业内给予其很高的评价,预计能在2019年之前上市,未来五年销售额峰值能达到8亿美元。
图4:米内网全球药物研发库查询结果
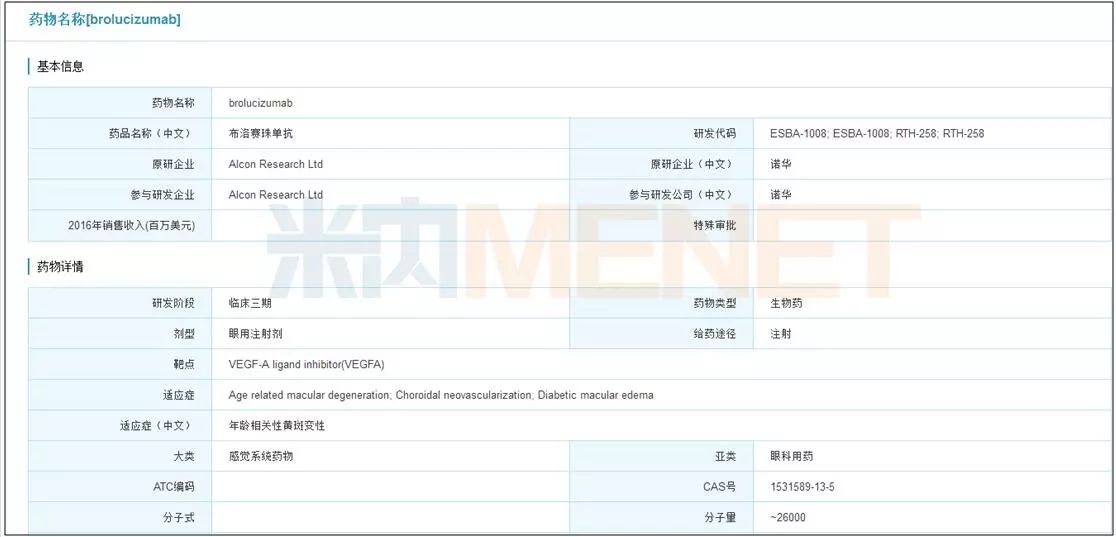
(点击图片可放大)
诺华正在开发的临床新药 Siponimod 是特定类型的鞘氨醇-1-磷酸(S1P)受体的选择性调节剂。S1P受体通常表达在中枢神经系统的特定细胞表面,这些S1P阳性细胞往往引起中枢神经系统损伤,驱动多发性硬化症病情中的功能性丧失。Siponimod的作用机理便是通过进入大脑并结合这些特定受体,可以防止活化这些危害性细胞,从而有助于减少机体和认知功能的损坏。Siponimod在临床三期试验中与安慰剂相比能显著减少残疾进展的风险,业内人士也对其前景表示看好,预计2019年之前能够上市,未来销售额峰值能达到8亿美元。
图5:米内网全球药物研发库查询结果
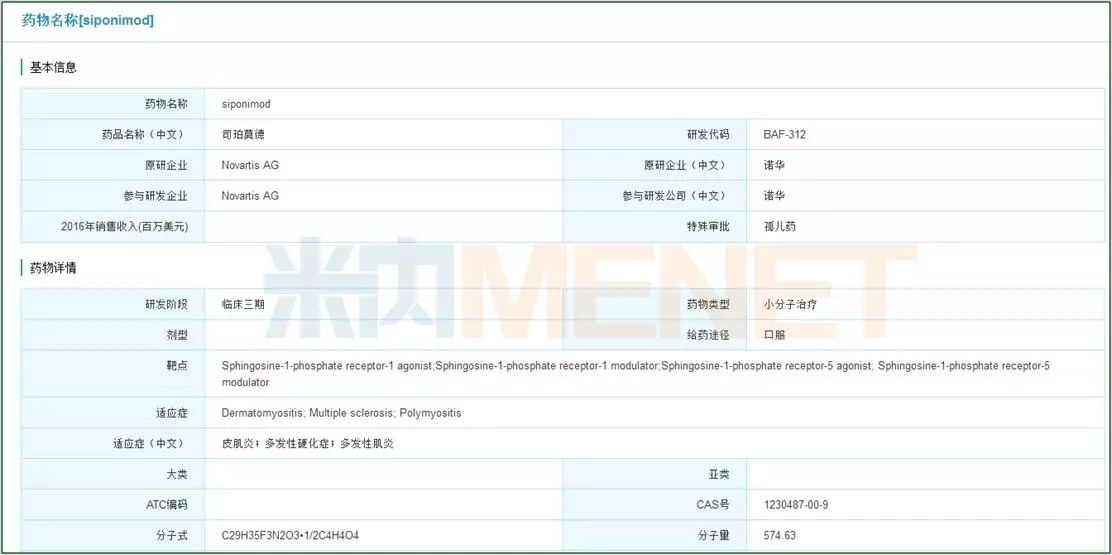
(点击图片可放大)
诺华与安进于2015年8月达成合作协议,共同开发Erenumab用于发作性偏头痛(EM)和慢性偏头痛(CM)的治疗。双方将共同负责Erenumab在美国市场的商业化,安进保留该药在日本的独家商业化权利,诺华则拥有该药在欧洲、加拿大及其他地区的独家商业化权利。Erenumab是一种单克隆抗体药物,通过靶向阻断降钙素基因相关肽(CGRP)受体来预防偏头痛,是目前唯一一个处于后期临床开发的直接靶向CGRP受体的药物分子。在临床三期试验中,Erenumab能有效的预防发作性偏头痛(EM)和慢性偏头痛(CM),显著降低每月偏头痛天数。基于优秀的临床试验表现,诺华于2017年7月21日宣布,美国FDA已经接受了Erenumab的BLA申请,预计能在2018年上半年获批上市,未来五年市场销售额峰值能达到10亿美元。
图6:米内网全球药物研发库查询结果
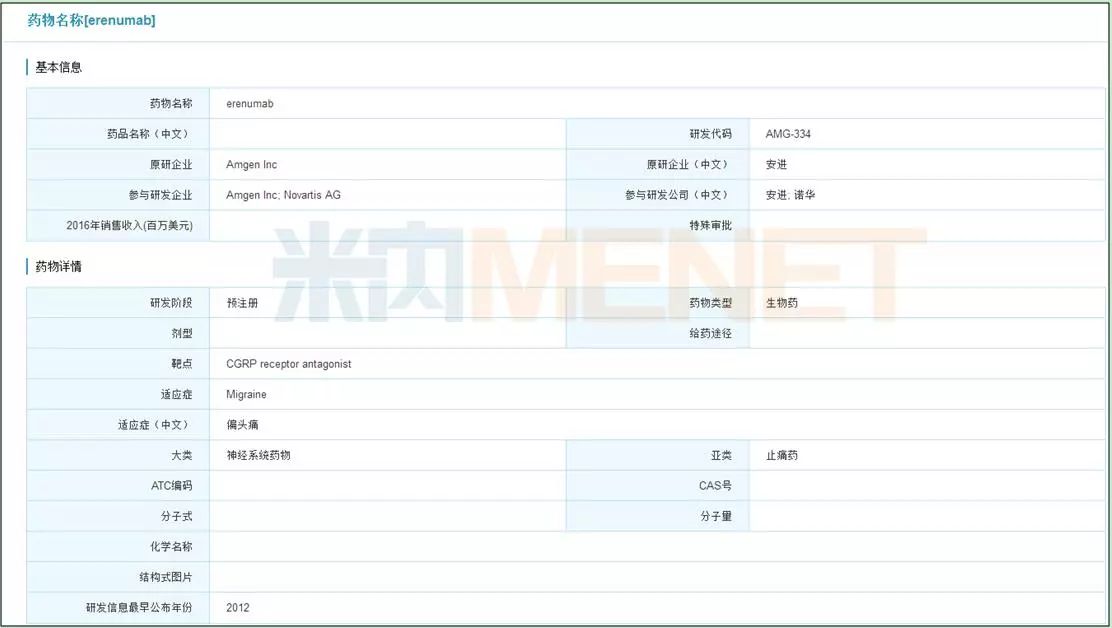
(点击图片可放大)
Kisqali (Ribociclib)于2017年3月13日获得美国(FDA)的批准,由诺华开发,是继辉瑞Ibrance之后第二个CDK4/6抑制剂,用于治疗HR阳性/ HER2阴性绝经后妇女晚期转移乳腺癌。Kisqali对乳腺癌的疗效显著,在2016年5月的临床试验因为表现优秀被提前终止,是辉瑞Ibrance(Palbociclib)的有力竞争对手。Ibrance作为原研首创在商业上非常成功,上市第一年(2015年)的销售额就达到7.23亿美元,2016年更是达到21.35亿美元,预计未来五年销售峰值能达到60亿美元。诺华的Ribociclib排在这个激烈竞争领域的第二位,虽然疗效出色,但相比Ibrance晚上市两年时间,且与Ibrance相比并无明显优势,故一些机构(如Cowen and Company)预计其销售远远低于Ibrance,预计未来五年销售峰值能达到14亿美元。
图7:米内网全球药物研发库查询结果

(点击图片可放大)
2017年诺华最大的成果莫过于首款CAR-T疗法Tisagenlecleucel-T(CTL-019)于8月31日被FDA批准。该疗法有着广阔的市场前景,在抗癌领域中有着划时代的意义。Tisagenlecleucel-T用于治疗难治或至少接受二线方案治疗后复发的B细胞急性淋巴细胞白血病,其余多个适应症拓展的临床研究正在紧锣密鼓的进行中。由于目前CAR-T疗法存在如价格昂贵、无法规模批量生产、毒副作用(细胞因子释放综合征、神经系统毒性等)、对实体瘤效果不佳等诸多问题,该创新疗法还需要比较长的时间才能成为大众化产品,预计未来五年其销售额峰值能达到9亿美元。
图8:米内网全球药物研发库查询结果
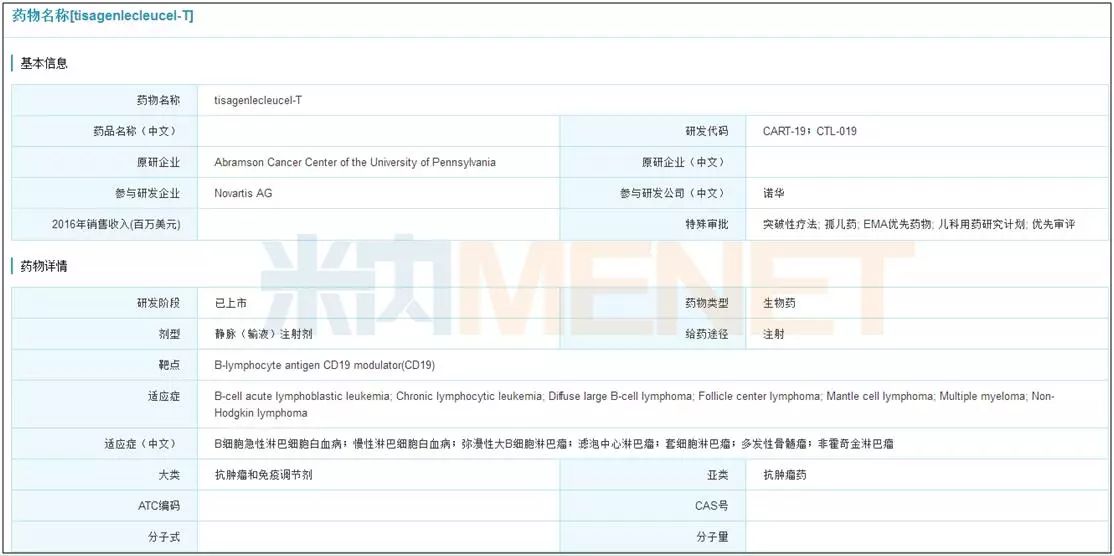
(点击图片可放大)
创新是企业发展的核心动力之一。新药研发催生出的一系列“重磅炸弹”,为一众跨国巨头带来巨额经济效益,诺华便是其中的佼佼者。随着国家鼓励创新政策不断落实,新药研发投入也在不断加大,相信国产药企也能出现下一个“诺华”。
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。
投稿及报料请发邮件到[email protected]
稿件要求详询米内微信首页菜单栏
商务及内容合作可联系QQ:412539092














