重要提示:
《证券期货投资者适当性管理办法》于
2017
年
7
月
1
日起正式实施,通过本微信订阅号发布的观点和信息仅供海通证券的专业投资者参考,完整的投资观点应以海通证券研究所发布的完整报告为准。若您并非海通证券客户中的专业投资者,为控制投资风险,请取消订阅、接收或使用本订阅号中的任何信息。本订阅号难以设置访问权限,若给您造成不便,敬请谅解。我司不会因为关注、收到或阅读本订阅号推送内容而视相关人员为客户;市场有风险,投资需谨慎。

一、主要资料
北京康蒂尼于
2002
年
7
月
3
日注册成立,是一家专业开发孤儿药的公司。
2006
年
6
月,
GNI
收购北京康蒂尼
12%
股权后,北京康蒂尼成为一家中外合资企业。康蒂尼是中国不断发展的孤儿药市场中
IPF
(特发性肺纤维化)药物治疗领域的领导者,拥有自盈利驱动的业务模式,为其在研产品项目的研发持续提供资金。作为中国孤儿药市场的先行者,康蒂尼从事研发工作,且是首家亦是唯一一家推出的化药国家
1.1
类新药被纳入
2019
年
2
月
20
日颁布的中国首份罕见病药品清单的中国制药企业。
公司的主要产品包括:(
1
)艾思瑞(
2018
年占收入的
93.6%
),为吡非尼酮于中国的商品名,是一种具有抗纤维化、抗炎及抗氧化作用的小分子化合物,吡非尼酮可以有效延缓肺功能减退、减少
IPF
疾病进展风险。(
2
)其他非专利药,如吲达帕胺片、罗红霉素片、奥美拉唑钠肠溶片、前列舒丸、阿昔洛韦片、盐酸西替利嗪胶囊及当归苦参丸。
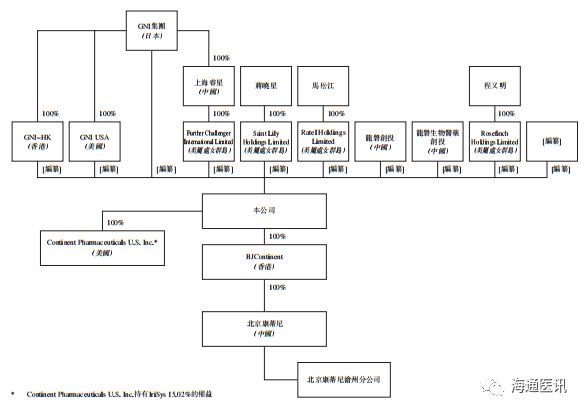
公司控股股东是
GNI
,持有公司
2090
万股,占总股本的
55.97%
。
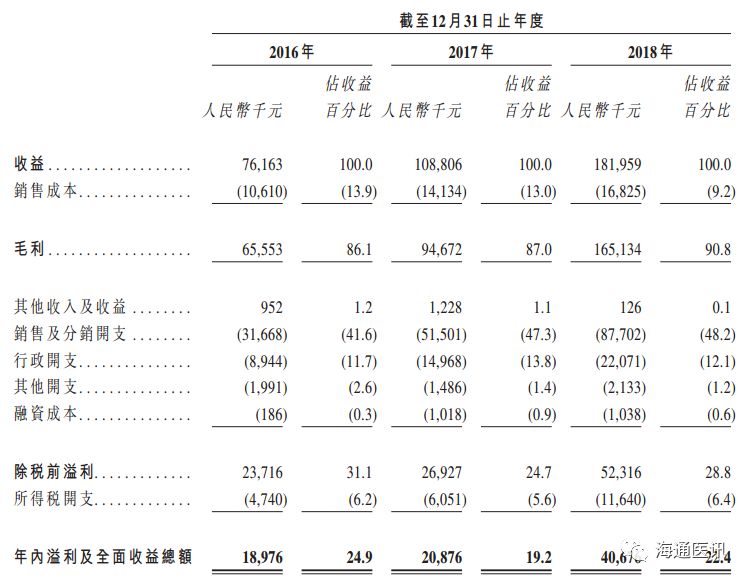
公司
2018
年实现收入
1.82
亿元,同比增长
67.23%
,近三年复合增速
54.57%
,
2018
年净利润
0.41
亿元,同比增长
94.85%
。
二、业务拆分
公司主营业务收入分为艾思瑞和其他非专利药两部分,其中
艾思瑞为一类新药及中国第一个获批用作治疗轻度至中度
IPF
的化药国家
1.1
类药物,是公司营业收入的主要来源(
2018
年销售
1.70
亿元,占总营收
93.6%
)
,自
2017
年以来,艾思瑞已被列为《国家医保药品目录》中的乙类药物,截至目前已被列入
29
个《省市医保药品目录》。此外,
IPF
已列入中国于
2018
年
5
月制订的首批罕见病目录的
121
中罕见病之一。
最近三年,公司主营业务的收入及构成情况如下:
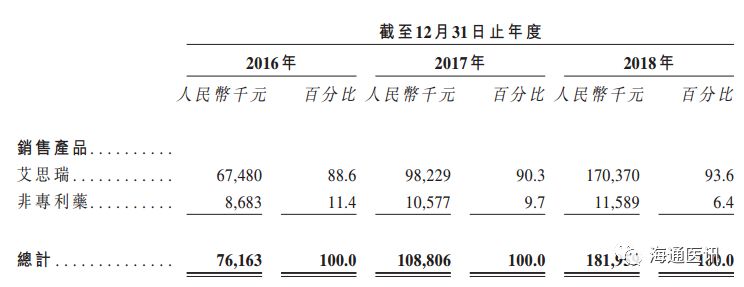
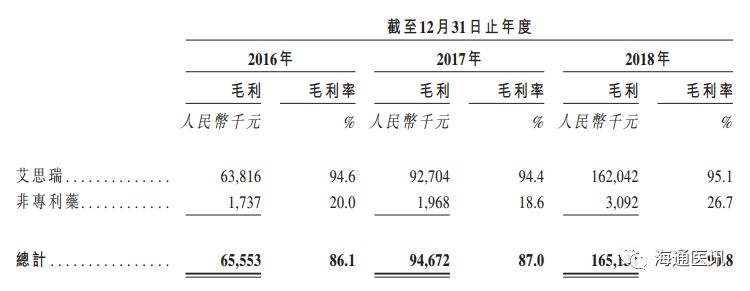
报告期内,公司主营业务毛利率
90.8%
,毛利主要来自于艾思瑞产品线(毛利率
95.1%
)。
下表为近三年公司主要产品的平均售价(经扣除增值税)及销量,其中艾思瑞单价584.70元,2018年销售近30万盒:
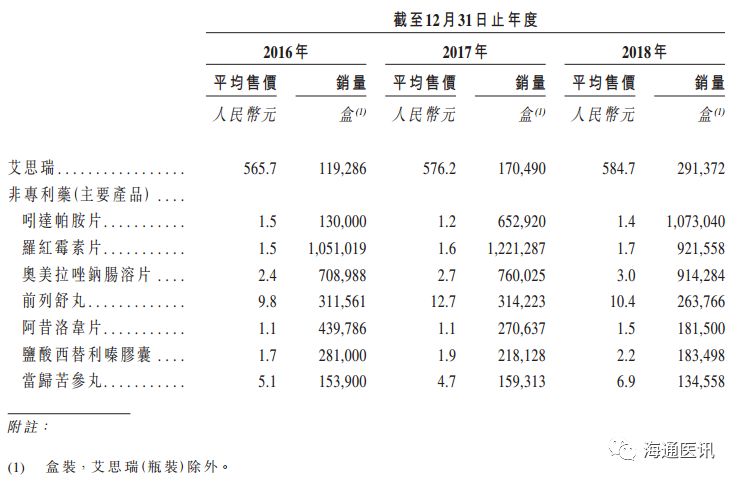
三、行业情况
中国于
2018
年
5
月发布了第一批《罕见病目录》,列有
121
种罕见病。《罕见病目录》每两年更新一次,预期将涵盖越来越多的疾病。中国孤儿药市场有望赶上全球孤儿药市场的发展趋势,预计将按复合年增长率
11.6%
由
2018
年上升至
2023
年的
2390
亿美元,并于未来十年继续增长。
中国
IPF
患者的数量从
2014
年的约
6.70
万人增加至
2018
年的
8.92
万人
,
相当于复合年增长率为
7.4%
,预计于
2023
年达到约
16.67
万人,相当于自
2018
年以来的复合年增长率为
13.3%
。中国的
IPF
治疗药物市场增长迅速,其从
2014
年的人民币
0.14
亿元飙升至
2018
年的人民币
1.77
亿元,复合年增长率为
88.8%
,预计将于
2023
年达到人民币
15.49
亿元,即
2018-2023
年的复合增长率为
54.4%
。
根据弗若斯特沙利文的资料,
2018
年,艾思瑞占中国超过
90%
的市场份额。目前中国
仅有四种
IPF
治疗药物在进行临床试验,且均为一期临床试验,预计不会于
2022
年第四季度前进入市场。
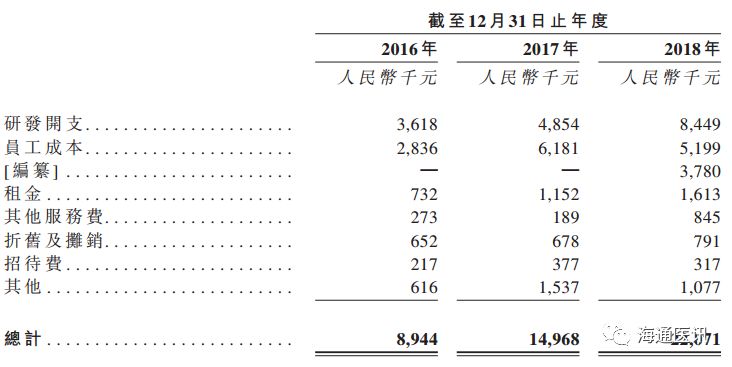
四、研发情况
公司于
2016
年、
2017
年、
2018
年投入的研发开支分别为
361.8
万、
485.4
万、
844.9
万元,分别占总收益的
4.8%
、
4.5%
及
4.6%
。
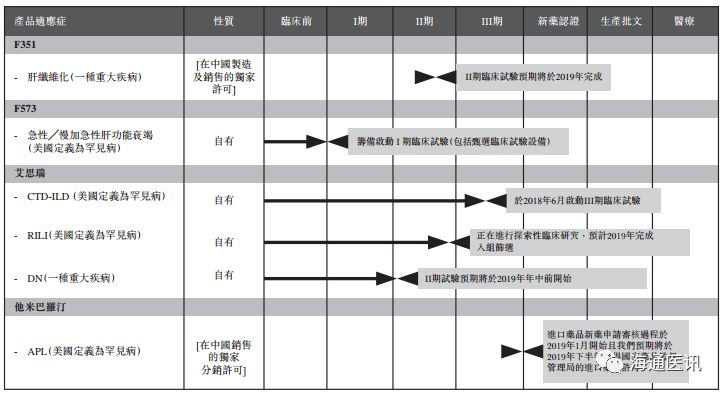
公司目前拥有的处于不同临床开发阶段的在研候选药品包括:
(1)
用于治疗肝纤维化的
F351
,预计
2019
年完成二期临床试验;
(2)
用于治疗急性
/
慢加急性肝功能衰竭
(
美国定义为罕见病
)
的
F573
,预计未来
12
个月内开始一期临床试验;
(3)
主要产品艾思瑞的三种新的适应症:
结缔组织病相关性间质性肺病
(CTD-ILD)
,美国定义为罕见病,
2018
年
6
月启动三期临床试验,预计
2023
年推出该新适应症;
放射性肺损伤(
RILI
),美国定义为罕见病,预计
2019
年完成入组筛选,
2023
年推出该新适应症;
糖尿病肾病(
DN
),预计
2019
年中期启动二期临床试验,
2023
年推出该新适应症。
(4)
此外,康蒂尼与
GN-HK
于
2019
年
4
月
10
日订立一份合作框架协议,内容有关由
GNI-HK
向康蒂尼授出在中国销售用于治疗美国定义为罕见病的急性髓样白血病
(APL)
的他米巴洛汀的独家分销许可。须待双方日后同意订立的独立许可及分销安排后,方可作实。
在研产品中,
F351
未来五年对公司业务影响可能最大,中国拥有庞大的肝纤维化市场潜力及临床需求,且目前并无可靠治疗。
根据弗若斯特沙利文的资料,
2018
年中国有超过
3
亿慢性肝病患者,
3480
万人发展为肝纤维化的慢性乙肝患者,且将持续增长,并于
2023
年达到
3550













