
科学家们发现高水平的维生素C通过结合肿瘤抑制蛋白Tet2影响细胞的数量和功能并影响白血病的发展。
细胞代谢的底物,中间体和产物具有影响细胞识别和转化为癌症的潜力。两篇论文(一篇由Agathocleous等人在线于Nature,另一篇由Cimmino等人在Cell中发表)发现维生素C在干细胞生物学中的作用。他们表明维生素C的水平也被称为抗坏血酸盐,主要通过对Tet2蛋白的影响来调节血液造血干细胞的数量和功能。这种改变又改变了白血病的进展。
研究人员在干细胞中分布代谢物的能力先前受到限制:这种分析通常需要数百万个细胞。例如,小鼠血细胞由少于0.01%的造血干细胞(HSC)5组成,使得难以获得足够的研究数目。 Agathocleous等人通过开发一种用于分析少至10,000个细胞中的代谢物的方法来克服这个问题。使用这种技术,他们发现在不同分化阶段的小鼠血细胞的代谢特征之间存在明显差异。

作者发现维生素C的含量在未成熟干细胞和祖细胞的数量上高于分化较高的细胞类型。与这一发现一致,他们表明,编码维生素C进入的蛋白质的基因Slc23a2的表达在HSC中比在更分化的细胞中更高。重要的是,研究人员证实了他们在人类血细胞中的观察。
Agathocleous和同事们下一步试图确定维生素C水平是否调节HSC数量和功能。不同于人类不能合成维生素C并完全依赖于膳食来源,小鼠产生的酶是古洛糖内酯氧化酶(Gulo),其在肝脏中产生维生素C.因此,缺少Gulo基因的小鼠也依赖于维生素C的饮食来源。作者证明,缺乏Gulo的小鼠在喂养低维生素的饮食时发展出维生素C缺乏症。这些小鼠具有比对照更多的HSC,并且它们的HSC具有增加的功能

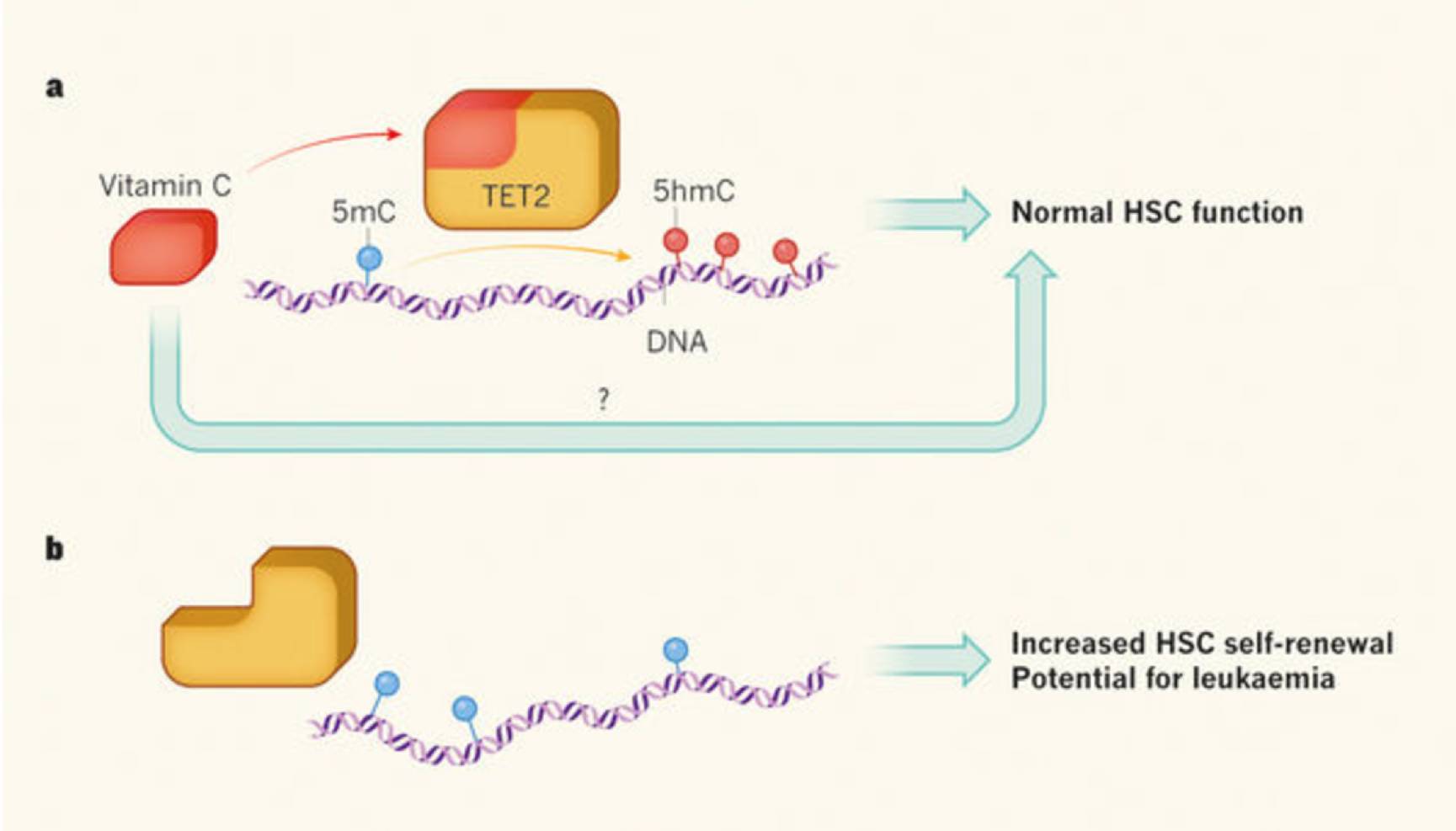
维生素C是Tet2的辅因子,它调节甲基基团DNA的修饰 - 一种可导致基因表达变化的调控机制。具体来说,Tet2催化DNA去甲基化的中间步骤,将分子5-甲基胞嘧啶转化为5-羟甲基胞嘧啶(5hmC)。 Tet2的遗传灭活,就像维生素C耗尽一样,导致HSC数量增加,以及一个HSC分化区块。根据这一点,Agathocleous等人发现维生素C耗尽导致5hmC的降低,表明Tet2活性降低。作者接下来比较缺乏Tet2,Gulo或两者的小鼠,并发现它们之间的5hmC水平和HSC功能仅有轻微的差异,这意味着维生素C耗尽的作用在很大程度上是介导的(尽管不完全是由Tet2) )。
Cimmino等人通过采取替代方法得出了类似的结论。这些动物中Tet2表达的恢复逆转了由Tet2损失引起的HSC功能增强和阻断HSC分化。研究人员接下来证明,它们可以在药理学上达到相同的效果,使用维生素C在体外和体内恢复Tet2的活性。治疗导致更高的5hmC水平,减少HSC自我更新和部分逆转Tet2突变体动物观察到的分化缺陷。
Tet2突变在人类的急性骨髓性白血病(AML)中很常见。因此,两组都检查了维生素C对这种癌症的影响。 Agathocleous等人使用小鼠模型,其中AML由两个突变--Tet2失活和基因FLT3-ITD的过表达(在人类AML的20-30%中发现的突变)10驱动。作者发现维生素C的消耗加速了这些白血病的增长,部分是由于Tet2功能受损。膳食维生素C可以逆转这种作用。
Cimmino等人使用从人体取得的AML细胞,他们在体外研究或移植到小鼠中。在这两种情况下,维生素C补充诱导分化和白血病细胞死亡。在小鼠中,这些变化导致AML进展率降低。
自20世纪70年代以来,维生素C对人体健康和特别是癌症的影响一直是争论的焦点。流行病学研究发现低维生素C降低与心血管疾病和癌症,相关的总体生存和死亡之间存在不同的关联。相比之下,癌症治疗的临床试验没有提供维生素C补充剂对肿瘤生长或存活有益的证据。对于这种差异的一个解释可能是维生素C补充仅对真正缺乏维生素C的人有效,维生素C缺乏的人仅占美国人口的7%。
维生素C和Tet2功能先前已经与炎症相关,这也是与干细胞功能改变,心血管疾病和癌症风险相关的疾病.。
目前的研究支持维生素C缺乏症改变HSC功能并可能影响白血病和其他疾病风险的假说。将来,包括综合性临床,基因组和代谢数据在内的大规模人群研究可能定义维生素C与癌症,心血管疾病和死亡之间的治疗相关关系。这些研究可以证明在进一步定义Tet2突变,维生素C,炎症和癌症之间的关系方面特别有用。
柠檬可能不会为白血病做坏事。尽管如此,我们还是更了解什么使得干细胞正常和癌变成为一个突破。






