在仔细标测之后,首先需要在最早激动点进行消融。但有时你会发现,很多点都“差不多早”(激动时间或提前QRS波的程度),这往往提示壁内起源。
A. 如果GCV/AIV能记录到最早激动点(比其他心内膜或穿间隔支都早),则可以尝试在静脉系统里消融(如图4所示)。消融前应行多体位冠状动脉造影,尤其要注意LAO位(“蜘蛛位”)。一般来说,在心动周期的任何时段内,如果至少2个体位造影提示靶点距离冠状动脉在5 mm以内,则不建议放电消融。在GCV/AIV内消融的最大限制来自于以下几点:(1)消融导管无法到位;(2)由于阻抗过高无法成功放电或达到足够能量;(3)过于靠近冠状动脉血管。在低流速的静脉系统中放电消融,必须使用冷盐水灌注导管,并建议逐渐增加消融能量(目标是20~40 W)。有时可关闭阻抗上限以达到充分能量输出。
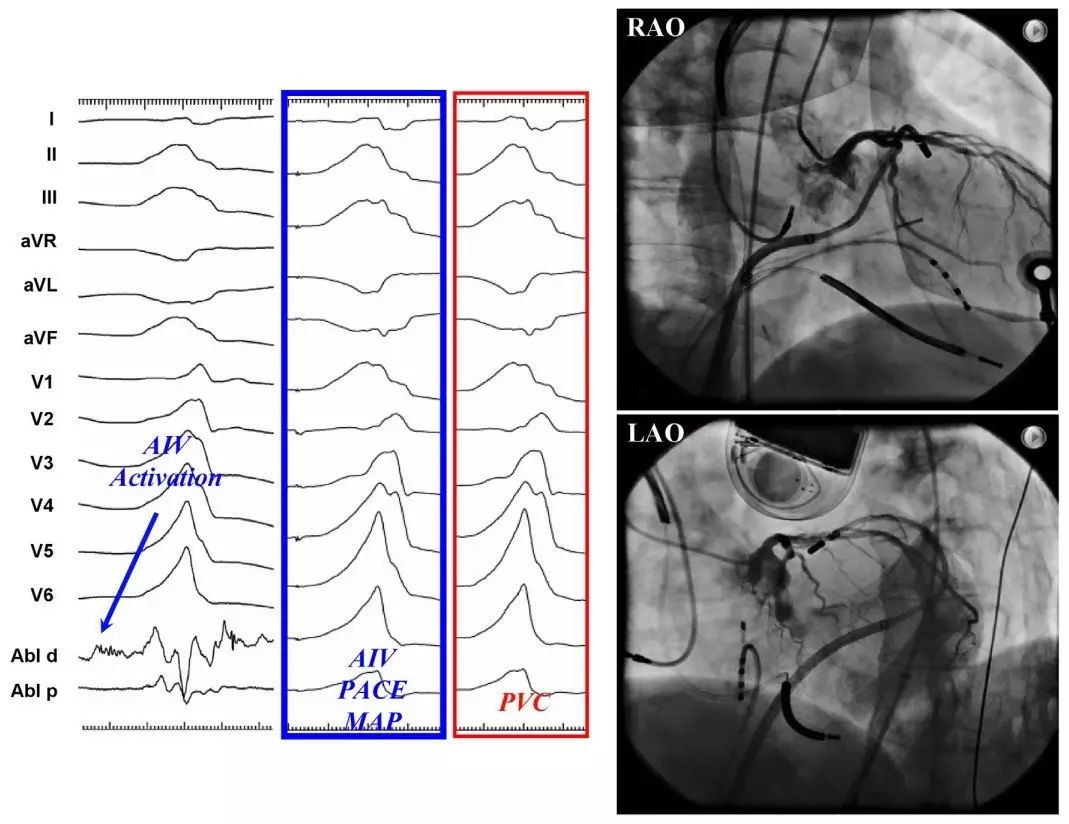
图4. LVS起源PVC消融。左图显示最早激动位于AIV内,右图造影确认消融位点无解剖禁忌。在AIV内该靶点处射频(RF)消融后PVC消失。通常应通过至少2个透视体位,来确认消融靶点距离冠状动脉至少5 mm以上。LAO为左前斜位,RAO为右前斜位。
B. 如果与冠状动脉之间的距离不够安全,GCV/AIV内消融理论上不可行,或在穿间隔支内记录到最早激动点,可在LCC或LV内膜面尝试第一次放电,该处刚好正对于静脉系统里标测到的心外膜最早激动点(如图5及图6所示)。如果ICE显示消融导管与LMCA间距离足够安全,不一定需要行冠脉造影。即便局部激动时间(local activation time,LAT)的提前程度或起搏标测都不如GCV/AIV内靶点满意,但该方法在过半数的病例中还是行之有效的。如果该方法无效或仅一过性有效,可以再从RVOT间隔面进行尝试,尤其是那些激动时间仅轻微落后,RVOT最早激动点与AIV靶点解剖学距离在10 mm以内的靶点(如图7所示)。通常为了达到透壁损伤,可能需要较长的消融时间(≥3 min)及滴定到较高功率(40 W)。

图5. 从左室内膜面基底部成功消融LVS起源PVC病例。伸入穿间隔支的单极导丝(箭头所指)可记录到最早激动点(比GCV/AIV及其他内膜面激动更早),提示壁内起源。消融导管置于LV内膜面,刚好与最早激动点相对,消融放电可成功消除PVC。A图为初始CS造影;B图和C图分别为RAO及LAO体位下导管位置的透视图;D图为CARTO三维重建显示消融导管及靶点位置;E图为单极导丝及消融导管分别记录到的靶点腔内图;F图为单极导丝起搏标测图,起搏图形与临床早搏基本吻合。
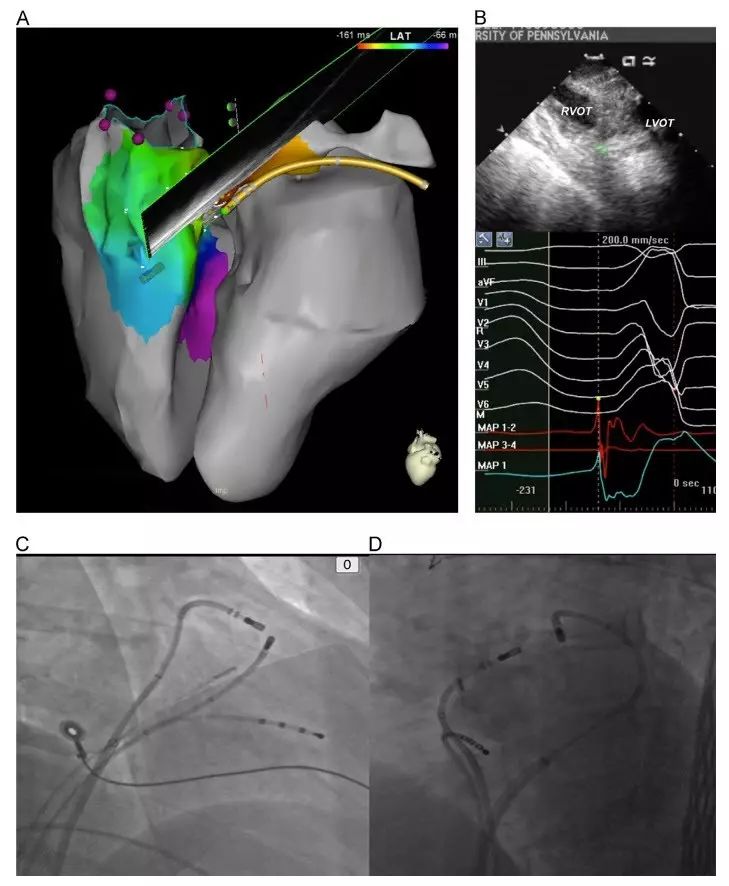
图6. 从RVOT成功消融LVS起源PVC病例。A图三维重建显示RV、LV及静脉系统的解剖关系,其中消融导管置于AIV中。B图为心腔内超声(ICE)所显示的RVOT扇面图,图中可见消融导管头端(绿色标识)。该处双极及单极最早激动时间为-35 ms。C及D图分别为RAO及LAO位透视下,AIV内消融导管与另一根在RVOT内导管的相对位置关系(注意两者的比邻位置)。PVC的最早激动点在AIV内,但冠脉造影提示该靶点距前降支(LAD)距离过近,存在消融禁忌。后在RVOT(邻近结构)内放电,4 s后PVC消失,尽管该处激动相对较晚,起搏标测结果也并不理想。RVOT为右室流出道,LVOT为左室流出道。

图7. 在LCC内成功消融LVS起源PVC病例。LCC内最早激动点仅比AIV内稍许提前(距QRS波起始40 ms)。LAO位透视(上图右侧)上LCC位于主动脉根部最左侧,RAO位透视时位于中部(上图左侧)。LCC腔内电图提示一较大的室波及一较小的远场心房波。注意导管头端与AIV内+极导管间的邻近距离。AIV为前室间静脉;GCV为心大静脉;LCC为左冠窦。
C. 如果在GCV/AIV内及内膜面邻近结构消融均无法成功,或技术上无法实现,最终可能需要行经皮心外膜消融。除非激动标测提示靶点位于可到位区,否则不推荐轻易尝试该方法。心外膜消融的结果并不理想,三分之二的病例也因为靶点过于靠近冠状动脉而不得不放弃。因此冠脉造影是必须的步骤,同时也需通过高能量输出起搏(20 mA,最大脉宽)来仔细确认膈神经的走行。
D. 如果心内膜及心外膜消融都不可行,最后可考虑外科消融。




