BCYC的技术基于Greg Winter爵士和Christian Heinis教授的创新性研究工作,而格雷格·温特爵士是单克隆抗体的先驱,并于2018年获得诺贝尔化学奖。头顶光环的BCYC吸引了众多知名投资机构的亲睐,他们的持仓成本如何,即将迎来的重磅催化剂又会对市场带来怎样的搅动,欲知详情,请移步下文。
关键总结:
(1)BCYC最早创立于2009年的英国,公司的Bicycle(双环肽)技术最早源于诺奖获得者Sir Greg Winter,当前已有较多的技术积累。
(2)公司当前自主研发的方向是基于Bicycle的Bicycle Toxin Conjugates(BTC)的药物研发,Bicycle药物主要与其它机构合作研发。
(3)研发最靠前的BTC药物BT1718的I/II期初步的Topline试验结果预计将于2019年H2发布。该试验结果的分析见“研发管线分析”。该试验结果是初判BTCs研发思路的关键试验结果,将非常大程度地影响公司实际价值及股价。
(4)研发最靠前的Bicycle药物THR-149已在7月1日公布I期的Topline试验结果,主要因疗效逊于已获批的该适应症下其它作用靶点的药物,公司股价即日发生微跌,后持续微跌。I期试验的更新数据将在09/05/2019-09/08/2019和10/12/19 - 10/15/19发布。虽然仅为更新数据,但有可能负面影响股价。相同作用机制的小分子药物KVD001(KALV)目前处于临床II期,将在2019H2发布Topline试验结果,若试验结果好于THR-149,将负面影响BCYC的股价。
(5)截至2019年Q2,公司共有现金1.085亿美元现金,总的现金资产合计1.2亿美元。季度总亏损仅为798.8万美元。公司机构持仓成本均高于12美元。公司当前股价7.69美元,总市值为1.36亿美元。
(6)BCYC上市于2019年5月23日,四家大机构认购了IPO份额(不含绿鞋)的68.8%,近期个人投资者在减少,推测公司已基本被机构控盘。机构的持仓成本基本都在12美元/股以上。
Bicycle Therapeutics(BCYC)成立于2009年,是一家最早创立于英国的生物医药公司,主要基于Sir Greg Winter和Professor Christian Heinis的创新性研究工作。Greg Winter爵士是单克隆抗体领域的先驱,供职于剑桥大学,因其在噬菌体展示用于抗体的定向进化(directed evolution of antibodies)的相关工作,与Frances Arnold和George Smith共同分享了2018年的诺贝尔化学奖。Sir Greg Winter是BCYC的联合创始人,目前仍是公司的非执行董事。
公司自创立以来,积累了诸多技术专利,包括3个用于新型支架的专利,11个用于筛选平台技术的专利,63个用于双环肽和相关偶联物的专利,以及6个用于临床适应症和其他开发资产的专利。
公司开创了双环肽(Bicycles)类药物的研发工作。Bicycles是完全合成的短肽,限制形成(通过半胱氨酸上的二硫键)两个环,以稳定其结构几何(如下图所示)。这种限制的目的是提供高亲和力和选择性,及让分子呈现相对较大的表面区域而使靶标具有成药性。
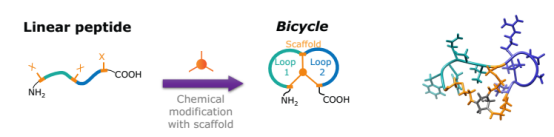
图1
和其它类型的治疗药物相比,Bicycles具有如下图的特点。
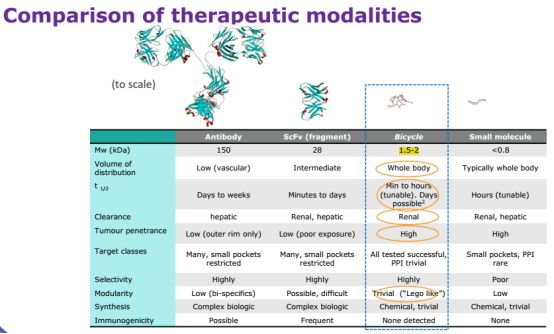
图2
而Bicycles是通过公司基于噬菌体展示的Bicycle Platform筛选得来。根据公司资料,噬菌体展示文库大于1015。在筛选得到目标Bicycles后,公司还将对该序列进行优化(使用非天然氨基酸进行改造),得到PK/PD均符合预期的Bicycles。根据靶标筛选和优化的Bicycles可以单独成为治疗疾病的候选药物。
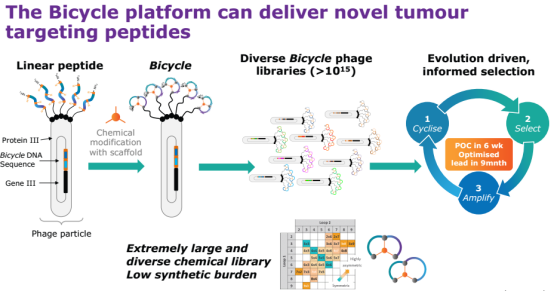
图3
此外,在Bicycles分子上,公司通过利用Linker缀合毒性分子,形成一类具有靶向效果的细胞毒性药物,名为Bicycle Toxin Conjugates (BTCs)。该研发思路与ADC(antibody drug conjugate)非常类似,不同的是靶向靶标的分子由单克隆抗体变为Bicycles,缀合物方面BCYC选择毒素分子。BTCs的分子量大大小于ADCs,因此关键特征是更容易穿透进入肿瘤组织中,根据BCYC公布的部分BTCs的研究资料,一些BTCs还能更好地被肿瘤截留。下两图分别为BTCs候选药物BT1718和BT8009的的分子结构。

图4
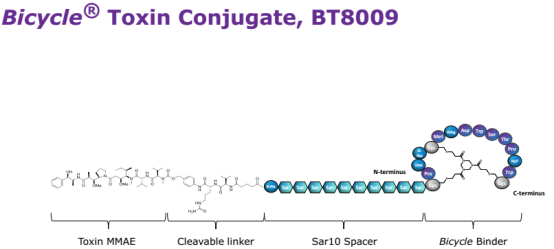
图5

图6
BCYC自主研发策略偏向于BTCs用于肿瘤的治疗。
在研药物BT1718是一种靶向MT1-MMP、携带毒性分子美登素衍生物DM1的BTC。BT1718目前已进入临床I/II期,用于MT1-MMP高表达的实体瘤。该临床试验将评估药物的安全性、可耐受性及有效性,由Centre for Drug Development of Cancer Research UK, or CRUK合作并出资完成
,初步的Topline试验结果预计将于2019年H2发布
(公司的招股书确认)。
BT5528和BT8009为另两种BTCs,靶标分别为Ephrin type-A receptor 2(EphA2)和Nectin-4,携带的毒性分子为MMAE,目前仍在进行临床前的验证。
研究表明,MT1-MMP、EphA2和Nectin-4在许多医疗需求高度未满足的肿瘤类型中过表达,包括肺癌、乳腺癌、胃癌、子宫内膜癌、胰腺癌、膀胱癌、卵巢癌、食管癌和其他癌症。
公司主导的其它在研项目均在药物发现阶段。根据BCYC的Company presentation,BT8009被寄予了厚望,可能的原因是选择Nectin-4的ADC药物Enfortumab Vedotin(Astellas和SGEN共同研发)在mUC适应症下表现突出,目前已提交BLA。
对外合作方面
,公司与多个合作者在抗感染、心血管、血液学、眼科、呼吸等适应症上有合作。
与Oxurion NV (OXUR:BB)合作的药物THR-149是一种血浆kallikrein抑制剂,为Bicycle,为糖尿病黄斑水肿的候选药物。BCYC仅参与该药临床前工作,获得先期付款、里程碑付款和销售分成。THR-149目前已在进行临床I期试验,7月1日发布了Topline结果。
I期试验的更新数据将在09/05/2019-09/08/2019和10/12/19 - 10/15/19发布。
BCYC还在2016年11月与ANZ达成了一项合作,合作领域为呼吸、心血管及代谢性疾病。
其它的合作对象包括Bioverativ, Inc.(or Bioverativ)、Dementia Discovery Fund和Sanofi。
截至2019年Q1,公司已因对外合作产生了累计2650万美元的收入,包括来自ANZ的770万美元、来自Oxurion的410万美元和来自Bioverativ的1470万美元。
关键点评:
本质上来说,基于Bicycle Platform进行的新药筛选和优化过程是一种全新的药物发现方法,基于该方法是否能寻找到合适的Bicycle其实仍首先依赖于开发者对于疾病、治疗手段和靶标的深刻认识,是否能得到理想的Bicycle也存在较大的运气成分。
BCYC选择将自主研发重心放在BTC上,而在Bicycle药物上选择与其它公司合作开发,并收取先期付款、里程碑付款和销售分成,是非常聪明的做法。
但BTC药物的成药前景还需临床上的佐证。
BT1718:
该药选择的靶标为膜型1基质金属蛋白酶(MT1-MMP)。MT1-MMP是一种基质金属蛋白酶,参与组织重建过程,在细胞侵袭和迁移过程中扮演重要角色。MT1-MMP在正常成人组织中低表达,但在多种肿瘤的肿瘤细胞亚群和基质细胞中呈高表达。根据公司进行的肿瘤样本检测结果,在卵巢癌、膀胱癌、肺癌、子宫内膜癌和三阴乳腺癌中,MT1-MMP的表达率为58%-100%。在缀合物方面,罗氏ADC药物Kadcyla使用的也是DM1。Kadcyla已于2013年获批乳腺癌的治疗。
BT1718的临床前数据披露比较充分。关键结果包括:
1. BT1718与MT1的血液结合素域的结合能力非常强,Kd值约为2nM.
2. BT1718的Bicycle部分不会直接激活MT1和相关蛋白酶,但是使用荧光标记的Bicycle时,该化合物发生快速内在化并最终分布在溶酶体。
3. 在接种肿瘤的小鼠模型中,Bicycle被注射到体内后会迅速聚集到肿瘤处,60分钟内,有15-20%的被注射药物沉积到肿瘤。
4. 在细胞系衍生肿瘤(CDX)和病人源的异体肿瘤(包括肺癌、乳腺癌、结直肠癌、胃癌、头颈部癌和多发性骨髓瘤)(PDX)小鼠模型中,BT1718的治疗效果与MT1-MMP的表达水平相关,即中和高表达的肿瘤模型显示PR或CR。起效浓度为3-10mg/Kg,每周1次或2次给药。
BT1718的临床I/II期试验设计:
Phase1stage1/2为剂量递增试验,受试者为晚期肿瘤患者,经
IHC确认MT1-MMP为高表达
。Phase IIa为扩大试验,Part A和Part B选择的肿瘤类型还被建议为
NSCLC or TNBC
。
总结:
从分子设计来看
,在临床前试验中已证实Bicycle部分能快速实现肿瘤定位、发生内在化并分布于溶酶体,但Bicycle缀合DM1后是否顺利发生以上过程还有待临床前动物试验和临床试验检验。因为Bicycle的分子量仅有1.5-2kDa,需拖曳一个毒性分子,而单克隆抗体分子量约为150kDa,最多携带8个毒性分子,相当于20kDa的物体拖曳一个毒性分子(当然单克隆抗体目前携带的毒性分子数量极限并非受限于拖曳能力)。在动物模型中,公司仅简单描述了PR/CR与MT1-MMP的表达水平相关。
目前有理论认为基质细胞与癌细胞耐药性的产生有关,而BT1718除了靶向肿瘤细胞还能靶向基质细胞,对于疗效是加分项。
缀合物DM1已是被验证的分子,只要该BTC能实现靶向性并内吞,该药的效果能较大程度上得到保证。
从临床设计来看
,I/II期试验选择的是MT1-MMP高表达的肿瘤,相较于不考虑MT1-MMP表达水平(如IMMU的Sacituzumab Govitecan做I/II期临床时入组标准不考虑Trop-2的表达水平,仅记录存档),成功概率相对较高。
(MT1-MMP高表达的肿瘤发生比例目前未知。
)
试验从2018年3月开始,若根据公司公布的时间表,试验数据在2019年H2发布的话,试验已进行超过一年。又临床前试验条件已将起效浓度缩窄了较小的范围,该试验起始剂量理论上应比较容易出现阳性结果。
THR-149
:与Oxurion NV (OXUR:BB)合作的药物THR-149是一种基于BCYC平台发现的Bicycle,是一种新型的血浆kallikrein抑制剂,玻璃体内注射给药,当前选择的适应症为糖尿病性黄斑水肿。
糖尿病患者易发生糖尿病性视网膜病变,进而导致糖尿病性黄斑水肿(DME)。DME患者视力模糊,最终可能导致失明(在少数情况下)。DME适应症下当下销售最好的药物是REGN的Eylea。Eylea是一种名为阿柏西普的蛋白药物,用于DME时可以是玻璃体内注射,2014年7月获批。根据Informa的数据,Eylea在DME适应症下的巅峰销售额为2.449亿美元。DME下另一种销售表现不错的药物为罗氏的Lucentis,Lucentis和Eylea一样作用于VEGF,但是为单抗药物,2012年获批上市,巅峰销售额为2.3亿美元。
DME适应症下VEGF靶标仍然是热门,但是已有多家公司进行Kinin-Kallikrein System靶点的研究。当前研究进度最快的是KALV的KVD001,为眼内注射的小分子药物,目前处于临床II期,将在2019H2发布Topline试验结果,I期数据并未公布,Merck公司在2017年与KALV达成合作协议,在KVD001完成II期后将有可能收购该药物。其它的Kinin-Kallikrein System靶点药物为小分子,主要为口服给药,目前均处于临床前。
THR-149是Kinin-Kallikrein System靶点药物中最早公布Topline的药物。THR-149的I期Topline数据公布于2019年7月1日。结果显示,单次注射THR-149后起效迅速(在第一天即起效),14天最佳矫正视力(BCVA)最高提高7.5letters,在90天时,12名患者平均提高6.5letters。而Eylea(VEGF Trap-Eye)的早期数据中,表现最差的试验组(每月注射一次持续三个月+随后每两月注射一次),24周时BCVA平均提高了8.5letters。事实上,THR-149的Topline数据发布当日(7月1日)BCYC股价盘前上涨10%,但收跌1.59%,此后股价呈持续下跌趋势。















