
“华兴资本医疗与生命科技行业周报”定期发布,专注从资本角度,解读一周数据,提供最新行业观察。
医疗与生命科技是华兴资本多年来关注并深耕的领域,目前已为超过100个融资及并购项目担任财务顾问。
医疗与生命科技行业创新不断涌现,已经发展成为最活跃的行业之一,华兴资本始终支持、陪伴这一领域创业企业成长,致力为行业带来理性专业的声音。
关注华兴资本微信公众号(ID:iChinaRenaissance),后台点击“兴观点”-“行业观察”-“生命科技”,获取更多医疗与生命科技行业相关信息。
11月9日,荣昌生物正式在港交所挂牌上市,发行定价为52.10港元每股,发行市值249.22亿港元,总募资额达39.87亿港元。上市首日涨幅39.54%,总市值达347.76亿元。
荣
昌生物
是一家致力于发
现、开发和商业化全球同类首创、同类最佳生物药物的创新性药企。
打造出一个包括抗体和融合蛋白平台、抗体偶联药物平台、双功能抗体平台等三大平台
在内的世界级自主创新研发引擎。
公司在自身
免疫、肿瘤、眼科等重大疾病领域已开发
10
余款全球首创、同类领先的在研生物药,其中
5
款产品针对
17
种适应症正在进行临床试验。
11
月
8
日,南新制药发布公告称,公司拟通过发行股份及支付现金的方式购买兴盟苏州的
100%
股权,交易各方初步商定标的资产预估值不超过
26.712
亿元。
南新制药以仿制药起家,该公司目前的核心产品为抗流感药物帕拉米韦氯化钠注射液,这是南新制药产业化并上市的第一款国家1.1类创新药。兴盟主要从事高端生物药的研发、生产及商业化,并向医药公司提供定制研发与生产服务,在研产品包括4个生物创新药和5个生物类似药,覆盖抗感染、肿瘤等领域。

11
月
10
日,安博生物宣布,完成
2
亿美元
Crossover
轮融资。本轮融资由
Fidelity Management & Research Company
,
Blackrock
旗下基金和账户,
Cormorant Asset Management
,
HBM Healthcare Investments
,
Invus
,
Adage Capital Partners
和
Suvretta Capital Management
投资。
Ambrx是专注于使用扩展的遗传密码开发精准生物制药的临床阶段生物制药公司。Ambrx技术使用扩展的遗传密码将合成氨基酸整合到蛋白质中,所有合成氨基酸插入过程都在活细胞内完成。这些合成氨基酸的定点插入使得精准设计制造生物制药成为可能。

11
月
10
日,瑞科生物宣布,完成超
15
亿人民币
B
轮融资。本轮融资由君联资本和济峰资本联合领投,红杉资本中国基金、祥峰投资、海通开元、基石资本、元生创投、清松资本、光大控股跟投,老股东东方富海旗下基金、深圳沃盈投资旗下基金、宁波浩金致同继续跟投。
瑞科生物是一家由前国家CDC疫苗研发专家团队融合资深疫苗产业化团队共同创立的高科技企业。公司目前已有HPV系列疫苗、重组带状疱疹病毒疫苗、结核病疫苗、重组新冠疫苗等为代表的多条产品线。本次融资募集资金将主要用于公司重点品种产业化基地建设、HPV九价疫苗、重组新冠疫苗等产品临床试验、后续产品管线研发和核心技术平台建设及国际化拓展等方面业务的推进。
11月12日,景杰生物宣布,完成5.3亿元B轮融资。本轮融资由IDG资本领投,达晨、弘晖资本、苏州隆门创投跟投。老股东国投创业继续跟投。
景杰生物是中国蛋白质组学技术应用与开发的领先者,公司以“蛋白质组学--精准医学”前沿研究领域为科学背景,已形成集研发、生产、服务于一体的创新型商业模式,现已建成整合蛋白质组学平台,内含蛋白质组学技术平台、表观遗传学技术平台、生物标志物发现平台、高质量抗体开发平台、诊断试剂盒平台和大数据分析平台。
近日,Prometheus Biosciences宣布,完成1.3亿美元战略融资。本轮融资由Eventide Asset Management和RTW Investments领投,Perceptive Advisors, Cormorant Capital, Cowen Healthcare Investments, Point72 Asset Management, Irving Investors, Ascend Global Investment Fund, Cedars-Sinai Medical Center跟投。
Prometheus Biosciences
是一家美国炎性肠病治疗于诊断产品研
发
商,公司开创了一种精确医学方法,用于发现、开发和商业化用于诊断和治疗炎性肠病的新型治疗和伴随诊断产品。
公司的精密医学平台
Prometheus 360
将专有的生物信息学发现方法与胃肠道生物信息学数据库相结合,以识别新的治疗靶标并开发候选治疗剂来参与这些靶标。
近日,
Carbon Health
宣布,完成
1
亿美元
C
轮融资。本轮融资由
Data Collective
,
Dragoneer Investment Group
,
Builders VC
,
Brookfield Asset Management
投资。
Carbon Health是一家医疗信息化领域的公司,致力于在整个卫生系统中建立一个巨大的网络,将小型诊所、大中型医院于患者之间的联系变得更加紧密而简单。Carbon将虚拟护理与诊所的个人护理结合起来。通过Carbon的移动应用程序,患者可以查看健康记录,建立预约,付款或进行视频访问。

1.
礼来新冠中和抗体获FDA紧急使用授权,2020年底前将生产100万剂
2.
多款新冠疫苗公布进展
3.
复宏汉霖
新冠肺炎治疗候选药物在美国获批临床

礼来新冠中和抗体获FDA紧急使用授权,2020年底前将生产100万剂
11月9日,礼来宣布,其新冠中和抗体bamlanivimab获得美国FDA的紧急使用授权,用于治疗近期确诊的12岁以上成人和儿童轻中度高风险新冠患者,包括年龄在65岁以上或患有某些慢性病的人。Bamlanivimab于10月7日向FDA递交EUA申请,到如今获批不过一个月的时间。Bamlanivimab是礼来与AbCellera公司合作开发的用于治疗和预防COVID-19的IgG1单克隆抗体,可以直接结合SARS-CoV-2的刺突蛋白,阻断病毒黏附和进入人宿主细胞,从而起到中和病毒的作用。
信息来源:创药工坊
多款新冠疫苗公布进展
i.
辉瑞/BioNTech新冠疫苗保护效力达90%:11月9日,辉瑞和BioNTech联合宣布,双方联合开发的mRNA候选新冠疫苗BNT162b2,在3期临床试验的中期有效性分析中显示出高达90%的保护效率。对接种疫苗参与者和接种安慰剂参与者之间病例的比较表明,从第2次疫苗接种后7天开始,出现有症状的COVID-19患者人数比接种安慰剂的对照组少90%以上。这一数值显著高于FDA设定批准紧急使用授权所需的50%的疗效标准。
ii.
11月12日,Moderna宣布,其正在进行的3期临床试验COVE已经积累到足够的COVID-19病例,正在准备向独立的数据安全监查委员会递交病例数据。3期临床试验COVE旨在检验mRNA新冠候选疫苗mRNA-1273预防出现症状的COVID-19疾病的能力及其安全性。mRNA-1273是一种编码融合前稳定形态的新冠病毒刺突蛋白的mRNA疫苗,由Moderna和美国国立过敏与传染病研究所疫苗研究中心的研究者共同开发。这一候选疫苗在临床前研究和1期临床试验中均已表现出良好的安全性、耐受性、以及免疫原性。
iii.
近日,CureVac宣布,其在研疫苗CVnCoV的详细1期临床试验结果。在1期临床试验中,18-60岁的血清型阴性和阳性的志愿者相隔28天,随机接种两次候选疫苗或安慰剂。试验结果显示,CVnCoV能够剂量依赖性地诱发与刺突蛋白结合的抗体和中和抗体的产生。CVnCoV是一款无化学修饰的mRNA新冠疫苗,编码新冠病毒全长刺突蛋白。CureVac预计在2021年第一季度向欧盟EMA递交监管申请。
iv.
Arcturus候选疫苗1/2期临床结果积极:11月10日,Arcturus Therapeutics宣布,其与杜克-新加坡国立大学医学院联合开发的mRNA新冠疫苗ARCT-021在1/2期临床试验中获得积极结果。在1/2期临床试验中,总计106名21-80岁的志愿者接受了不同剂量的疫苗接种。初步试验结果显示,所有接受评估的剂量均能够剂量依赖性地激发针对新冠刺突蛋白的抗体。候选疫苗同时激发Th1主导的CD4阳性T细胞反应,和针对刺突蛋白受体结合域的CD8阳性T细胞反应。新加坡经济发展局承诺将投资4500万美元支持这一候选疫苗的生产,并且可能出资1.75亿美元购买这一疫苗。
v.
11月13日,俄罗斯流行病学和微生物学国家研究中心发布公告称,Sputnik V®的III期研究中期分析显示,Sputnik V®具有积极的有效性。在20例确诊的冠状病毒病例进行的统计分析中, Sputnik V®在接种第二剂后的有效率高达92%。在安全性方面,除了流感样症状外,没有报告过严重的不良事件,包括疲劳,头痛和发烧。西藏诺迪康药业全资子公司TopRidge Pharma 通过分期支付900万美元合作对价,获得Sputnik V®疫苗在中国大陆及港澳台地区的注册、开发、生产、进口或商业化产品及向指定区域出口等相关权益许可权。
信息来源:
药明康德,医药观澜,贝壳社,
医麦客
复宏汉霖新冠肺炎治疗候选药物在美国获批临床
11
月
6
日,复宏汉霖宣布,其自主研发的
ACE2-Fc
受体融合蛋白
HLX71
用于治疗新型冠状病毒肺炎的新药临床试验申请于近日获美国
FDA
批准。
HLX71
为复宏汉霖第二款获得美国
FDA
临床试验批准的新冠肺炎治疗候选药物。
HLX71
为
C
末端带有
IgG1 Fc
的重组人血管紧张素转换酶
2
融合蛋白,其
ACE2
蛋白可充当
“
诱饵
”
,与
SARS-CoV-2
病毒
S
蛋白的
RBD
区域结合,且具有较强的结合力,可以阻断病毒与宿主细胞表面的
ACE2
结合,防止
SARS-CoV-2
病毒感染细胞,进而用于新冠肺炎的治疗。
信息来源:
医药观澜

1.
荣昌生物
ADC
新药获
FDA
胃癌
2
期临床试验许可及快速通道资格
2.
中生尚健首个创新药获批临床,靶向
CD47
3.
全球首张心血管狭窄
AI
三类证获批
4.
诺辉健康肠癌早筛产品医疗器械注册证获国家药监局批准

荣昌生物ADC新药获FDA胃癌2期临床试验许可及快速通道资格
11月12日,荣昌生物宣布,其自主研发的靶向HER2抗体偶联药物药物注射用维迪西妥单抗获得FDA针对晚期或转移性胃癌以及胃食管结合部腺癌的2期临床试验许可。同时,FDA还授予维迪西妥单抗治疗胃癌适应症的快速通道资格。今年8月,维迪西妥单抗用于治疗局部晚期或转移性胃癌患者的有条件新药上市申请获中国国家药品监督管理局受理,这也是我国首个提交新药上市申请的自主研发的ADC新药。
信息来源:贝壳社
中生尚健首个创新药获批临床,靶向CD47
11月9日,中生尚健生物医药宣布,其向中国国家药品监督管理局药品审评中心提交的靶向CD47的SG404项目新药临床试验申请已获得批准。这是中生尚健自2020年3月成立以来的首个项目获批临床。SG404是重组人SIRPα-Fc融合蛋白,通过亲和力及结构优化,可有效阻断CD47-SIPRα信号通路,且不引起红细胞凝集。
信息来源:医药观澜
全球首张心血管狭窄AI三类证获批
11月11日,数坤冠脉CT造影图像血管狭窄辅助分诊软件获得了国家药品监督管理局颁发的医疗器械三类注册证,这是全球首张心脏冠脉狭窄AI医疗器械注册证。数坤冠脉AI基于原创的深度学习神经网络,具有10亿级别的神经元,100多项发明专利。AI能够帮助医生完成复杂的心脏图像三围重建,进而诊断出血管的起源、走形、血管壁的斑块、管腔狭窄等,可以给医生呈现管腔狭窄判断、斑块显示、斑块性质判断等数据,并自动生成结构化报告。以往,患者完成CT检查,医生需要手动完成图像重建、病灶检测、测量、报告书写等工作,耗时约40分钟左右,而这一整套流程,数坤冠脉AI仅需1分钟即可全自动完成,诊断效率呈指数级提升。
信息来源:器械之家
诺辉健康肠癌早筛产品医疗器械注册证获国家药监局批准
11月10日,诺辉健康旗下肠癌早筛产品常卫清-KRAS基因突变及BMP3/NDRG4基因甲基化和便隐血联合检测试剂盒医疗器械注册证正式获批。该试剂盒体外定性检测人粪便样本中的KRAS基因突变、BMP3和NDRG4基因甲基化及血红蛋白,用于对肠镜依从性差的结直肠癌高风险人群的筛查。该产品不能替代肠镜,不能用于普通人群的肿瘤筛查,临床诊断过程中不应以本产品检测结果作为临床诊断的唯一依据。

1.
辉瑞
JAK
抑制剂达到
3
期临床终点,有望斩获第
5
个适应症
2.
信达生物及康方生物公布
CD47
单抗进展
3.
Five Prime Therapeutics FGFR2b
靶向疗法
2
期临床结果积极
4.
mRNA
癌症疫苗
/Keytruda
组合早期临床结果积极
5.
臻和
MRD
检测震撼上市

辉瑞JAK抑制剂达到3期临床终点,有望斩获第5个适应症
11月8日,辉瑞宣布,其口服小分子JAK抑制剂托法替尼在一项治疗活动性强直性脊柱炎成人患者的3期临床试验中达到主要和关键性次要终点。FDA已经接受辉瑞为托法替尼递交的补充新药申请,预计在明年第二季度做出回复。如果获批,将是托法替尼斩获的第5个适应症。托法替尼可以有效抑制JAK1和JAK3的活性,阻断多种炎性细胞因子的信号传导。已经获得FDA批准治疗四种适应症,包括类风湿性关节炎、银屑病关节炎、溃疡性结肠炎成人患者,和2岁以上多关节型幼年特发性关节炎患者。
信达生物及康方生物公布CD47单抗进展
i.
11月11日,信达生物制药宣布,其CD47单抗Letaplimab在美国开展的单药治疗晚期恶性肿瘤的1a期临床研究结果。本研究共入组20例受试者,Letaplimab完成了所有预设剂量的爬坡,各剂量组均未发生剂量限制性毒性,整体耐受性良好。无导致永久停药的药物相关不良反应,无治疗相关死亡发生。Letaplimab单药也在此项研究中观察到了一定的抗肿瘤活性。Letaplimab以CD47为靶点的重组全人源IgG4单克隆抗体,增强巨噬细胞对肿瘤细胞的吞噬,并促进了T细胞的交叉激活。
ii.
近日,康方生物披露,其第二代CD47抗体AK117的人体临床研究进展。AK117在已完成和正在进行的剂量爬坡队列受试者中均未发生药物相关的贫血症状,因此无需使用低剂量诱导。各队列受试者对药物耐受性良好,无剂量限制性毒性事件发生。AK117在保留抗肿瘤活性的同时,消除了红细胞凝集作用,并显著降低其介导的巨噬细胞对红细胞吞噬活性,展示出了区别于其它抗CD47抗体药物的差异化特征。
信息来源
:医药合作投融资联盟,医药魔方
Five Prime Therapeutics FGFR2b靶向疗法2期临床结果积极
11月11日,Five Prime Therapeutics宣布,其“first-in-class”靶向FGFR2b的单克隆抗体疗法bemarituzumab,与化疗联用,在一线治疗晚期胃癌或胃食管连接部癌FGFR2b阳性,HER2阴性患者的2期临床试验中获得积极结果。Bemarituzumab与化疗联用,与化疗相比,将这些患者的死亡风险降低42%。Bemarituzumab具有双重作用机制,不但可以通过与FGFR2b结合,阻断其介导的生长因子的信号传导,而且可以通过抗体依赖性细胞介导的细胞毒作用杀伤癌细胞。再鼎医药已经与Five Prime达成合作协议,获得这款创新疗法在大中华区的开发权益,并负责该药物在大中华区的临床试验。
信息来源:药明康德
mRNA癌症疫苗/Keytruda组合早期临床结果积极
11月12日,Moderna宣布,其个体化癌症疫苗mRNA-4157与默沙东免疫检查点抑制剂Keytruda联用在早期临床试验中获得积极结果。在治疗HPV阴性的头颈部鳞状细胞癌患者的1期临床试验中,达到50%的总缓解率和9.8个月的中位无进展生存期。mRNA-4157与Keytruda联用,个体化癌症疫苗能够激发免疫系统的T细胞反应,而免疫检查点抑制剂能够消除肿瘤对T细胞的免疫抑制,这两种疗法的组合有望产生协同效应,增强抗癌效果。这一结果进一步展示了mRNA疫苗在预防传染病以外,治疗癌症方面的潜力。
信息来源:药明康德
臻和MRD检测震撼上市
11月7日,臻和科技于CSCO臻和精准治疗高峰论坛上推出其MRD检测。MRD检测是基于臻和MinerVa平台,主要针对肺癌I-III期接受非姑息性手术的患者,行肿瘤循环DNA检测,进行肺癌术后复发风险评估,帮助临床医生对患者进行更加个体化和精准的治疗方案和策略的选择。
信息来源:臻和基因

1.
诺禾致源科创板首发过会
2.
微创医疗分拆上市
3.
美敦力最新脊柱手术机器人
“
中国首秀
”
,达芬奇迎强劲对手

11月10日,北京诺禾致源科技科创板首发过会。据其最新招股书显示,本次发行前总股本36,000万股,本次公开发行股票不超过4,020万股,本次公开发行不进行股东公开发售,且公开发行股票的总量占公司发行后总股本的比例不低于10%。诺禾致源主要依托高通量测序技术和生物信息分析技术,建立了通量规模领先的基因测序平台,并结合多组学研究技术手段,为生命科学基础研究、医学及临床应用研究提供多层次的科研技术服务及解决方案;同时,基于在基因测序及其应用领域的技术积累,自主开发创新的基因检测医疗器械。
信息来源:IVD资讯
11月
6日,微创医疗建
议分拆微创心通医疗科技有限公
司已向联交所递交上市申请表格。
微创心通主要从事研发、制造及销售治疗瓣膜性心脏病的器械业务。
微创医疗有7大板块业务,包括心血管介入产品业务、心律管理业务、骨科医疗器械业务、大动脉及外周血管介入产品业务、神经介入产品业务、外科医疗器械业务、心脏瓣膜业务。
微创心通主要从事研发、制造及销售治疗瓣膜性心脏病的器械业务。
根据微创医疗2020年半年报显示,上半年心脏瓣膜业务实现营收520万美元,折合人民币约3,400万元,占总营收1.7%,超越外科医疗器械业务成为微创医疗的第六大业务版块。
美敦力最新脊柱手术机器人“中国首秀”,达芬奇迎强劲对手
近日,美敦力的Mazor X Stealth Edition智能脊柱外科手术机器人系统于第三届进博会亮相,这是该款机器人系统在中国的首次公开亮相。
Mazor X Stealth Edition脊柱外科手术定位与导航系统能为脊柱外科医生提供涵
盖术前规划与模拟、精确的手术入路引导和实时可视化信息的全流程支持,并支持常规开放手术、微创手术以及复杂侧弯手术等多种脊柱外科手术类型,帮助医生实现更精准、安全、高效的手术目标。
Mazor X StealthTM Edition目前已在海外市场进行了超4.5万台手术,为患者植入了20多万颗螺钉。
这款产品有望于明年登陆国内市场。
○
医疗与生命科技资本市场本周动态一览:
近期交易概况(2020年11月09日-11月12日)

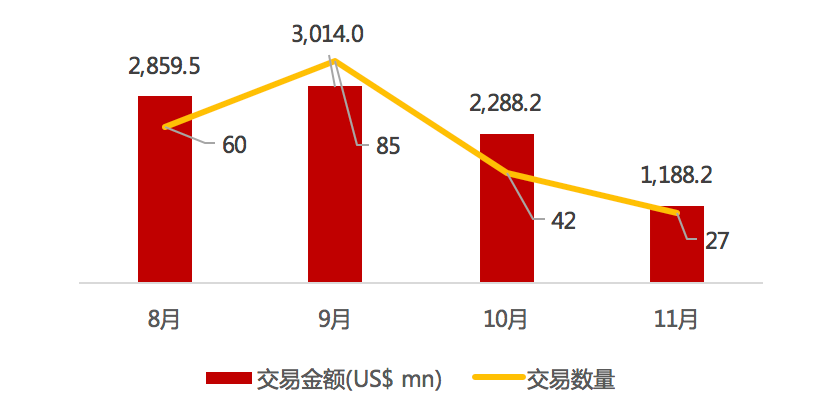
* 数据来源:华兴资本内部整理
上市公司市值及估值倍数一览
(2020年11月13日)市值单位:百万美元

< < 左右滑动图片查看完整表格 > >

















