众所周知,肿瘤细胞素来狡猾,擅长伪装,极易躲避T细胞的“扫描系统”。它们的首要目标就是成功潜伏于机体的免疫系统之中,为此它们可以无所不用其极。
其中,结盟T细胞表面的PD-1分子,便是策反T细胞的重要手段之一,以此可使得骁勇善战的T细胞顿时变得萎靡不振、疲顿不堪。
因而,衰竭T细胞的缴械投降也使得免疫系统兵败如山倒,只能任由肿瘤细胞在机体之中兴风作浪。
那么为了在与肿瘤的激烈鏖战中吹起胜利的号角,重振T细胞的雄风就是迫在眉睫的事情。显然,近年来通过破坏PD-1/PD-L1的联盟,可使得T细胞重新变得生龙活虎,发挥出其应有的威力。
但遗憾的是,即便如此,该法并不能“唤醒”所有患者的T细胞。因而,研究者们也一直在寻找背后的原因以及克服的方法。
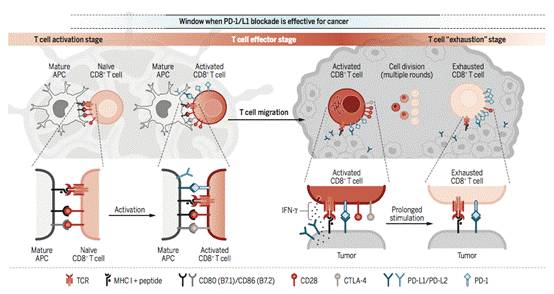
但近日Science发表的两篇文章表明,即使PD-1牵制的“刹车系统”被释放,肿瘤特异性T细胞仍需要其他“染料”来扩大其队伍,修复有效的免疫反应。而这一“染料”就来自于T细胞共刺激因子CD28。

其实,T细胞活化需两种信号:TCR信号和共刺激因子信号(如CD28),而T细胞表面还存在着共抑制因子(如PD-1),可作为免疫检查点维持着免疫稳态。
目前学术界普遍认为PD-1阻断主要通过抑制TCR信号转导来逆转衰竭T细胞(进行性功能丧失),而不是在T细胞应答的激活和效应阶段。
可现在越来越多的证据表明,除此之外,PD1阻断还能靶向未衰竭的T细胞,且其在T细胞应答的早期阶段及免疫监视过程中也发挥了一定的作用。
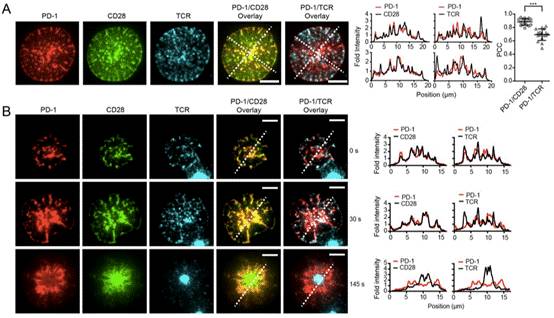
Hui等研究者首先通过TIRF显微镜发现,在PD-1与PD-L1相互作用的30s内,CD28与PD-1会在TCR附近短暂的向心聚集成簇,有利于活化的PD-1对CD28的去磷酸化作用。
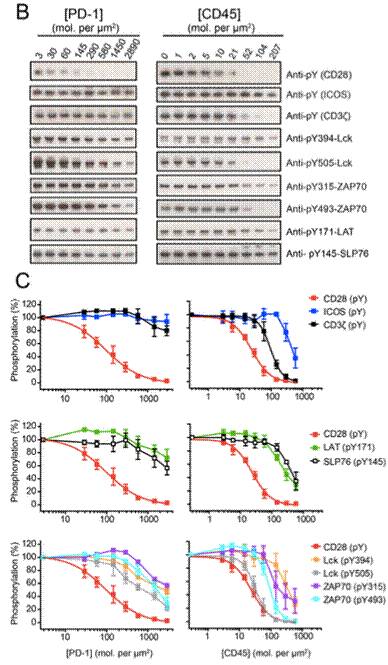
随后他们构建了无细胞生物重建系统证明了,PD-1与PD-L1的结合可导致PD-1细胞质结构域中的两种酪氨酸(Y224和Y248)在激酶Lck的作用下磷酸化,进而募集了细胞溶质酪氨酸磷酸酶SHP2来使PD-1本身以及CD28去磷酸化,进而可终止CD28信号传递并调节免疫抑制功能。

接着,他们鉴定了PD-1结合磷酸酶SHP2的直接靶标,并发现相比于TCR,CD28会成为PD-1阻断后的优选靶标,其次便是能磷酸化TCR、CD28和PD-1的酪氨酸激酶Lck。
另外,在完整的细胞体系中,相较于TCR,也是CD28在PD-1活化中优先被去磷酸化,反映出PD-1主要通过灭活CD28信号来抑制T细胞的功能。
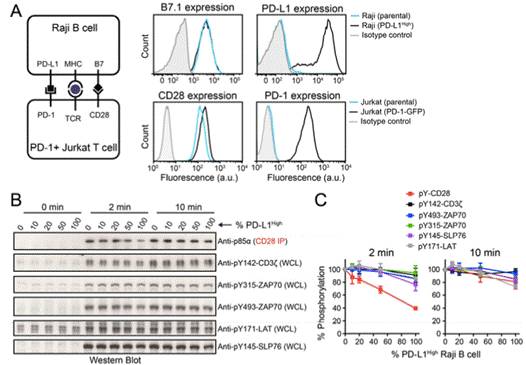
因而,在本文研究中证实了
PD-1活化后可直接靶向CD28的胞质区域,且具有比T细胞受体下游分子更高的亲和力,进一步强调了CD28和PD-1通路之间的相互作用




