▎药明
康德/报道
1. 人工智能加速“渐冻人症”研究
ALS也称渐冻人症和Lou Gehrig病,是由中枢神经系统内控制骨骼肌的运动神经元退化所致,患者的肌肉逐渐衰弱和萎缩,大脑渐渐丧失控制随意运动的能力,最终导致呼吸衰竭和死亡。该疾病最著名的患者可能是《时间简史》的作者、英国物理学家史蒂芬·霍金(Stephen Hawking)博士。全球每年约有14万个新发病例确诊,却没有药物能治愈这种疾病。美国食品和药物管理局(FDA)只批准过两种药物用以减缓ALS的进展,一种在1995年上市,
另一种则是在今年刚刚获批
。

▲英国物理学家史蒂芬·霍金是一名ALS患者(图片来源:REUTERS)
近日,在开发肌萎缩性脊髓侧索硬化症(ALS)治疗的赛场上,人工智能也加入了角逐。英国的Sheffield神经科学转化研究所(Sheffield Institute for Translational Neuroscience)采用人工智能(AI)来加速药物开发进程并取得初步成果。通过分析巨大的化学、生物和医学数据库以及科学论文,AI提炼出新的生物靶点和潜在的药物。
由AI找到的一个候选化合物在临床前测试中效果良好,有望防止运动神经元细胞的死亡,从而推迟疾病发作。
该研究所的Richard Mead博士打算在12月的医疗会议上介绍研究结果,目前正在计划临床试验。
无独有偶,美国亚利桑那州的Barrow Neurological Institute在去年使用IBM的超级计算机Watson发现了与ALS相关的5个新基因,仅仅用了数月时间。还有数家公司也在进行AI辅助的药物开发,美国马里兰州的InSilico Medicine最近还推出了专门针对ALS的药物发现平台。虽然AI机器人尚不会取代科学家和医生,但他们可以采用比传统方法快几倍的方式来寻找药物,节省研发时间和成本。
2. MyndYou利用AI技术检测阿兹海默病患者的言语模式变化
生物技术公司MyndYou开发了一种人工智能(AI)诊断工具,
来远程跟踪并自动检测阿兹海默病(AD)患者言语模式中的微妙变化。
他们正在与麻省总医院(Massachusetts General Hospital, MGH)合作进行测试。目前缺乏用于了解患者认知行为变化的客观数据,这项技术是为了把数据收集变成患者日常生活的一部分。
原发性进行性失语(PPA)这种神经退化性语言障碍经常与额颞叶退变(FTLD)或阿兹海默病相关。 PPA症状通常是定性评估的,但许多临床医生认为评估方式还有改善空间。这项研究旨在开发出能更客观有效地评估PPA和AD的方法。
▲MyndYou收集患者日常活动数据进行多维度认知分析,希望提供个性化疗法(图片来源:MyndYou官网)
AD患者将每周打电话到评估中心与研究人员进行短暂对话。AI会记录患者的声音,并从与认知变化相关的角度分析其言语模式。收集的参数还可以包括其他日常活动的信息,比如睡眠。MGH正在利用MyndYou的平台测试一些可定量的评估选项,这能够提高筛查的准确性,而且能客观地检测细微的认知变化,并根据结果调整护理方式。MyndYou相信,这种技术为住家患者提供个性化护理,使出现认知变化的成年人保持自理的时间更长久。
MyndYou希望最终能协助制药公司开发治疗AD的药物。
3. 礼来的偏头痛新药lasmiditan达到3期临床试验终点
礼来(Eli Lilly)近日宣布,其在研的
急性偏头痛新药lasmiditan在第二期3期临床试验SPARTAN中达到研究的主要终点和关键次要终点
。这些结果与第一期关键3期临床试验SAMURAI的结果一致。礼来计划于2018年第二季度向美国FDA提交lasmiditan的新药申请。
偏头疼是一种神经系统疾病,表现为反复发作的严重头疼,并伴有恶心、呕吐、对声光敏感、视力变化等症状。超过3600万美国人有偏头疼,其中女性的发病率要高于男性三倍。但到目前为止,这一领域还有很大的医疗需求未被满足。
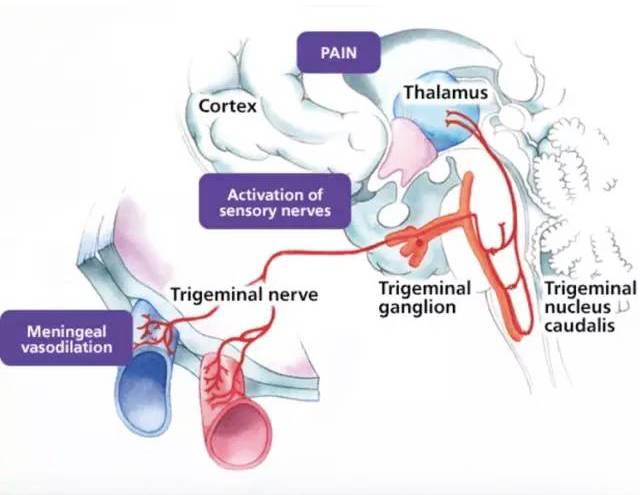
▲Lasmiditan的作用机理(图片来源:CoLucid官网)
Lasmiditan可以在三叉神经通路中选择性靶向5-HT1F受体,用于快速治疗偏头疼,但没有偏头疼治疗相关的血管收缩。它的作用在临床试验中得到了验证。SPARTAN是第二期3期临床试验,评估三种剂量(50 mg、100 mg和200 mg)的lasmiditan快速治疗偏头疼的安全性和疗效。在第一次用药后2小时内,服用lasmiditan的患者中有更多的人偏头疼症状缓解,这一结果与对照组相比,在所有三个剂量组中都有统计学上的差异,到达了主要终点。 此外,服用lasmiditan的患者中有更多的人在第一次用药后2小时内出现最困扰的症状(MBS)的缓解,到达了关键次要终点。
“Lasmiditan代表了20年来急性治疗偏头疼领域的首个重大创新,可以为3600万有偏头疼的美国人提供急需的治疗新选择,”礼来生物医药总裁Christi Shaw女士说。
相关阅读:速递 | 礼来大手笔,近十亿美元收购偏头痛公司
4. 多动症新药ORADUR-Methylphenidate ER在台湾进行的3期临床试验结果良好
日前,DURECT公司宣布其合作伙伴友霖生技医药 (Orient Pharma Co., Ltd.) 在台湾地区进行的ORADUR-哌甲酯-ER (ORADUR- Methylphenidate-ER) 治疗多动症的临床3期试验获得积极结果。

多动症(attention deficit hyperactivity disorder, ADHD)是一种较为常见的神经性行为疾病,在美国它影响到500万年龄3~17岁儿童的生活。
多动症的主要特征为注意力不集中,过度活动和冲动。这些症状通常在患者为儿童时出现,但是在有些患者身上可以持续一生。
在美国,大约50%的多动症患者接受药物治疗,其中安非他明 (amphetamine) 或哌甲酯一类的兴奋剂是常用的一线疗法。但是根据2010年全国药物使用与健康调查(National Survey on Drug Use & Health) 估计,大约有110万超过12岁的美国人会滥用这些药物来获得快感或者提高表现。
ORADUR-哌甲酯-ER胶囊是DURECT公司开发的治疗多动症的新药。这种药物在药物释放技术上有创新,
一方面延长药物的释放时间
,让患者每日只需服用一粒胶囊;
另一方面在药物的封装形式上加入了防止被滥用的防范措施
。友霖生技医药于2009年从DURECT公司获得在某些亚洲和南太平洋国家开发与销售ORADUR-哌甲酯-ER胶囊的许可。
在台湾进行的这项多中心,随机双盲,含安慰剂对照的双向交叉临床3期试验中,110名年龄为6~18岁的儿童接受了治疗,其中99名儿童完成临床试验。根据SNAP-IV量表对儿童多动症症状的评估,
ORADUR-哌甲酯-ER胶囊的疗效显著优于安慰剂
(在意向治疗患者群中p=0.0044)。同时在这项临床试验中没有出现严重的副作用。友霖生技医药对药物安全性的分析表明ORADUR-哌甲酯-ER胶囊的安全性与其它治疗多动症的药物相当。
相关阅读:速递 | 3期试验结果积极!多动症新药有望上市
参考资料:
[1] How AI robots hunt new drugs for crippling nerve disease
[2] Startup MyndYou using AI to treat Alzheimer’s disease
[3] Lilly announces positive results for second Phase 3 study of Lasmiditan for the acute treatment of migraine
[4] DURECT (DRRX) Release: ORADUR-Methylphenidate ER capsule achieves primary endpoint in Phase III study in ADHD in Taiwan







