正文
abstract
齐鲁制药和福建广生堂的富马酸替诺福韦二吡呋酯获批上市
据米内网MED药品审评数据库统计,5月份CDE新增药品注册申请419个,较上月有所回升。
2017年1-5月CDE新增药品注册申请情况(按受理号计)
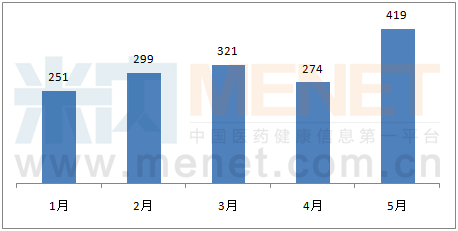
(数据来源:米内网MED药品审评数据库,如无说明,下同)
从申请类型看,5月份新药申请与仿制申请数量回归年内平均水平,进口申请则连续第二个月下滑。
2017年1-5月各申请类型新增药品注册申请情况(仅统计新药、仿制和进口)
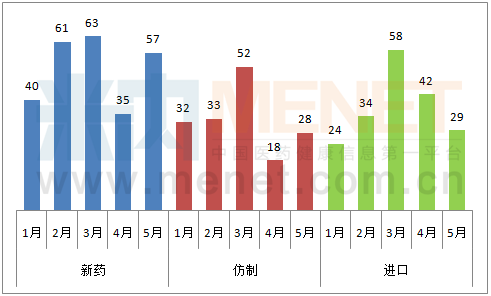
国内新药申报:恒瑞医药4个1类新药进入CDE 均为国内首家
据米内网MED药品审评数据库,2017年5月新增新药申请57个,其中属于1类新药的申请有39个,涉及19个品种。重组埃博拉病毒病疫苗完成临床试验阶段后在本月申报生产,恒瑞医药在本月有4个1类新药进入CDE,分别是注射用SHR-A1403、SHR7280原料药及其片剂、SHR9146原料药及其片剂和SHR0532原料药及其片剂。下面是5月部分新增1类新药的简介:
注射用SHR-A1403是一种人源化抗c-Met单克隆抗体,恒瑞医药在1月份公布了该品种通过美国FDA审批进入临床,据了解目前国内外尚无已上市的同靶点的同类型产品。
SHR7280是一种促性腺素释放激素(GnRH)拮抗剂,用于治疗子宫内膜异位。
SHR9146是一种IDO抑制剂,据了解IDO在多种肿瘤细胞及抗原提呈细胞中高表达,通过调节机体色氨酸和代谢产物水平发挥免疫调节功能,是肿瘤免疫疗法中重要的小分子调控靶点。恒瑞医药也在5月初公布SHR9146通过美国FDA审批进入临床。
RO7049389是罗氏研发(中国)有限公司申报的1类新药,该品种是一种HBV衣壳蛋白装配抑制剂,用于治疗乙肝。
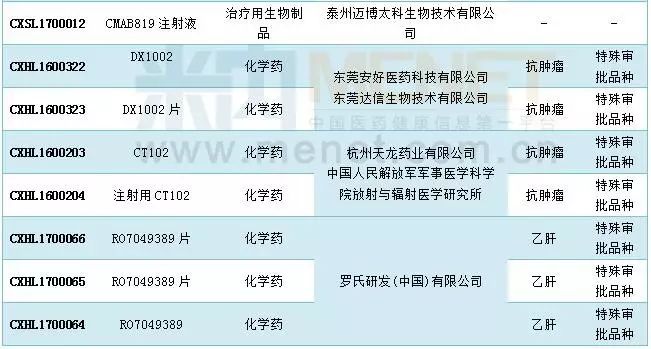
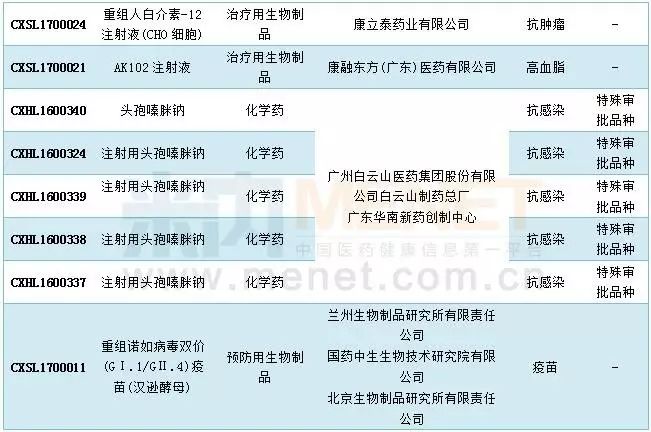
2017年5月国内1类新药申报情况
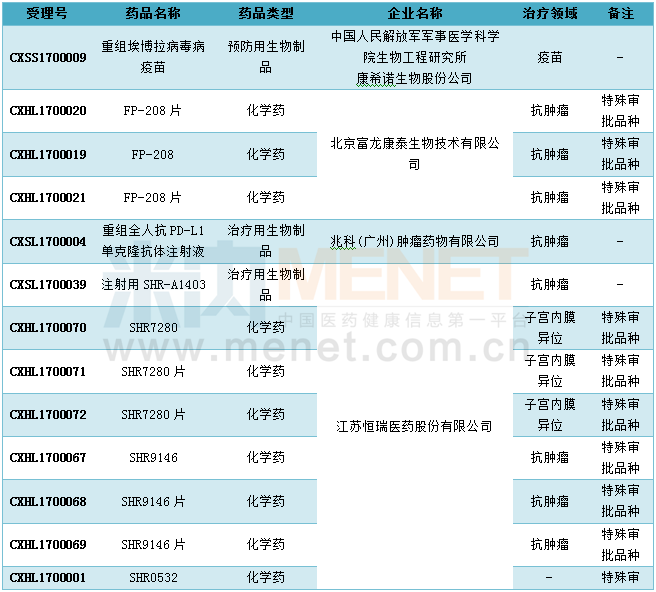
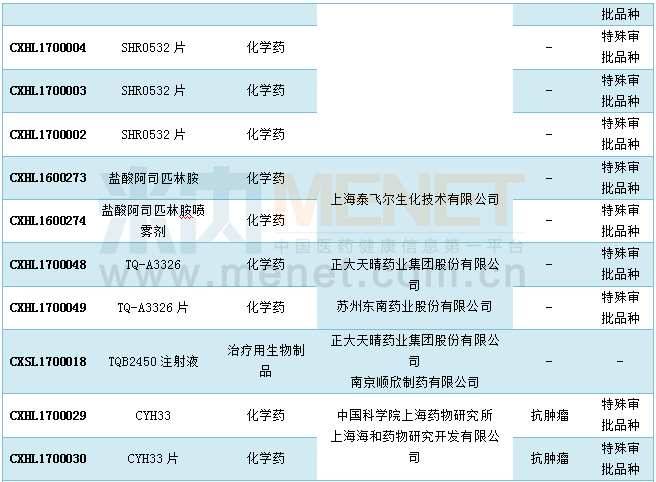
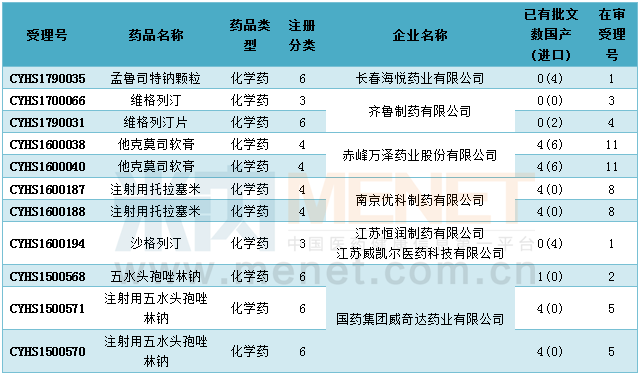
5月国内仿制申请为28个,比上月有所回升。据米内网MID药品索引数据库统计,在5月进入CDE的仿制申请中维格列汀原料药在国内尚无相关生产批文,此外孟鲁司特钠颗粒、维格列汀片、沙格列汀原料药、五水头孢唑林钠原料药及其注射剂、丁苯酞氯化钠注射液、注射用阿扎胞苷、利奈唑胺片、盐酸莫西沙星片、替格瑞洛片以及吉非替尼原料药等10个品种目前在国内均为独家品种。
2017年5月国内仿制申报情况
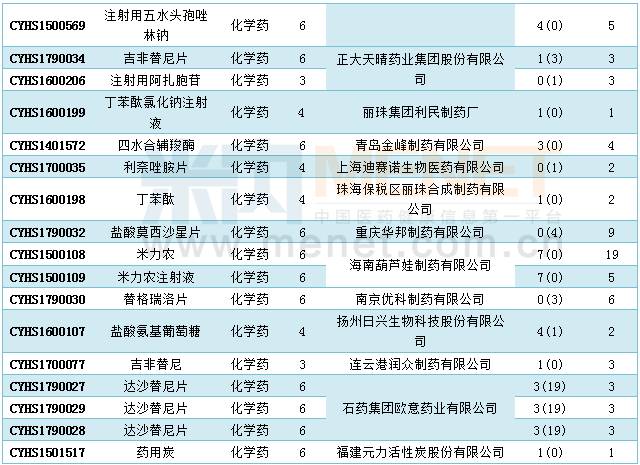
(批文数统计至2017年5月31日)
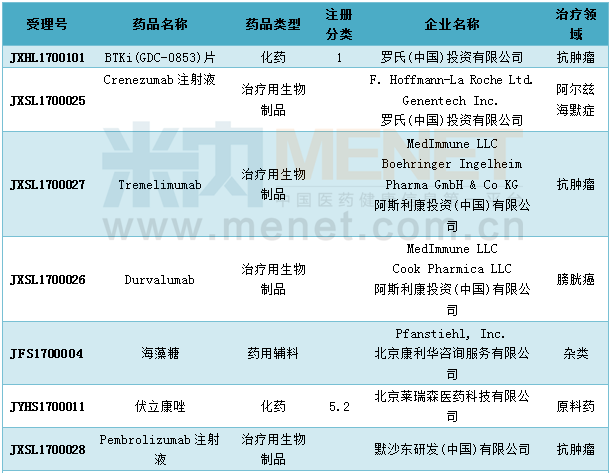
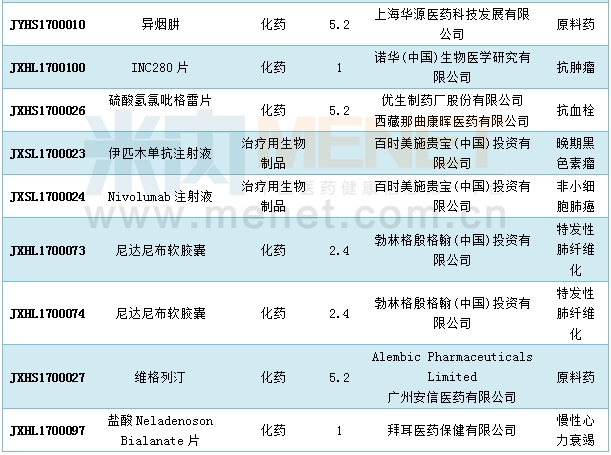
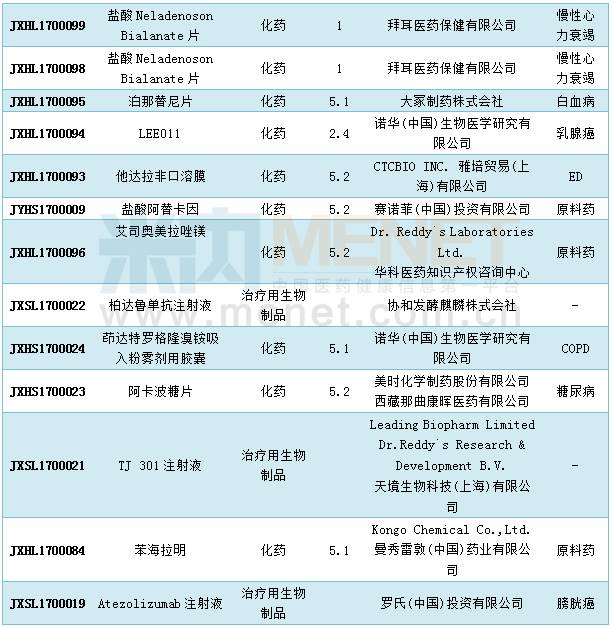
5月份CDE新增进口申请29个,涉及26个品种,以5类的申请较多,其中有3个1类新药申报临床,分别是BTKi(GDC-0853)片(罗氏)、INC280片(诺华)和盐酸Neladenoson
Bialanate片(拜耳)。
资料显示,GDC-0853是Genentech公司发现的一种新型BTK抑制剂,用于抗肿瘤治疗。诺华申报的INC280是一种高选择性口服小分子Met抑制剂,用于抗肿瘤治疗。盐酸Neladenoson Bialanate片是一种高选择性的腺苷A1受体部分激动剂,研发用于治疗慢性心力衰竭。
2017年5月进口申报情况
获批情况:两个厂家的富马酸替诺福韦二吡呋酯获批生产
据米内网统计,5月份有两个厂家的富马酸替诺福韦二吡呋酯获批生产,分别是齐鲁制药的富马酸替诺福韦二吡呋酯原料药及其片剂、福建广生堂的富马酸替诺福韦二吡呋酯胶囊剂。
替诺福韦是全球最新一代抗乙肝病毒药物,被世界各国慢性乙肝防治指南一致推荐为治疗慢性乙肝的一线用药。此前富马酸替诺福韦二吡呋酯在国内只有原料药批文和片剂批文,胶囊剂未有相关批文,且国内生产厂家成都倍特批准的适应症为抗HIV治疗。
本次福建广生堂获批的富马酸替诺福韦二吡呋酯胶囊适应症为乙肝感染,而齐鲁制药也成为继成都倍特药业和吉利德之后在国内第三家同时拥有该品种原料药批文和片剂批文的厂家,齐鲁制药获批的富马酸替诺福韦二吡呋酯片暂无确切适应症信息。值得注意的是成都倍特药业在本月也获得富马酸替诺福韦二吡呋酯片的补充申请批件,结合成都倍特药业富马酸替诺福韦二吡呋酯片之前的相关申报以及临床试验登记信息,此补充申请批件可能就是增加乙肝感染的适应症。
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。
投稿及报料请发邮件到[email protected]
商务及内容合作可联系QQ:412539092















