2006年,基于与参考药物(Genotropin®,辉瑞)相当的质量,安全性和有效性,欧洲药物管理局(EMA)将Omnitrope®批准为重组人生长激素(rhGH)的生物仿制药。在几项持续的批准后研究中,研究者继续收集生物仿制药rhGH的长期疗效资料。有意义的主题包括基于外推的适应症的疗效,以及当患者从其他rhGH产品改用生物仿制药rhGH治疗时,是否影响生长激素治疗的效果。来自临床开发研究和批准后10年的经验数据证实了生物仿制药rhGH在所有批准适应症中的临床疗效和有效性。此外,从欧洲获得批准的生物仿制药rhGH的十年经验确定了生物仿制药审批程序的科学有效性和批准过程。外推适应症的临床效果以及从其他rhGH改用生物仿制药rhGH的影响,这些担忧已缓解。对于需要rhGH治疗的儿童,生物仿制药rhGH是一种有效治疗方案。
生长激素(GH,生长激素)是一种有效的代谢激素,在脂质,碳水化合物和蛋白质的代谢过程中有重要作用。对于缺乏内源性GH的儿童,使用GH替代疗法可刺激线性生长并增加生长速度。GH治疗也被批准用于其他适应症,如Turner综合征(TS)和Prader-Willi综合征儿童(PWS),胎龄较小的矮小儿童(SGA)和慢性肾功能不全儿童。在所有儿科适应症中,早期诊断和GH起始治疗对优化治疗效果至关重要。在成人和儿童中,生长激素通过增加氮保留、刺激骨骼肌生长以及通过动用身体脂肪维持正常的身体组成。
自1985年以来,临床上已在使用GH重组人生长激素(rhGH)的替代疗法。2006年,基于与参考药物(Genotropin®,辉瑞)相当的质量,安全性和功效,欧洲药品管理局(EMA)批准了Omnitrope®(生物仿制药rhGH; Sandoz,Kundl,
Austria
)。在几项持续的批准后研究中,研究者继续收集生物仿制药rhGH的长期疗效资料。有意义的主题包括基于外推的适应症的疗效,以及当患者从其他rhGH产品改用生物仿制药rhGH时是否会影响GH治疗的效果。本文回顾了生物仿制药rhGH在其临床开发计划和上市后临床应用10年中的疗效。
Omnitrope开发计划的临床研究摘要见表1。生物仿制药rhGH的III期临床开发计划的目的是证明其与参考药物的疗效和临床可比性。AQ研究是一项在患有生长激素缺乏(GHD)的儿童(n=89)中开展的多中心,随机,对照,开放式的III期研究。该研究旨在比较生物仿制药rhGH与参考药物的疗效和安全性,并评估了生物仿制药rhGH的长期(7年治疗)疗效和安全性。评估的效果参数包括身高,身高标准差积分(HSDS),年生长速率(HV)和年生长速率标准差积分(HVSDS)。9个月的治疗期证明了生物仿制药rhGH与参考药物的临床可比性。
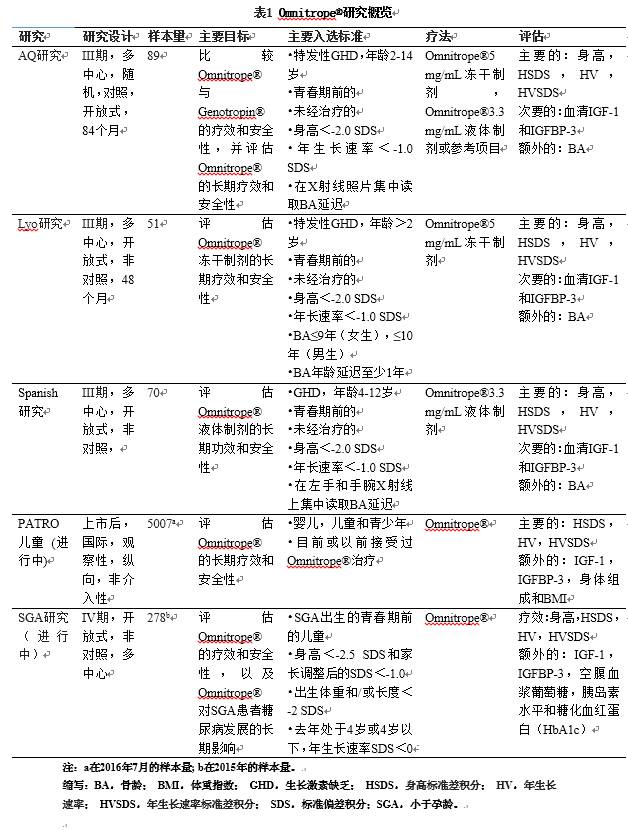
例如,在9个月后,生物仿制药rhGH和参考药物在平均HV的基线调整差异为-0.20 cm/年(95%置信区间[CI]:-1.34,0.94),平均HVSDS为0.76(95%CI: - 0.57,2.10)。生物仿制药
rh
GH还显示出长期功效(长达7年),即在基线和治疗结束之间的所有四个参数都观察到显著改善。
第二项研究(Lyo研究)是对患有GHD的儿童(n=51)中生物仿制药rhGH 5mg/mL冻干制剂的非对比研究。评估的主要效果参数是身高,HSDS,HV和HVSDS。通过基线的效果参数的统计学显著增加证明了生物仿制药rhGH的疗效。对每一个,平均差异在基线和所有后续访问之间具有统计学意义(长达48个月;表2)。
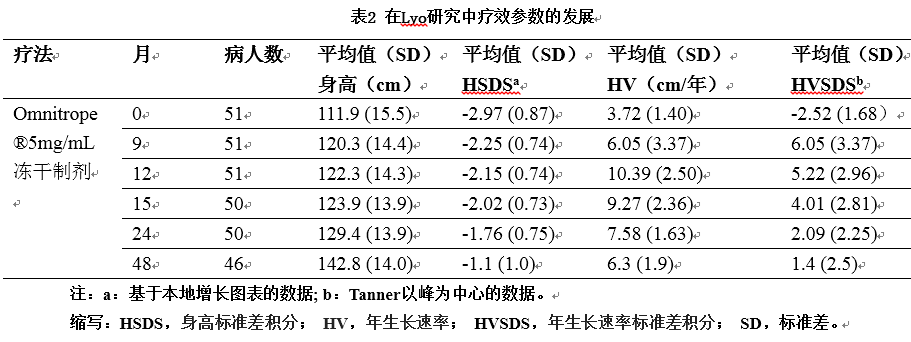
第三项研究评估了长期(长达5年)在患有GHD的儿童(n=70)中使用3.3 mg/mL液体制剂生物仿制药rhGH 治疗的疗效和安全性。4年后,记录的这些值明显增加(与基线相比):平均身高(31.1cm [95%CI:29.6,32.6]),HSDS(1.42 [95%CI:1.13,1.70]),HV(2.4cm [95%CI:1.7, 3.1])和HVSDS (3.5 [95%CI:2.7,4.3])。5年后,继续给仍在生长的患者提供治疗(如通常的临床实践),并持续监测以确定成年身高(n=39)。评估所有辅助参数的结果(身高,HSDS和HV)表明,rhGH治疗引起阳性生长反应并导致身高参数的标准化。在最初的III期试验中,预计的最终身高值的平均身高增益为12-18厘米,导致女性的最终成年身高为157.7厘米,男性为167.5厘米。治疗延长期结束时,女性的平均身高增加为11.6厘米,男性的平均身高增加为18.9厘米,女性的平均成年身高达157.6厘米,男性为165.5厘米。
生物仿制药rhGH的一些批准后研究正在进行中,并继续为儿科GHD和基于外推的适应症中的生物仿制药rhGH提供数据。于2006年开始,对使用Omnitrope®治疗(PATRO)的患儿进行研究,这是一项持续的长期上市后监督(PMS)计划;生物仿制药rhGH的长期疗效是次要目标。截至2016年7月,已有5007名患者参加了PATRO儿童研究;用生物仿制药rhGH治疗的平均(标准差[SD])持续时间为32.4(22.8)个月。大多数患者患有GHD(n=2854,57%);相当多的患者还诊断出SGA(n=1280,26%),TS(n=228,5%)和PWS(n =154,3%)。使用生物仿制药rhGH进行长达4年的治疗明显改善了所有适应症的生长参数;正如所料,初治患者的身高增益比预处理的患者更多(参见图1中的例子——GHD和SGA)。不同适应症的结果也是阳性的。例如,在入选GH的初治TS患者中,HSDS从基线的-3.05提高至4年的-1.77。在初治的PWS患者中,HSDS从-1.60提高到-0.39。
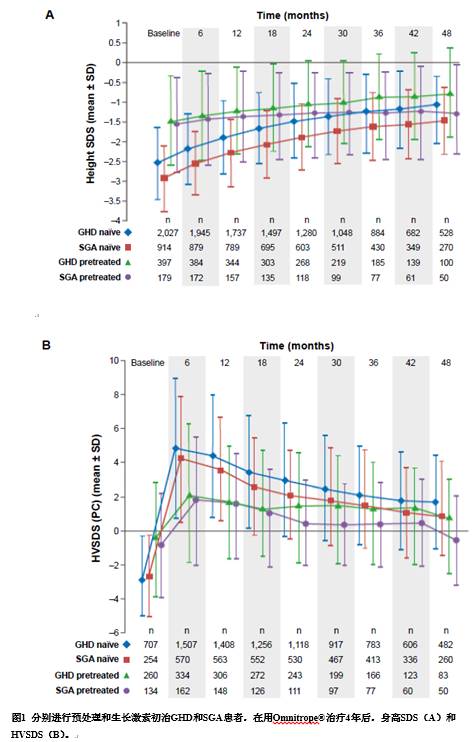
生物仿制药rhGH另一项正在进行的研究是对SGA患者进行的rhGH的最大前瞻性临床研究。这项IV期研究始于2007年,已招募了278名儿童,其中249名儿童完成了2年治疗。用生物仿制药rhGH治疗是有效的;平均HSDS基线为-3.39,治疗1年为-2.57,治疗2年为-2.15。平均HVSDS(以峰为中心)也从基线的-2.13提高到1年的+4.16和2年的+2.23。
将来自三个III期研究(介入),SGA儿童(介入)的
IV期
研究和PATRO儿童PMS(观察)的数据汇总用于各种疗效分析。这种混合疗效群体包括所有诊断为GHD和SGA的患者,在治疗6个月后具有可评估的身高评价;对于PATRO儿童,仅包括GH初治的受试者。在每个原始研究使用生长参数进行计算(尽可能使用局部生长指标)。
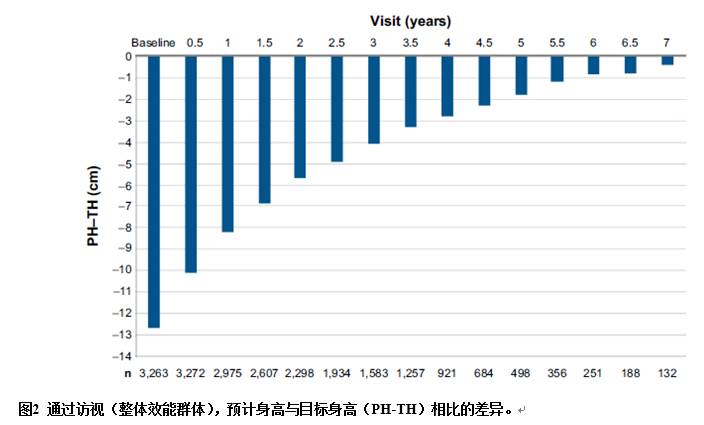
在研究中还计算了预测身高和目标身高。在III期研究(合并),SGA IV期研究和PATRO儿童中,还分别分析了生长参数。混合疗效群体包括3582名受试者(3103名来自PATRO儿童,273名来自SGA IV期研究,206名来自III期研究)。如图2所示,整个混合疗效群体的预测身高减去目标身高,显示出用rhGH治疗的好处。在治疗开始时,预测身高与目标身高之差为-12.6厘米;经过7年的治疗,差异只有-0.4厘米。
在介入和观察(PMS)研究中,受试者之间生长参数的比较如图3(GHD)和图4(SGA)所示。示例为基线在7-9岁(青春期前)的患者。来自PATRO儿童观察研究的数据证实了介入性研究报告中生物仿制药rhGH的疗效。
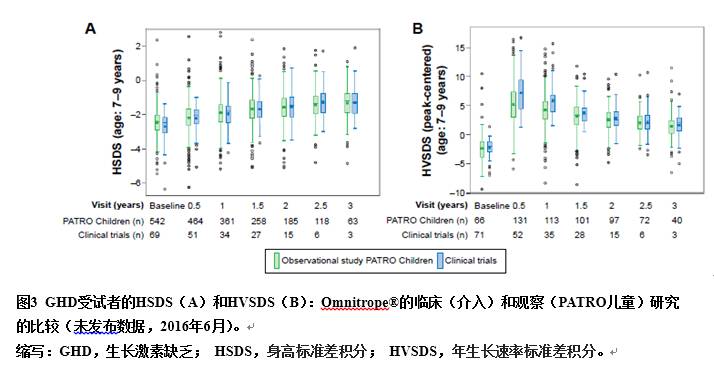
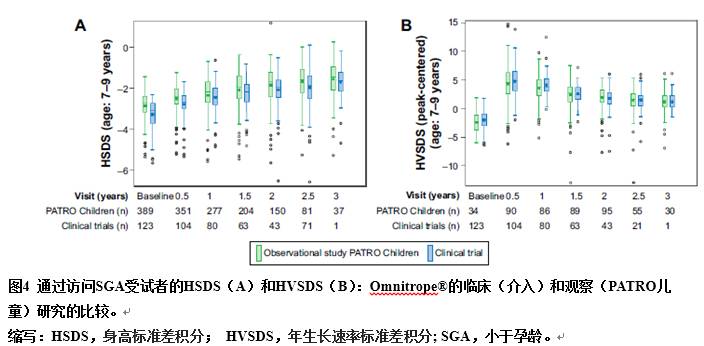
通过对III期临床资料的分析,研究者评估了从参考药物rhGH转变为生物仿制药rhGH的疗效以及安全性的影响。从参考药物改用生物仿制药rhGH,对疗效无负面影响;正如所料,对于用生物仿制药rhGH连续治疗的儿童,对IGF-I和IGFBP-3的生长结果和影响仍在继续,而且没有显著差异。
使用综合数据库进行的回顾性研究,调查了在常规临床护理期间,从非生物仿制药rhGH制剂改用生物仿制药rhGH治疗的患者的有效性,这些患者为患有GHD、特发性身材矮小(ISS)和TS的儿童(n=103)。rhGH治疗患者的生长行为没有受到改用生物仿制药rhGH的负面影响,生长速率与换药前的预期保持一致。
临床开发研究和批准后10年的经验数据证实了生物仿制药rhGH在所有批准适应症中的临床疗效和有效性。自欧洲批准以来,生物仿制药rhGH的十年经验肯定了生物仿制途径和批准过程的科学有效性。外推适应症的临床效果以及从其他rhGH改用生物仿制药rhGH的影响,这些担忧已得到缓解。对于那些需要rhGH治疗的儿童,生物仿制药rhGH是一种有效治疗方案。
参考文献:
López-Siguero JP, Pfäffle R, Chanson P, et,al.Ten years' clinical experience with biosimilar human growth hormone: a review of efficacy data.Drug Des Devel Ther. 2017 May 16;11:1489-1495. doi: 10.2147/DDDT.S130320. eCollection 2017.
识别微信二维码,添加生物制品圈小编,符合要求即可有机会进入抗体微信交流群
!














