
欢迎点击「PaperRss」↑关注我们!
蛋白质的泛素化修饰是一类具有多种效应的蛋白质翻译后修饰,与众多的生理过程和疾病密切相关。线性泛素化是一类新型的泛素化修饰,广泛参与炎症、抗入侵病原体的选择性自噬以及先天免疫相关的信号通路。
线性泛素链组装复合物(LUBAC)是目前发现的唯一一个介导线性泛素链合成的E3泛素连接酶,由催化亚基HOIP和两个调节亚基SHARPIN、HOIL-1L所组成
。尤其重要的是,LUBAC中任何一个亚基的功能缺失会在小鼠模型或人类身上引起炎症、免疫缺陷甚至胚胎死亡。已有的研究表明,单独的HOIP处于低活性状态,自身的UBA结构域与催化核心区域之间存在自抑制。HOIL-1L或SHARPIN的结合可以激活HOIP,从而有效地催化线性泛素链的合成,但是目前HOIP自抑制的结构基础,以及SHARPIN和HOIL-1L激活HOIP的分子机理依然未知。

近期
,中国科学院上海有机化学研究所生命有机化学国家重点实验室潘李锋课题组成功解析了HOIP
UBA结构域结合SHARPIN
UBL结构域的复合物的晶体结构,发现SHARPIN与HOIL-1L可以同时结合在HOIP的UBA结构域上的两个截然不同的位点,既可以单独、也能协同激活HOIP的酶活性。
系统的生物化学和酶学实验研究详细地揭示了HOIP的激活机制:SHARPIN或HOIL-1L的结合,改变了UBA结构域和催化核心区的相对取向,从而解除自抑制,并促进底物进入催化核心,加速线性泛素链合成。
该工作还清晰地解决了一个在以往研究中存在激烈争议的基本问题:HOIP的哪一个结构域直接结合了SHARPIN?上海有机所研究人员用蛋白质复合物结构和生物化学实验证实了是HOIP的UBA结构域,而非NZF2结构域与SHARPIN结合。SHARPIN与HOIL-1L协同结合HOIP还很好地解释了LUBAC复合物在细胞内存在的三种不同组合,以及对应的不同酶活性。该项研究工作以
Structural Insights into
SHARPIN-Mediated Activation of HOIP for the Linear Ubiquitin Chain
Assembly
为题,在线发表于Cell Reports(2017, 21, 1–10)。
该研究工作得到了中科院战略性先导科技专项(B类)、生命有机化学国家重点实验室,国家自然科学基金委、科技部、中组部青年千人计划和上海市科委的相关资助。(来源:
中国科学院上海有机化学研究所)
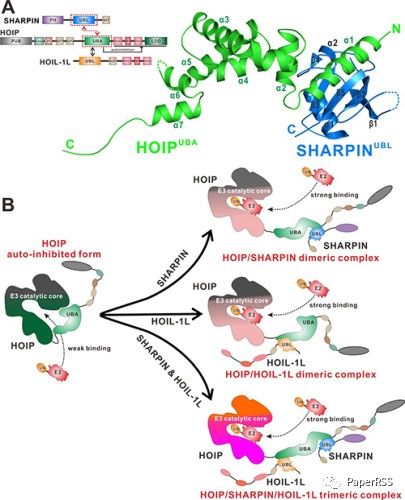
(A)SHARPIN,HOIP,HOIL-1L蛋白的结构域组成以及HOIP的UBA结构域结合SHARPIN的UBL结构域的复合物晶体结构;(B)在LUBAC复合物的三种组合方式中,SHARPIN和HOIL-1L可以单独或协同结合HOIP,促进底物(E2)的结合,激活HOIP的酶活性。
Cell Rep 2017 Oct;21(1):27-36
State Key Laboratory of Bioorganic and Natural Products Chemistry,
Shanghai Institute of Organic Chemistry, University of Chinese Academy of Sciences, Chinese Academy of Sciences, 345 Lingling Road, Shanghai 200032, People's Republic of China. Electronic address:
Abstract:
The linear ubiquitin chain assembly complex (LUBAC) is the sole identified E3 ligase complex that catalyzes the formation of linear ubiquitin chain, and it is composed of HOIP, HOIL-1L, and SHARPIN. The E3 activity of HOIP can be effectively activated by HOIL-1L or SHARPIN, deficiency of which leads to severe immune system disorders. However, the underlying mechanism governing the HOIP-SHARPIN interaction and the SHARPIN-mediated activation of HOIP remains elusive. Here, we biochemically and structurally demonstrate that the UBL domain of SHARPIN specifically binds to the UBA domain of HOIP and thereby associates with and activates HOIP. We further uncover that SHARPIN and HOIL-1L can separately or synergistically bind to distinct sites of HOIP UBA with induced allosteric effects and thereby facilitate the E2 loading of HOIP for its activation. Thus, our findings provide mechanistic insights into the assembly and activation of LUBAC.





