中国医药工业杂志
体内体外相关性的评价方法及应用
Evaluation and Application of in vivo-in vitro Correlation
包圆圆,张 琪,吴闻哲*
(中国医药工业研究总院药物制剂国家工程研究中心,上海 201203)
摘要:
体内体外相关性评价旨在建立药物制剂的体内生物学特性和药物制剂的理化性质之间的关系。体内体外相关性评
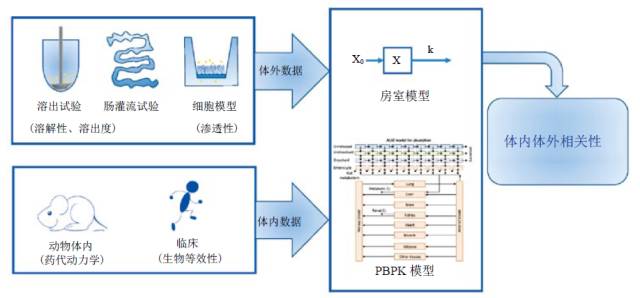
价的理论基础是生物药剂学分类系统,溶出度和渗透性等体外试验,以及基于动物和人体的体内试验是获取药物制剂理化性质和生物学特性的常用试验方法。本文从房室模型和生理药物动力学(PBPK)模型两方面系统地介绍了数学建模的流程和评价体系的应用;还综述了体内体外相关性在口服制剂改良中的应用和在非口服制剂评价中的最新发展。
关键词:
体内体外相关性;溶出度;渗透性;生理药物动力学模型;综述
20 世纪50 年代初,针对药物安全性和有效性
的研究表明,药物的体外释放特性会影响药物的体内生物利用度和疗效,从而提出了体内体外相关性( IVIVC) 的概念。在仿制药申报、药物新剂型开发、质量控制和生产变更中,常使用生物利用度(bioavailability,BA) 和生物等效性(bioequivalence,BE) 等指标来确保药物的一致性。由于临床试验成本高、耗时长、风险大,所以近年来FDA、EMA
等机构都致力于建立可靠的IVIVC 评价方法,以便
指导甚至替代临床试验。基于现今热点,本文综述了体内体外相关性的评价方法及应用[1—3]。
1 IVIVC 的评价体系
1.1 生物药剂学分类系统(BCS) 的发展
BCS 是IVIVC 评价体系的理论基础。该理论
于1995 年由Amidon 等首次提出,它将口服药物分成4 类,用以区分药物在胃肠道内的溶解性强弱和药物的透膜能力[4]。
根据传统的BCS 分类,BCS Ⅰ类药物如美托
洛尔、普瑞巴林等渗透性高、溶解性好,理论上其体内吸收应该表现良好,但试验测得的体内吸收数据与预测不符。进一步研究表明,药物的渗透性易受到细胞内转运体的影响,所以2005 年Benet 教授等将肝代谢、转运体等因素引入BCS 系统,用排泄物中药物代谢产物的回收率来表征渗透性,提出了基于体内药物处置的生物药剂学分类系统
(BDDCS),并用已有人体渗透性数据的29 种药物
对该分类方法进行验证,其分类准确率为93%,优于传统BCS 分类的准确率(65%~ 70% )。2010年EMA 采纳了BDDCS 的分类方法,2011 年Benet等用该分类系统对900 多种药物重新分类,成为IVIVC 研究中连接药物体外性质和体内过程的理论纽带[5—6]。
1.2 IVIVC 的体外试验
药物的体外特性主要是指药物制剂的理化特
性,包括药物的稳定性、粒度分布、亲脂性、渗透性和溶出速率等。总结近年的研究表明,溶出曲线测定和渗透性试验是IVIVC 评价体系中常用的体外试验方法。
1.2.1 溶出曲线
对于BCS Ⅰ和BCS Ⅱ类药物,溶出试验是预
测药物体内吸收的主要方法。各国药典中常用的体外溶出方法为转篮法和桨法,对于非常规剂型,如小规格固体制剂,可使用小杯法;微球等缓释制剂,可使用往复筒法;缓释制剂中低溶解度活性成分的测定,可使用流通池法;相比于往复筒法,美国药典(USP) 中的装置7往复架法,可以选配不同的制剂支架,用于测定非崩解的缓释制剂( 如透皮贴剂、渗透泵和动脉支架等) 的溶出行为;此外根据USP36-NF31,透皮制剂还可选用装置5( 桨碟法) 和装置6( 筒法)[7]。
1.2.2 渗透性试验
对于BCS Ⅲ类和BCS Ⅳ类药物,药物在吸收
部位的渗透性是其吸收程度的限速步骤。渗透性的体外测定方法主要有离体肠灌流法和细胞模型法。离体肠灌流法主要适用于口服制剂的渗透性测定,但该法易受生物样品个体差异性的影响。Caco-2 细胞模型及其衍生模型的适用范围则更为广泛,可用于测定鼻用制剂、栓剂、滴眼剂和透皮制剂的渗透性。由于Caco-2 细胞模型可以模拟主动转运、细胞旁路吸收和胞吞途径,所以它也可从细胞代谢层面考察口服药物在胃肠道的吸收程度[7—8]。
1.3 IVIVC 的体内试验
用于测定药动学数据的体内试验包括基于人
体的临床生物等效性试验和基于动物的药代动力学试验。
2 IVIVC 的建立方法
IVIVC 研究的最终目的是实现体外数据对体内
药动学过程的可预测性。将体内外试验测得的数据建立相关关系主要依赖于数学建模,主要方法有房室模型和生理药物动力学(PBPK) 模型。
2.1 房室模型与溶出条件的优化
房室模型是将机体视为一个系统,按照吸收、
分布、消除的特性将转运速率相似的部分视为同一室,是药动学分析中的抽象概念。根据房室模型理论,对药- 时曲线进行反卷积得到体内吸收曲线,再结合体外溶出数据,对二者进行线性回归,最后绘制体内吸收- 体外释放相关性曲线,得到相关系数R2[11]。通过房室模型建立体内体外相关性主要可用于筛选合适的体外溶出条件,从而通过体外试验控制药物的生产质量、评估仿制药与原研药的一致性。然而, BCS Ⅲ和BCS Ⅳ类药物体内吸收的限速步骤并非溶出速率,药物的体外溶出曲线难以与
体内数据建立相关关系,所以基于溶出试验提供的
体外数据、用房室模型建立相关关系的方法仅多用于BCS Ⅱ类药物。
2.2 PBPK 模型
由于低渗透性药物的限速步骤并非溶出速率、
非口服制剂的溶出方法不够完善、且抽象的房室模型与人体的解剖结构没有直接联系,按照房室模型反卷积得到的药物吸收数据较难与体外数据建立联系,Teorell 等于1937 年首先提出了PBPK 模型的设想[13]。PBPK 模型的核心在于设计一套针对某种制剂的模拟其体内过程的装置,然后利用模型药物已有的体内外数据来寻找相关性规律,再将找到的数学规律建立模型、设计软件,从而应用到对该类药物体内过程的预测中。基于数学理论的PBPK 模型对药物的剂型和BCS 分类均没有限制。
3 药物制剂中IVIVC 的应用
3.1 口服制剂与IVIVC
现有的研究表明:BCS Ⅰ类药物在体内能被快
速吸收,可直接用体外溶出数据代替临床试验数据,FDA 已允许部分该类药物在申报过程中申请生物等效性试验豁免;BCS Ⅲ和BCS Ⅳ类药物渗透性差,易受细胞代谢和肝脏代谢影响,体内外数据较难建立相关性,近年来有很多研究尝试通过建立可靠的PBPK 模型来建立IVIVC,但实际应用中还是以体内试验数据作为考察标准。总体而言,IVIVC 在口服制剂中的应用主要集中于BCS Ⅱ类药物[16]。
3.1.1 IVIVC 与BCS Ⅱ类药物的处方设计
对于已建立IVIVC 的BCS Ⅱ类药物,结合
质量源于设计(QbD) 的理念,IVIVC 可以用于指导该类药物制剂的处方优化。Xia 等用PBPK 模型分析了食物对BCS Ⅱ类药物的影响[ 17]。试验中的待测药物为pH 依赖型弱碱性药物NVS123,GastroPlus 软件预测的体内药动学数据表明当引入食物参数时,该药的生物利用度会显著提高。在随后进行的随机双盲临床试验中,观察到合并高脂类饮食志愿者的体内药动学曲线与体外预测一致( 误差小于30% )。进一步分析表明,将药物灌装于胶囊中或合并高脂类饮食服用时,能刺激胃肠道蠕动,减少弱碱性药物与胃酸的作用时间,所以该药物适合制成胶囊剂。
3.1.2 IVIVC 与BCS Ⅱ类药物的合理用药
改变BCS Ⅱ类药物的体外试验条件,利用已
建立的IVIVC 模型可预测相应的体内吸收效果,从而指导合理用药。Mercuri 等研究了硝苯地平速释胶囊的体内体外相关性[18]。体外溶出试验分别采用了转篮法、桨法、往复筒法和流通池法,使用了水、人工胃液( 根据USP38 配制pH 1.2 的无胃蛋白酶的人工胃液SGFsp、pH 1.6 的模拟禁食状态的人工胃液FaSSGFst)、人工胃液乙醇混合液( 乙醇含量47% )、人工胃液橙汁混合液(pH 3.4)、人工胃液橙汁乙醇混合液等作为溶出介质,得到多条溶出曲线;使用了1983 年Rämsch 测得的临床数据作为参考,反卷积得到体内吸收曲线;将多条溶出曲线与吸收曲线进行点对点的线性回归。分析相关系数R2的结果表明:由于难溶性药物的堆积,在水和人工
胃液条件下使用转篮法与桨法测得的溶出曲线不能
与体内数据建立相关性;在含有乙醇时药物的溶出速率略有加快,其中在50 r/min、人工胃液乙醇混合液的条件下,药物的吸收曲线与溶出曲线呈现指数相关(y=2.446 8×e0.035 6x);而在加入橙汁时,用4种溶出方法测得的溶出曲线均能与体内吸收曲线建立良好的相关性。所以,预测饮酒可能会促进硝苯地平的体内吸收,影响用药安全;而合用橙汁等酸性饮品不会对药物的吸收产生影响。
3.2 非口服制剂的IVIVC
由于肠道外给药时作用部位各异,缺少普适的
体外试验方法,非口服制剂的IVIVC 研究仅在肠道外缓释制剂和透皮制剂上略有突破[19]。
3.2.1 注射微球与埋植剂的IVIVC 研究
肠道外给药的聚合物微球或埋植剂是聚乳酸等
高分子材料包裹药物制成的缓释制剂,为了保证药物在体内缓慢稳定地释放,控制药品质量的体外试验需要与体内试验具有良好的数据相关性。常用的体外试验方法包括:采样分离法、膜透析法、流通池法和扩散池法。Jie 等用流通池法筛选了利培酮微球的制备工艺,将溶出曲线进行卷积、计算药物的体内药动学参数,对比家兔试验得到的体内数据,证明市售制剂Risperdal® 的AUC 体内外差异仅为0.08%;将家兔肌肉注射后的药- 时曲线进行反卷积,结合不同工艺制品中药物的体外释放曲线进行线性回归,得到的R2 在0.95 ~ 0.98 范围内,均为点对点的A 级相关[20]。
3.2.2 透皮制剂的IVIVC
透皮制剂的传统评价方法为扩散池法。
Mohammed 等用扩散池法和HPLC 法测定了烟酰胺的体外透皮吸收数据,与用共聚焦拉曼光谱测得的体内摄取数据进行对比分析,结果表明烟酰胺的皮肤渗透性在体内体外呈现良好的相关性[21]。对于透皮制剂的体外溶出试验,欧洲药典和USP 中收载了基于桨法的改进装置:在距搅拌桨(25±2)mm处放置一个碟型支架作为释放室。Yang 等利用













